本文以铝及其化合物和较活泼金属与酸反应的有关计算为例,分析简述数形结合思想的应用。
一、铝盐与强碱的反应
例1向30 mL 1 mol/L的AlCl3溶液中逐滴加入浓度为4 mol/L的NaOH溶液,若产生0.78 g白色沉淀,请用图示法计算加入的氢氧化钠的体积。
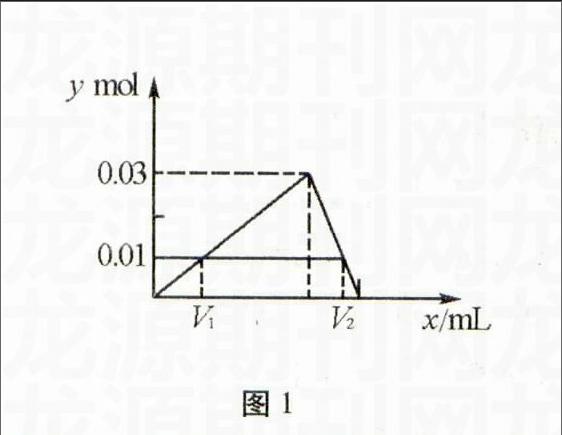
图1
解题思想如图1 x表示加入NaOH的体积,y表示沉淀的物质的量,从图中很快就可以得知加入的NaOH的体积有:
V1=30/4 mL;V2=110/4 mL。
反思如果不用画图的解题方法,学生在刚开始学习这部分知识时很容易只考虑第一种情况,忽视将铝离子沉淀完全,然后沉淀部分溶解的情况。但是学生如果画了图,图中曲线的交点非常明确告诉学生这里有两个值。
变题练习1将AlCl3溶液和NaOH溶液等体积混合,得到的沉淀物中和溶液中所含的铝元素的质量相等,则原AlCl3溶液和NaOH溶液的物质的量浓度之比可能是,画图解题(B、D)。
A.1∶3 B. 2∶3 C. 1∶4 D. 2∶7
二、偏铝酸盐和酸反应
例2向100 mL 0.25 mol·L-1的AlCl3溶液中加入金属钠完全反应,
(1)恰好生成只含NaCl和NaAlO2的澄清溶液,则加入金属钠的质量是多少?
(2)得到沉淀最大值是需金属钠的物质的量是多少?同时生成氢气标准状况体积多少升?
(3)在(1)的溶液中滴加盐酸,如果得到沉淀最大值时需HCl的物质的量多少?如果将一半铝元素生成沉淀,则需HCl的物质的量又是多少?
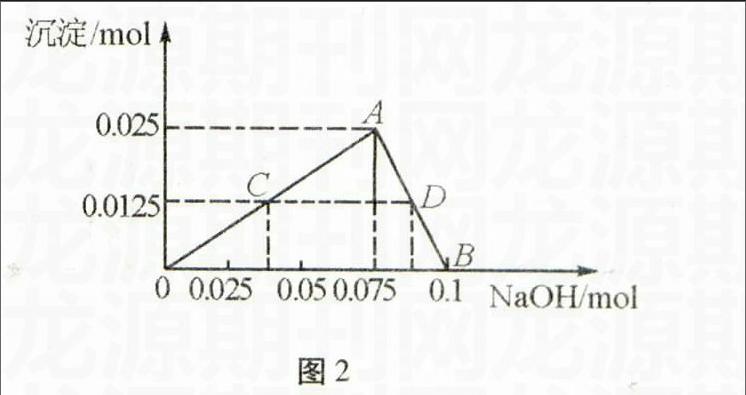
图2
解题思想(1)(2)应用守恒法可求解。(3)以横坐标表示氢氧化钠的物质的量,纵坐标表示得到沉淀的物质的量作图(见图2)。图中A点是沉淀最大值点,对应横坐标的氢氧化钠物质的量
为0.075 mol,此时需要金属钠的物质的量为0.075 mol;B点是生成只含NaCl和NaAlO2的澄清溶液点,对应横坐标氢氧化钠的物质的量为0.1 mol,金属钠的物质的量为0.1 mol;C和D点对应的纵坐标是沉淀一半铝元素的点,同时也可以在横坐标上找到加入盐酸反应的氢氧化钠的物质的量。再利用元素物质的量守恒原理很快就可以得到各小题答案:
(1)Na的物质的量是0.1 mol;质量为2.3 g。
(2)沉淀最大时,钠的物质的量是3×0.025=0.075mol,产生标准状况氢气:0.0375×22.4=0.84L;
(3)铝元素一半沉淀时加入盐酸可以从图中BD段和BC段
对应横坐标的物质的量进行寻找。因此得到沉淀一半时加入盐酸分别是:0.0125mol和0.0625mol。
反思:在教学中不采用数形结合思想,有几个方面会导致学生思维混乱:①该题中的反应较多;学生不知从何入手。②开始是从金属钠出发,而且第一小题问题是直接到NaCl
和NaAlO2,跨度有点大;③题中提出问题:反加盐酸,学生思维转变不到位等等。这样学生的解题是在写出很多方程式的基础上进行,繁、乱、不全面是必然的。
当然对题中信息处理作图是一个需要学生体现能力的过程,学生必须要对题中信息进行处理,找到可以作图的物理量,而且可以通过图中横纵坐标代表的物理量将题目信息体
现出来,题目问题体现出来,这样才能离答案越来越近。这是这一思想解题的关键。教师必须认真引导,学生练习掌握。
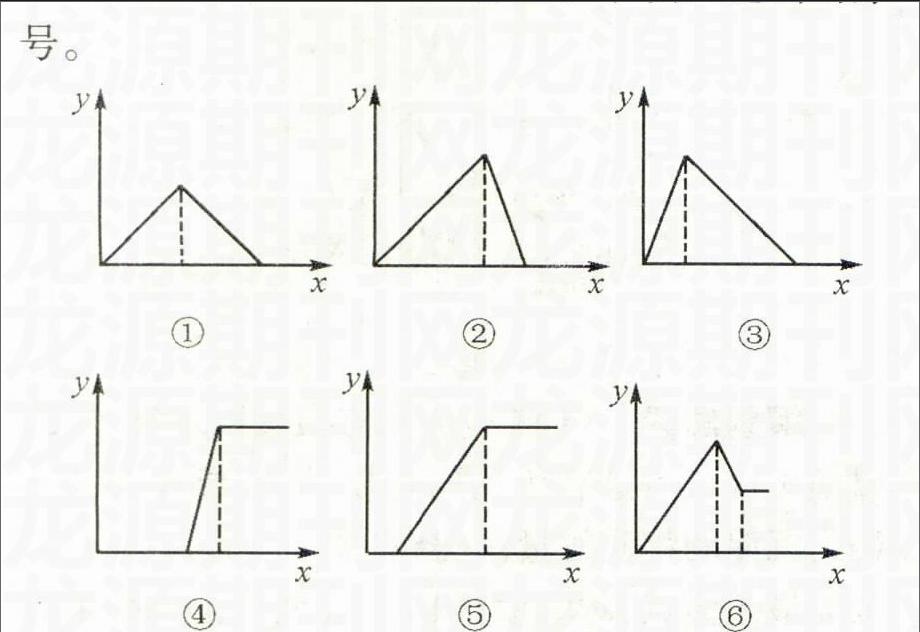
变题练习2在下列各选项中填入适当的序号。
A.x轴代表在搅拌情况下向NaOH溶液中加入铝盐物质的量,y轴代表混合物中沉淀量的变化,那么该坐标图应是 ④ ;
B.x轴代表在搅拌情况下向铝盐溶液中加入NaOH物质的量,y轴代表混合物中沉淀量的变化,那么该坐标图应是 ② ;
C.x轴代表在搅拌情况下向偏铝酸钠溶液中加入盐酸物质的量,y轴代表混合物中沉淀量的变化,那么该坐标图应是 ③ ;
D.坐标图 ⑥ 可以表示在搅拌情况下向MgCl2和AlCl3的混合溶液中加入NaOH物质的量(x轴)和产生沉淀量(y轴)的变化关系。
图3
变题练习3把镁铝合金用稀硫酸溶解,加入氢氧化钠溶液的体积与生成沉淀的质量关系如图3,则合金中镁和铝的质量比是(B)。
A.2∶3 B. 8∶9 C.4∶3 D.4∶9
三、较活泼金属和酸反应的题型
例3有质量都为A g的金属钠、镁、铝、铁四种金属,分别和0.5 L 2 mol/L的稀盐酸反应,试讨论A的不同取值范围时, 生成氢气体积大小的顺序。(同温同压)
解题思想对题中信息分析以横坐标代表金属质量,纵坐标代表生成氢气的物质的量作图(见图4)。图中OA段是铝和盐酸反应曲线;OB段是镁和盐酸反应的曲线;OC直线是钠和盐酸反应的曲线:OD段是铁和盐酸反应的曲线。
图4
作图的思路先计算酸完全反应是消
耗各金属的质量,铝是9 g,镁是12 g,钠金属活泼,酸完全反应消耗钠23 g,但钠会继续和水反应,因此曲线是OC的直线延长;铁是28 g。
图示分析:从图中曲线可知:
(1)当0镁>钠>铁;
(2)当12≤A<23时,放出氢气的情况是:铝=镁>钠>铁;
(3)当A=23时,放出氢气的情况是:铝=镁=钠>铁;
(4)当23镁=铝>铁;
(5)当28≤A时,放出氢气的情况是:钠>镁=铝=铁。
反思此类题型主要是比较的物质有多种,而且讨论的区间有交叉的区域,如果学生单从化学方程式的反应比例进行讨论,会出现:①讨论的物质多,思维容易乱;②讨论区间交叉处不能理清;③容易漏某些讨论区间等问题。因此,这时解题思想的引导对解决此类题型非常重要,而且数形结合思想对学生的掌握没有障碍,只要教师适当指点,同学们很容易学会解题。
此类题型作图的关键是:要找准横纵坐标的物理量,不然图作出后,图中曲线不具有解决题中问题的功能。这是教师在指导学生解题时要特别强调的。
(收稿日期:2014-09-10)
- 谈如何培养小学生数学创造性思维能力
- 微课运用于小学数学拓展课中的策略浅析
- 浅谈初中音乐欣赏课教学方法
- 关于初中地理课堂中引入“生活化”教学的研究
- 探讨情境教学在初中历史教学中的应用
- 生命教育在初中生物教学中的有效渗透
- 遇见美好
- 在小学数学教学中培养学生良好的学习习惯
- 浅析如何构建高中生物高效课堂
- 小“角度”,大文章
- 激活学生经验,让学习真正发生
- 初中体育教学中学生伤害事故防范策略探讨
- 职高语文教学对学生实施多元性评价的路径探究
- 智障儿童生活语文教学精准施策探析
- 探究职高电子信息工程专业学生技能的培养
- 教育惩戒需要走向规范化建设
- 提高中职旅游管理专业服务礼仪教学实效的对策
- 高中生物核心素养的内涵与培养策略分析
- 思维导图在高中英语复习课中的应用探析
- 初中物理学困生成因分析及转化策略研究
- 高中语文教学中传统文化的渗透分析
- 基于学生核心素养的中小学数学课程衔接研究
- 关于创新开展校园课外体育活动的探索
- 促进义务教育均衡发展
- 浅谈高中数学学困生的形成原因及解决措施
- going along
- going-around
- going back
- going by
- going concern
- goingconcern
- going-down
- going down
- goinger
- goingest
- going forward
- going in
- going off
- go in / go into sth
- going on
- going out
- going over
- going-over
- going places
- going rate
- goingrate
- going round
- goings'
- goings
- goings on
- 抓狂
- 抓狗儿子看狗母
- 抓猫
- 抓瓜丝
- 抓生产
- 抓痒
- 抓痒处
- 抓皮
- 抓着东西往上爬
- 抓着荷叶摸藕
- 抓着葫芦当瓢打
- 抓着葫芦当瓢打——昧了良心
- 抓着鸡毛当令箭
- 抓瞎
- 抓破
- 抓破纸灯笼
- 抓破绽
- 抓破脸
- 抓破脸皮
- 抓碴儿
- 抓空子
- 抓窍门
- 抓管理上等级的宣传方法
- 抓粒豆
- 抓紧