张运飞 李红英
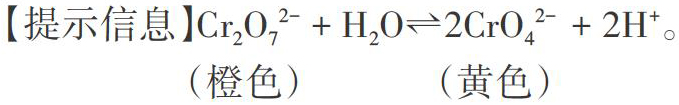
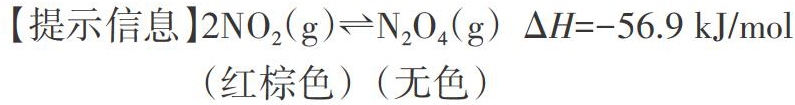
[摘? ?要]化学之美,美在实验、美在真实、美在和谐。通过化学实验教学,培养学生科学探究意识,落实化学学科核心素养,让学生感受化学之美、生活之美。
[关键词]实验之美;化学平衡;影响条件;勒夏特列原理
[中图分类号]? ? G633.8? ? ? ? [文献标识码]? ? A? ? ? ? [文章编号]? ? 1674-6058(2020)29-0069-03
《化学平衡》是人教版高中化学选修4《化学反应原理》第二章第三节的教学内容,是高中二年级选学理科学生需要学习的重点知识。根据新课程标准的要求,结合教学参考用书的建议,该部分内容的教学安排5课时。本节课是第2课时,教学重点为:影响化学平衡移动的条件探究及勒夏特列原理的归纳总结。
一、教学背景
1.课程标准
对影响化学平衡移动因素的学习要求,新课程标准中使用的行为动词为“了解”,具体为:通过实验探究,了解浓度、压强、温度对化学平衡状态的影响。新课程标准明确要求“探究影响化学平衡移动的因素”为学生必做实验。在开展“外界条件对化学平衡的影响”实验探究活动中,发展学生的演绎推理、系统假设等思维能力。
2.学情分析
在必修2《化学反应的速率和限度》一节中,学生对“化学平衡的建立”有了一定的了解,知道可逆反应具有一定的反应限度,了解了化学反应的限度决定了反应物在该条件下的最大转化率。学生初步学习了化学平衡理论知识,本节课将从实验的角度让学生体验外界条件对化学平衡状态的影响。
二、教学节选
教学环节1 演示实验,发现规律
【演示实验】向大试管中加入约8 mL蒸馏水,滴加4滴FeCl3溶液(颜色很淡),滴加2滴0.01 mol/L KSCN溶液,静置。
【学生活动】学生仔细观察实验现象:KSCN溶液滴入后,立刻变为红色,且红色逐渐扩散开来。现象很美,学生惊叹。
【教师提问】FeCl3溶液中滴加KSCN溶液后溶液颜色为何变红?能否用化学方程式表示该变化过程?请尝试在速率关系图上分析该变化过程。
【学生活动】利用所学知识解释观察到的现象:溶液变红色是由于Fe3+与SCN-反应生成了Fe(SCN)3(红色),反应的离子方程式为Fe3++3SCN-[?]Fe(SCN)3;画出速率时间关系图,最终溶液红色不再改变,说明反应达到化学平衡状态。
【演示实验】用长滴管吸取大试管中的红色液体于两支小试管中(各2滴管),分别向其中滴加1滴1 mol/L KSCN溶液和3滴饱和FeCl3溶液,与大试管中的液体颜色对比。
【教师提问】溶液红色加深,说明哪种微粒的浓度发生了变化?如何变化?加入的是什么微粒?浓度又有何变化?所用溶液的浓度和数量的意义何在?
【学生活动】思考,交流,汇报:两支小试管中溶液红色都加深了,说明Fe (SCN)3溶液浓度都发生了改变,且都是增大。第一支小试管加入的是1滴1 mol/L KSCN溶液,与未加入前相比,KSCN溶液刚加入的瞬间,SCN-浓度增大,溶液红色加深,说明Fe3+和SCN-发生反应继续生成Fe (SCN)3,SCN-浓度在刚加入的瞬间增大后又因反应消耗而降低。第二支試管中加入的是3滴饱和FeCl3溶液,与未加入前相比,FeCl3溶液刚加入的瞬间,Fe3+浓度增大,溶液红色加深,说明Fe3+和SCN-发生反应继续生成Fe (SCN)3,Fe3+浓度在刚加入的瞬间增大后又因反应消耗而降低。画速率时间关系图,分析速率图。
【演示实验】分别向上述两支小试管中各滴加2滴0.01 mol∕L NaOH溶液。
【学生活动】观察现象,思考,汇报:滴加2滴0.01 mol∕L NaOH溶液后,溶液红色变浅。
【教师提问】溶液红色为何变浅?说明什么问题?
【学生活动】加入2滴0.01 mol∕L NaOH溶液后,OH-会消耗溶液中的Fe3+,Fe3+浓度降低后,化学平衡随之被破坏,并向着生成Fe3+的方向移动。画速率时间关系图,分析速率图。
【归纳总结】旧的化学平衡被破坏,建立新的化学平衡,此过程被称为化学平衡状态的移动,简称平衡移动。
其他条件不变,增大反应物浓度,平衡正向移动;减小反应物浓度,平衡逆向移动。
设计意图:本环节从学生非常熟悉的氯化铁溶液与硫氰化钾溶液反应变红色的实验入手,降低学习门槛,激发学生兴趣。学生认真观察实验现象,从理论的角度分析宏观现象背后蕴含的微观本质,并画出速率时间关系图,归纳出本节课的第一个规律:在其他条件不变时,改变反应物浓度,化学平衡随之发生改变。本环节重在培养学生的“宏观辨识与微观探析”化学学科核心素养。
教学环节2 扩大范围,验证规律
【教师提问】其他条件不变,减小生成物浓度,或增大生成物浓度,平衡是否移动?如果移动,方向如何?
【提示信息】Cr2O72-? + H2O[?]2CrO42-? + 2H+。
(橙色)? ? ? ? ? ? ? (黄色)
【学生活动】小组交流讨论,根据所给信息设计实验。
【学生实验】取1支试管,向其中加入5 mL 0.1 mol∕L K2Cr2O7溶液,再滴加5~15滴浓H2SO4,溶液由橙黄色变为橙色;取1支试管,向其中加入5 mL 0.1 mol∕L K2Cr2O7溶液,再滴加5~15滴6 mol∕L NaOH溶液,溶液由橙黄色变为黄色。
【教师提问】加入浓H2SO4和NaOH溶液后,K2Cr2O7溶液颜色发生改变,原因是什么?
【学生活动】思考,交流,汇报:加入浓H2SO4后,溶液中的H+浓度增大,而化学平衡向着H+浓度减小的方向移动,Cr2O72-浓度增大,溶液由橙黄色变为橙色;加入NaOH溶液后,溶液中的H+与OH-反应,H+浓度减小,平衡正向移动,CrO42-浓度增大,溶液由橙黄色变为黄色。画速率时间关系图,分析速率图。
【教师提问】当浓度发生变化时,可逆反应是如何面对浓度变化的呢?
【学生活动】思考,交流:通过平衡移动减弱浓度变化带来的影响。
【归纳总结】其他条件不变,增大反应物浓度或减小生成物浓度,平衡正向移动;减小反应物浓度或增大生成物浓度,平衡逆向移动。
设计意图:上一环节从反应物浓度的变化角度进行实验探究,本环节则从生成物浓度的变化角度进行实验探究。学生根据所给信息、设计实验、交流讨论、优化实验方案、预测实验现象、完成实验验证。本环节重在培养学生的“科学探究与创新意识”化学学科核心素养。
教学环节3 学以致用,推广规律
【教师提问】化学反应要么是吸热反应,要么是放热反应,改变温度,化学平衡状态会改变吗?如果会,做何改变?
【提示信息】2NO2(g)[?]N2O4(g)? ΔH=-56.9 kJ/mol
(红棕色)? (无色)
【教师活动】展示“二氧化氮—四氧化氮”球。
【学生活动】小组交流讨论,结合所给信息,设计实验。
【学生实验】取3个“二氧化氮—四氧化氮”球。将其中1个放入冰水中,气体红棕色变浅;将其中1个放入热水中,气体红棕色加深;第3个常温放置,气体颜色不变。
【师生活动】师生归结:温度不同,气体颜色不同。请学生分析温度对平衡的影响,画出速率时间关系图,分析速率图。
【教师提问】当温度发生变化时,该可逆反应是如何变化的呢?
【学生活动】通过平衡移动减弱温度变化带来的影响。
【归纳总结】其他条件不变,升高温度,平衡向吸热方向移动;降低温度,平衡向放热方向移动。
设计意图:本环节对温度这一影响化学平衡的因素进行实验探究,验证温度对平衡状态的影响。学生根据所给信息设计实验,从理论角度分析现象背后蕴含的微观本质,并画出速率时间关系图,归纳出本节课的第二个规律:在其他条件不变时,改变温度,化学平衡随之发生改变,并向着能够减弱这种改变的方向移动。本教学环节注重培养学生的类比及推理意识。
教学环节4 归纳总结,提炼原理
【教师提问】同学们,刚才我们通过实验探究了解到当其他条件不变时,改变温度或改变浓度会对化学平衡状态带来影响,也知道了具体有何影响。那么对于有气体参与的已经达到平衡状态的可逆反应,改变压强,平衡会移动吗?如果会,如何移动呢?
【学生活动】交流,讨论,汇报:根据刚才浓度及温度对平衡移动的影响,类比出对有气体参与的已经达到平衡狀态的可逆反应,改变压强,平衡将向着减弱这种改变的方向移动。
【师生活动】结合浓度与温度的改变对平衡状态的影响,将归纳总结进一步完善扩大,得到勒夏特列原理。交流、分享对勒夏特列原理的理解及其适应范围。
【师生感悟】多么神奇的可逆反应!外在,有非常美丽的实验现象;内在,当外界条件发生改变时,通过平衡移动来减弱外界的影响。同学们,我们的生活何尝不是如此呢?平衡之美,改变之美,让改变发生,让梦想成真!
设计意图:本环节依据前面浓度及温度对化学平衡的影响,类比推理出有气体参与的已经达到平衡状态的可逆反应,改变压强,平衡将向着能够减弱这种改变的方向移动。结合温度、浓度及压强对化学平衡的影响,提炼出经验规律,也就是勒夏特列原理。本环节重在培养学生的“变化观念与平衡思想”“证据推理与模型认知”化学学科核心素养,增强学生的类比及推理意识。
三、教学反思
笔者调查发现,随着新课程标准的颁布实施,中学化学越来越突出实验教学,但现阶段的实验教学似乎进入了一个误区,不少教师一味地追求数字化实验、创新型实验等“高大上”的实验,而忽略了传统的“试管实验”。“高大上”的实验教学看似更适应时代潮流,但有的时候不可避免地会将实验教学复杂化。本节课,涉及的实验均来自于教材中的演示实验,仪器简单、药品用量少、实验现象明显。学生动手实验,观察现象,由衷地感叹实验之美、化学之美及生活之美。当学生发现自己归纳的化学平衡状态影响规律竟然和著名的勒夏特列原理相同,本节课的情感释放瞬间达到高潮,学生自发地鼓起掌,为自己鼓掌,也为化学鼓掌,当下课铃声响起的时候,学生依然舍不得结束课程,意犹未尽。小实验,大智慧;小故事,大情怀。在以后的化学教学中,我们要坚守实验教学,让学生感受化学之美。
[? ?参? ?考? ?文? ?献? ?]
中华人民共和国教育部.普通高中化学课程标准(2017年版)[S].北京:人民教育出版社,2018.
(责任编辑 罗? ?艳)
- 公路隧道灾害事故分析及其风险评价
- 房屋建筑材料质量检测与控制研究
- 对建筑施工现场管理的相关探讨
- 对市政工程施工现场管理工作的探讨
- 工程管理组织内部知识共享建立及影响因素识别分析
- 建筑工程项目管理创新探究
- 论建筑工程施工中的精细化管理
- 广电系统内建筑工程安全管理的薄弱环节及其应对措施
- 开展测绘工程监理的几点思考
- 建筑工程管理的重要性与创新方法研究
- 浅谈民用建筑工程造价管理与控制措施
- 新型绿色建筑工程造价预算与成本控制分析
- 城市道路施工管理方法初探
- 建筑经济与生态经济的互动性机制探究
- 城市轨道交通工程建设项目管理的研究
- 面向服务的数字国土资源管理运用
- 虚拟现实技术在工程管理中的应用
- 浅谈建筑施工现场管理
- 探讨建筑施工项目的过程施工质量控制措施
- 论加强建筑造价和结算审计管理的对策
- 城乡一体化背景下绿色建筑产业化发展对策研究
- 试论施工单位成本精细化管理的突出问题及对策探讨
- 基于BIM技术的建筑与装饰工程造价控制分析
- 地质灾害的治理分析
- 土木工程施工中节能环保技术探析
- serenade
- serenaded
- serenader
- serenaders
- serenades
- serenading
- serene
- serened
- serenely
- sereneness
- serenenesses
- serener
- serenes
- serenest
- serening
- serenity
- sergeant
- sergeants
- sergeantships
- sergt
- serial
- serial bonds
- serialbonds
- serialentrepreneur
- serial entrepreneur
- 轻恬
- 轻悄
- 轻悄悄
- 轻悍
- 轻悠悠
- 轻惰
- 轻意
- 轻意招惹,自取其辱
- 轻慢
- 轻慢、鄙弃的样子
- 轻慢上司的命令
- 轻慢下属
- 轻慢不拘
- 轻慢不敬
- 轻慢不逊的话
- 轻慢世事
- 轻慢亵渎
- 轻慢他人
- 轻慢侮弄
- 轻慢侮辱
- 轻慢倨傲
- 轻慢凌侮
- 轻慢嘲笑
- 轻慢并加以戏弄或欺负
- 轻慢并戏弄或欺负