摘要:将“趣味化学实验”引入课堂教学是提高学生学习兴趣、启迪学习灵感的有效途径。围绕高中化学“气体的性质”这一章节,在原有教材实验的基础之上设计优化了“氨气与氯化氢”、“硫化氢与二氧化硫”、“氨气与氯气”、“喷泉实验”四个适合课堂演示的趣味性实验项目,介绍了实验的设计思想、内容及特色,并对其教学效果进行了实践和分析。
关键词:气体反应;趣味化学实验;实验优化设计
文章编号:1005–6629(2017)1–0068–04 中图分类号:G633.8 文献标识码:B
孔子曰:“知之者不如好之者,好之者不如乐之者。”这句话告诉我们,兴趣其实是最好的老师,一个人一旦对某一事物或某种活动产生兴趣,就会全身心投入其中。因此,课堂教学中,教师除了讲授基础知识、基本技能外,更重要的一点是要培养学生的学习兴趣,激发其求知欲望,引导其进入一种积极的、主动的学习状态。化学是一门以实验为基础的科学,本文以气体反应内容为例,结合高中化学的课堂教学,谈谈笔者利用演示实验激发学生学习兴趣的教学实践。
1 气体反应的实验设计
“气体的性质”是高中化学中重要的教学内容,也是教学难点之一[1],因为绝大多数气体无色无形,看不见摸不着,如何生动而又形象地描述气体的性质?不少教师会利用实验进行辅助性课堂教学[2],但实验应怎样设计才能吸引学生,激发其学习热情?笔者认为以下几点非常关键。一是所选内容在课堂上可当场操作演示,且实验现象要明显有趣,给学生以直观感受;二是实验过程要有悬念,能激起学生的好奇心,启迪学生学习的灵感,引发探究的欲望;三是由实验引出诸多问题让学生思考,留给他们进一步想象和拓展的空间。现举数例如下。
2 实验案例
2.1 氨气与氯化氢的反应
现行上海市高中化学教材中对氨气与氯化氢的反应是这样描述的[3]:取两根玻璃棒,分别在浓氨水及浓盐酸里蘸一下,然后将两根玻璃棒逐渐靠近但不接触,这时可以观察到在两根玻璃棒之间有白烟产生(图1a)。按照教材教师在课堂上演示了氨水与浓盐酸挥发然后再发生气相反应的过程,但从实际教学效果来看,留给学生的印象并不深刻。因此笔者将实验进行了如下改进:在一根长玻璃管两端塞上棉花,分别向两端同时滴入浓氨水和浓盐酸,马上用橡皮塞塞住,半分钟之后就可以看到白烟在玻璃管内生成;再仔细观察,会发现白烟的位置不在管的中央,而在靠近浓盐酸的一端(图1b)。通过改进的演示实验教学,学生理解了3个知识点:①氨水与浓盐酸分别在玻璃管的两端,距离较远,挥发扩散后才发生反应;②气体的扩散速率与气体式量有关(Graham扩散定律),在同温同压下气体扩散速度与气体密度的平方根成反比,因氨气的密度小,扩散速度快,故而反应在靠近浓盐酸的一端进行;③氨气和氯化氢反应生成固体氯化铵(白烟)。与教材实验相比,改进后的实验教学效果明显好于前者。

2.2 硫化氢与二氧化硫的反应
二氧化硫和硫化氢反应,教材里是这样设计的[4]:取一瓶二氧化硫和一瓶硫化氢气体(图2a),把两瓶气体混合,观察瓶壁上有什么现象,结论是瓶壁有浅黄色固体和水珠出现,这是一个定性实验。
笔者对教材实验装置进行了改进设计,采用矿泉水瓶收集两种气体(图2b)。在课堂演示时,将两瓶子撤去盖子后对接迅速用胶封住瓶口,按照Graham气体扩散定律,式量小(密度小)的气体扩散速率快,因此浅黄色固体和水珠应出现在盛装二氧化硫气体的瓶内,但实验结果恰恰相反,产物主要集中在硫化氢瓶内(图2c)。这一反常现象一下子引起了學生的兴趣,大家各抒己见。经过分析,得出了造成此实验现象的原因是:硫化氢与二氧化硫发生氧化还原反应(2H2S+SO2→3S↓+2H2O),反应物消耗比为2:1,即在同等条件下硫化氢瓶中的压强减小更快,由于压差的存在,导致二氧化硫气体被“吸入”硫化氢瓶中,并在其中生成硫和水。
此时,学生又进一步提出了疑问:既然硫化氢与二氧化硫反应使系统的压力下降,为何瓶子没有变形呢?再对实验过程中各环节进行检查和分析,得出了原因。由于实验中采用口香糖胶来封瓶口,导致装置的气密性还不够好。针对此缺陷再进行改进后,用插有短玻璃管的橡皮塞代替塑料瓶盖,两玻璃管口用乳胶管连接,中间夹以弹簧夹(图2d)。实验开始后松开弹簧夹,反应经数分钟或数小时(取决于玻璃管内径的粗细),可以看到玻璃管中生成黄色的硫,同时瓶子慢慢变瘪。以上实验结果环环相扣,过程充满悬念,给学生留下深刻印象。

2.3 氨气与氯气的反应
高三的教材告诉我们,氨气与氯气存在两个反应:
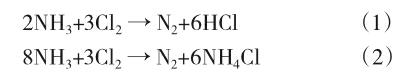
反应(1)中氨气与氯气的计量系数比为2:3,即在温度、压力相同时,反应600mL的氯气需要消耗400mL的氨气。反应(2)中的系数比为8:3,即反应600mL的氯气需要消耗1600mL的氨气。于是有不少学生猜测,只有当氨气的量超过400mL时,才会发生第二个反应生成氯化铵。那么实际情况真是如此吗?只有反应(1)进行完全了才进行反应(2)?
我们进行了演示实验。如下图3,取两个体积不同的矿泉水瓶,600mL的大瓶储存氯气,350mL的小瓶储存氨气,两瓶子用乳胶管相连。弹簧夹一经打开,在玻璃管及瓶中立刻产生白烟,说明反应(1)(2)几乎是同时发生的。与实验2.2相似,几分钟后,瓶子变瘪。

对此实验现象和结果进行讨论和分析后,得出了如下解释:氨气首先与氯气反应生成氯化氢,酸性的氯化氢气体又与碱性的氨气立即快速反应生成氯化铵;据实验现象还可得出后者反应速率远大于前者的结论。因此,不待反应(1)中的氯气消耗完,反应(2)已开始。这一演示实验生动地描述了“反应速率”这一概念,也给了学生一个启发,很多化学实验的结果和我们当初的想象是不一样的[5]。
2.4 喷泉实验
喷泉实验是高中化学实验中关于氨气性质的经典实验[6,7],教材中其装置如图4所示。当打开活塞时,烧瓶内的氨气迅速溶于水生成氨水(NH3+ H2O→NH3·H2O→NH4++OH-),在烧瓶内外产生压差,压差将烧杯中的液体压入烧瓶中形成喷泉,由于氨水使酚酞变红,所以喷泉呈红色,非常美丽。

由于原理比较简单,笔者便尝试着请学生对喷泉实验进行创新改进,并在其间插入诸多问题让其思考。例如,问题1,如果将烧瓶中的气体换成氯气,还能形成喷泉吗?学生经过思考后很快就回答不能,因为氯气在水中的溶解度较小。接着教师再提出问题2,那么能否设法提高氯气的溶解度呢?经过热烈讨论,学生给出了答案,采用氢氧化钠溶液代替水。
新实验采用如下设计:以氯气取代氨气,把胶头滴管中的水换成氢氧化钠溶液(浓度较高),在烧杯中也加入含酚酞的氢氧化钠溶液(浓度较低),溶液呈粉红色。实验中将胶头滴管中的氢氧化钠挤入圆底烧瓶,轻轻晃动圆底烧瓶片刻,再打开弹簧夹,因烧瓶内的氯气与氢氧化钠发生反应形成负压:Cl2+2NaOH→NaCl+NaClO+H2O,烧杯中的液体被压入瓶内,成功地完成了氯气的喷泉实验。此时观察仔细的学生注意到,喷泉的颜色由原来的粉红色变成了无色。这又是一个非常好的知识引入点。教师继而引入问题3,溶液为何褪色?经过启发,学生分析褪色的原因可能有两个:①氯气与氢氧化钠反应,消耗了氢氧化钠;②氯气与氢氧化钠反应生成次氯酸钠,生成的次氯酸氧化酚酞。原因究竟是哪一个?还是以实验事实来作答。利用烧瓶中的液体进行如下分析实验:在液体中滴入氫氧化钠,如果溶液再次变红,则可推断是原因①;或在液体中加入酚酞,如果溶液重新变红,则证明是原因②。实验结果显示,溶液中加入酚酞后才会再次显粉红色,说明使溶液褪色的真正原因是由次氯酸氧化酚酞所致。在本实验中,教师对实验加以变换,以问题为导向,通过对问题的层层剖析,结合现场操作演示,将氨气、氯气的物理及化学性质有趣地展现在学生面前。
3 结语
本文对四个原有教材实验进行了设计优化和拓展深化,将“氨气与氯化氢”、“硫化氢与二氧化硫”、“氨气与氯气”、“喷泉实验”四个反应作为课堂演示实验,并以问题为导向,通过递进式提问及对问题的层层剖析,结合现场演示,将几种气体的物理及化学性质生动直观地展现在学生面前。这些教学手段活跃了课堂氛围,激发了学生思维,巩固了所学知识,拓展了学生认知,提高了学习兴趣,收到了良好的教学效果[8,9]。同时需要提醒的是,上述气体均属于有毒有害气体,实验操作时须做好必要的防范措施,这一点也是为了对学生进行安全教育和环保意识的唤起。化学是以实验为基础的自然科学,化学反应往往伴随有色彩、形态、声音、能量、气味等变化,只要我们精心设计,将这些丰富多彩的实验内容引入课堂教学,就能激发学生的兴趣并使其成为学习的动力,让学生在愉悦、活泼的课堂氛围中潜移默化地接受教育,达到“润物细无声”的教学效果。
参考文献:
[1]王家昌.浅谈混合气体推断的起点与落点[J].数理化学习,2015,(12):42~43.
[2]魏书彬,陈加柱.浅议高中化学实验教学的问题与对策[J].化学教学,2015,(11):75~78.
[3][4]上海市中小学课程改革委员会编.化学(高中一年级第二学期)[M].上海:上海科学技术出版社,2012:23,6.
[5]钱胜.例谈克服教学中的“想当然”[J].化学教学,2013,(7):17~19.
[6]程萍,李美星.从实验学化学——氨的教学设计及思考[J].化学教学,2013,(6):60~63.
[7]吕亚娟,曾有德,张力,陈洁.喷泉实验的理论分析与实验研究[J].化学教育,2013,(10):75~77.
[8]王海燕,刘波.氯化钴溶液变色实验的定量控制及相关趣味实验介绍[J].化学教学,2008,(10):5~7.
[9]叶燕珠,吴新建等.初中化学趣味实验及相关探究课题[J].化学教学,2015,(1):52~54.
- 浅谈小学数学课堂练习设计的有效性
- 刍议小学数学学困生作业批改的策略
- 小学高年级数学教学中习题“变式”的应用探究
- 农村小学数学个性化作业教学分析
- 浅谈小学低年级数学有效课堂教学的激励性评价
- 数学日记在小学高年级课堂评价中的实践研究
- 义务教育小学阶段英语课堂教学有效性的评价标准研究
- 基于核心素养的小学语用实践作业探究
- 优化语文作业设计,提升小学生语文学习质量
- 小学课堂注意力现状调查与策略探究
- 小学生日常卫生习惯存在的问题及解决策略
- 动手能力在小学美术教学中的培养
- 在小学美术教学中培养学生想象力和创新能力的策略
- 论小学体育教学中学生素质能力的提高
- 小学体育教学中学生创造性思维的训练
- 小学数学教学中估算意识的培养探讨
- 小学语文有向开放之互动式课堂模式的构建和应用探究
- 浅析小学体育教学中学生竞争与合作意识的培养策略
- 小学低年级数学计算能力培养策略探究
- 听出乐趣 听出效率
- 小学数学教学中如何激发学生学习数学的兴趣
- 在小学数学教学中如何培养学生的思维能力
- 小学数学教学中独立思考能力的培养
- 小学数学教学中趣味性渗透策略研究
- 小学数学能力培养的教学策略
- short²
- short³
- short¹
- shot
- shot-blast
- shotgun
- shotgun marriage
- shotgunned
- shotgunner
- shotgunners
- shotgunning
- shotguns
- shot/gunshot
- shotgun wedding
- shotgun weddings
- shotless
- shotlike
- shot put
- shot putter
- shots
- shotted
- shotting
- shot up
- shot²
- shot¹
- 老毛病又犯了
- 老民
- 老民黑头
- 老气
- 老气横披
- 老气横秋
- 老气横秋老气横披
- 老水产
- 老水牛到水田里
- 老水牛拉马车——不合套
- 老汉
- 老江湖
- 老汤
- 老汪家
- 老沙
- 老没出息
- 老没正经
- 老油勺
- 老油子
- 老油子,老滑头
- 老油条
- 老油竹纸
- 老泉
- 老法
- 老法师