孟湘禄

[摘要] 目的 探討肠内营养粉剂AA-PKU2对苯丙酮尿症患儿智力发育及血清苯丙氨酸(Phenylalanine,PHE)水平的影响。 方法 选择2017年5月~2019年10月我院收治的苯丙酮尿症患儿106例,按随机对照原则分为两组,每组各53例。对照组给予低苯丙氨酸饮食治疗,观察组给予肠内营养粉剂AA-PKU2治疗。比较两组患儿身体指标、智力发育水平、血清PHE水平、生活质量测定量表(PedsQLTM)评分及不良反应情况。 结果 治疗8、32周后,两组患儿的身高、头围、体重均高于治疗前,差异有统计学意义(P<0.05),但组间比较差异无统计学意义(P>0.05);治疗32周后,观察组患儿血清PHE低于对照组,智力发育水平高于对照组,差异有统计学意义(P<0.05);治疗32周后,观察组患儿情感功能、生理功能、心理领域、角色功能、社会功能评分均高于对照组,差异有统计学意义(P<0.05);治疗期间,观察组不良反应发生率(11.32%)高于对照组(0.00%),差异有统计学意义(P<0.05)。 结论 对苯丙酮尿症患儿使用肠内营养粉剂AA-PKU2治疗,在不影响儿童身体发育的情况下,可显著提高患儿智力发育水平,降低血清PHE水平,提高生活质量,虽有不良反应发生,但均为轻症,患儿可耐受。
[关键词] 苯丙酮尿症;肠内营养粉剂AA-PKU2;智力发育;血清PHE;生活质量
[中图分类号] R725.8? ? ? ? ? [文献标识码] A? ? ? ? ? [文章编号] 1673-9701(2020)35-0023-04
[Abstract] Objective To explore the effect of enteral nutrition powder AA-PKU2 on the intelligence development and the serum phenylalanine(PHE) level among the children with phenylketonuria(PKU). Methods From May 2017 to October 2019, a total of 106 children with PKU admitted to and treated in our hospital were selected and divided into two groups according to random control principle, with 53 patients in each group. The control group was treated with low PHE diet, while the observation group was treated with enteral nutrition powder AA-PKU2. The body index, intelligence development level, serum PHE level, scores of the pediatric quality of life inventory measurement models(PedsQLTM) and adverse reactions(ADRs) were compared between the two groups. Results After 8 weeks and 32 weeks of treatment, the height, head circumference and body mass of the two groups of children were all higher than those before treatment, with statistically significant differences(P<0.05), but there was no statistically significant difference between the two groups(P>0.05). After 32 weeks of treatment, the serum PHE of the children in the observation group was lower than that in the control group, and the intelligence development level was higher than that in the control group, with statistically significant differences(P<0.05). After 32 weeks of treatment, the scores of emotion function, physiological function, psychological field, role function and social function of the children in the observation group were higher than those in the control group, with statistically significant differences(P<0.05). During the treatment, the incidence of ADRs in the observation group(11.32%) was higher than that in the control group(0.00%), with statistically significant difference(P<0.05). Conclusion Enteral nutrition powder AA-PKU2 for the children with PKU can significantly raise the level of intelligence development, reduce the serum PHE level and improve the quality of life without affecting their physical development. Although ADRs occur, all of them are mild and tolerable for the children.
[Key words] Phenylketonuria; Enteral nutrition powder AA-PKU2; Intelligence development; Serum PHE; Quality of life
苯丙酮尿症属于单基因隐性遗传病,是由于基因突变所致苯丙氨酸代谢异常,造成体内大量蓄积苯丙氨酸,并从尿中排出,在我国苯丙酮尿症的发病率在0.9‰左右[1-2]。若苯丙酮尿症治疗不及时,患儿在出生后3~4个月,可引发不可逆的神经系统损伤,从而影响患儿智力发育,危害患儿身心健康[3]。目前,临床治疗以饮食疗法为主,通过控制苯丙氨酸的摄入量以达到治疗目的,但往往治疗效果不理想,血清苯丙氨酸的浓度无法控制在理想范围内。鉴于此,本研究分析肠内营养粉剂AA-PKU2对苯丙酮尿症患儿智力发育及血清苯丙氨酸(Phenylalanine,PHE)水平的影响,现报道如下。
1 资料与方法
1.1 一般资料
经医院医学伦理委员会批准,将我院2017年5月~2019年10月收治的苯丙酮尿症患儿106例按随机对照原则分为两组,每组各53例。观察组中男31例,女22例;年龄1~6岁,平均(3.36±1.08)岁;出生孕龄39~42周,平均(40.93±0.89)周。对照组中男32例,女21例;年龄1~6岁,平均(3.32±1.05)岁;出生孕龄39~42周,平均(41.02±0.91)周。两组一般资料比较,差异无统计学意义(P>0.05),具有可比性。
納入标准:①符合苯丙酮尿症诊断标准者[4];②生命体征平稳,诊断时血清PHE浓度>360 μmol/L者[5];③患儿家属签署知情同意书。排除标准:①早产儿、低体重儿;②严重心肝肾功能异常者;③神经系统疾病、严重感染性疾病者;④顽固性腹泻、完全性肠梗阻者;⑤遗传代谢性疾病者;⑥恶性肿瘤或免疫功能受损者。
1.2 方法
对照组给予低苯丙氨酸饮食,将血清PHE控制在360 μmol/L。观察组给予肠内营养粉剂AA-PKU2(批准文号:国药准字J20150122,规格:80 g,EA制药株式会社)治疗,1~3岁患儿给予(176~192)g/d,4~6岁患儿给予(212~232)g/d,1次/d,具体剂量由医师决定。两组均治疗32周。
1.3 观察指标及评价标准
①治疗8、32周检测患儿身高、头围及体重。②根据格赛尔(Gesell)法评估患儿智力发育水平,包括精细运动、大运动、个人社交、语言等方面,总分100分,85分及以上为智力发育正常,70~84分为智力偏低,70分以下为智力发育异常[6-7];用高效液相色谱法测定患儿血清PHE水平。③根据儿童生活质量测定量表(The pediatric quality of life inventory measurement models,PedsQLTM)评估患儿生活质量,包括情感功能、生理功能、心理领域、角色功能及社会功能5个维度,总分100分,分数越高生活质量越好[8]。④记录患儿治疗过程中不良事件发生情况,包括呼吸道感染、腹泻等。
1.4 统计学方法
采用SPSS25.0统计学软件进行数据分析,计数资料以[n(%)]表示,采用χ2检验;计量资料用(x±s)表示,采用t检验,多组间比较采用方差分析,P<0.05为差异有统计学意义。
2 结果
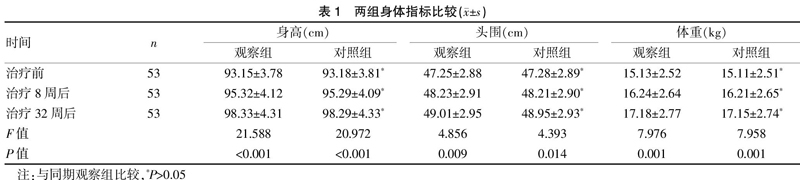
2.1 两组身体指标比较
治疗8、32周后,两组患儿的身高、头围、体重均高于治疗前,差异有统计学意义(P<0.05),治疗后各时间点,观察组与对照组比较,差异无统计学意义(P>0.05)。见表1。
2.2 两组智力发育及血清PHE水平比较
治疗前两组患儿的智力发育及血清PHE水平比较,差异无统计学意义(P>0.05);治疗32周后,观察组患儿的血清PHE低于对照组,智力发育水平高于对照组,差异有统计学意义(P<0.05)。见表2。
2.3 两组生活质量比较
治疗前,两组患儿PedsQLTM各项评分比较,差异无统计学意义(P>0.05);治疗32周后,观察组患儿的情感功能、生理功能、心理领域、角色功能、社会功能评分均高于对照组,差异有统计学意义(P<0.05)。见表3。
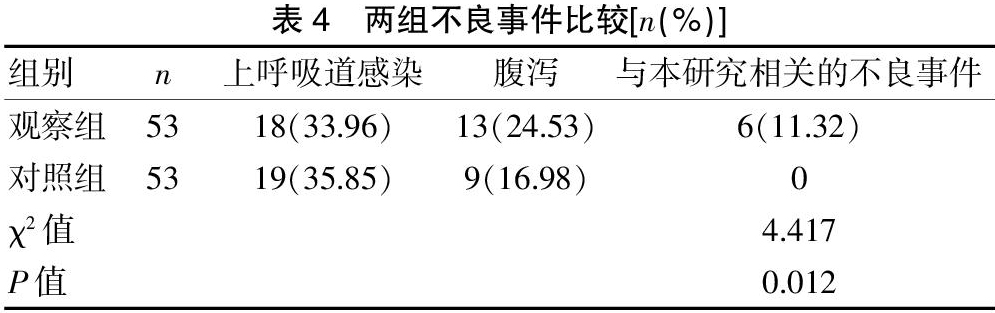
2.4 两组不良事件比较
治疗32周内,观察组患儿31例发生不良事件,考虑与本研究药物相关的事件为轻度腹泻6例;对照组患儿28例发生不良事件,均与本研究不相关,发生的不良事件无需处理或对症处理后均治愈。两组与本研究相关的不良事件比较,差异有统计学意义(P<0.05)。见表4。
3 讨论
苯丙酮尿症是由于患儿体内缺失苯丙氨酸羟化酶或其活性降低,使苯丙氨酸无法向酪氨酸转化所致,而次要代谢途径增强,导致苯乙酸、苯乳酸、苯丙酮尿酸等从尿中排出。本病的主要临床表现为精神异常、色素缺失、易有湿疹及智力发育迟缓等,由于早期无特异性症状,外表与健康儿童无异,以致误诊、漏诊较高[9]。苯丙酮尿症患儿体内苯丙氨酸可与中性大分子氨基酸1型转运体结合,抑制其与大分子中性氨基酸(Macromolecular neutral amino acid,LNAAs)结合,从而使血液中LNAAs含量降低,且抑制色氨酸羟化酶活性,从而降低血清素与多巴胺水平,影响患儿的生活质量[10-11]。目前,临床治疗方案为低苯丙氨酸饮食疗法,即控制患儿苯丙氨酸的摄入,而苯丙氨酸存在于蛋白质中,因此患儿饮食需对蛋白质有特殊要求,如无苯丙氨酸奶粉、蛋白粉等。但该疗法并不能彻底根治本病,虽然方法简单,但由于治疗时间长,饮食需严格控制,对患儿及家属是一个巨大考验[12]。有研究报道,苯丙酮尿症患儿通过饮食疗法并不能将血清苯丙氨酸浓度控制在理想范围,10岁以内的患儿中超过规定范围者超过30%,因此,通过饮食控制摄入量相对困难[13]。
本研究结果显示,治疗后两组患儿的身高、头围、体重均高于治疗前,观察组与对照组比较无明显差异,观察组患儿的血清PHE低于对照组,智力发育水平、情感功能、生理功能、心理领域、角色功能、社会功能评分高于对照组,治疗期间观察组的不良反应发生率高于对照组。说明肠内营养粉剂AA-PKU2治疗苯丙酮尿症,可在满足患儿生长发育的前提下,有效限制苯丙氨酸的摄入,使其浓度得到有效控制,且有效促进患儿的智力发育、提高生活质量,虽然有不良反应发生,但均为轻度腹泻,给予对症治疗后可治愈。肠内营养粉剂AA-PKU2是一种不含苯丙氨酸的药品,含有100%游离氨基酸,具有易吸收、无残渣性的优点,其中51%为碳水化合物,25%为蛋白质,并含有维生素、微量元素、其他氨基酸及矿物质,能够为患儿补充碳水化合物、氨基酸等所需营养物质,通过粪便排出少、所需消化液极少,其能量主要来源于食物淀粉、糊精,脂肪来源于大豆油,同时严格限制苯丙氨酸的摄入,为患儿提供更多生物效价较高的蛋白质,从而阻止了患儿神经功能受损,维持其正常智力发育,并且对患儿肠道黏膜功能起到维持作用,降低肠黏膜萎缩的发生[14]。少数患儿可出现轻度腹泻症状,考虑肠内营养粉剂AA-PKU2虽然不需要消化,但其渗透压相对较高,可引发腹泻等消化道反应,但症状并不严重,且可治愈,安全性良好[15]。
综上所述,肠内营养粉剂AA-PKU2治疗苯丙酮尿症,可满足患儿生长发育需求,有效限制苯丙氨酸的摄入,促进患儿智力发育,提高生活质量,虽然有不良反应发生,但均为轻度腹泻,给予对症治疗后可治愈,安全性良好。
[参考文献]
[1] 陆清,刘艳秋,杨必成,等. 苯丙酮尿症患者苯丙氨酸羟化酶基因的变异研究[J]. 中华医学遗传学杂志,2019, 36(11):1057-1061.
[2] Spronsen FJ,Wegberg AJ,Ahring K,et al. Key European guidelines for the diagnosis and management of patients with phenylketonuria[J]. Lancet Diabet Endocrinol,2017, 5(6):743-756.
[3] 吕书博,张展,赵德华,等. 苯丙酮尿症大鼠海马神经元损伤及其与BDNF/TrkB通路的关系[J]. 东南大学学报(医学版),2019,38(3):461-466.
[4] 中华医学会儿科学分会内分泌遗传代谢学组,中华预防医学会中华预防医学会出生缺陷预防与控制专业. 高苯丙氨酸血症诊治共识[J]. 中华儿科杂志,2014,52(6):420-425.
[5] 中华医学会医学遗传学分会遗传病临床实践指南撰写组. 苯丙酮尿症的临床实践指南[J].中华医学遗传学杂志,2020,37(3):226-234.
[6] 应艳红,鲜丹,袁飒. S-S检测法与Gesell量表在儿童语言发育评估中的一致性[J]. 中国听力语言康复科学杂志,2019,17(4):291-293.
[7] 梁静,王朝晖. S-S语言发育迟缓评价法与Gesell发育评估量表在幼儿语言评定应用中的對比[J]. 中国儿童保健杂志,2017,25(5):514-516.
[8] 黄卓燕,郝元涛,朱琦,等. 儿童生存质量测定量表PedsQL 3.0心脏病模块中文版的信度和效度分析[J]. 中国组织工程研究,2010,14(48):9037-9040.
[9] 朱玲,杨建平,董勤,等. 山西省新生儿疾病筛查中心十年苯丙酮尿症患儿治疗效果评估[J]. 中华全科医师杂志,2018,17(3):197-201.
[10] 韩宗兰,王兰英,王海楠,等. 影响苯丙酮尿症患儿生活质量的相关因素及干预措施[J].中国医药导报,2019, 16(6):90-93.
[11] 邱婷,许吟,王丽珍,等. 早期饮食治疗的苯丙酮尿症儿童生活质量现状分析[J]. 中国儿童保健杂志,2018, 26(7):796-799.
[12] 庞永红,褚英,刘雪楠,等. 淮海地区汉族苯丙酮尿症患儿苯丙氨酸羟化酶基因突变分析[J]. 中华实用儿科临床杂志,2018,33(20):1545.
[13] Walter JH,White FJ,Hall SK,et al. How practical are recommend ations for dietary control in phenylketonuria?[J].Lacent,2002,360(9326):55-57.
[14] 周雪莲,赵正言,江剑辉,等. 肠内营养粉剂AA-PKU2治疗1~8岁苯丙酮尿症患儿的有效性和安全性研究[J].中国当代儿科杂志,2014,16(1):11-15.
[15] 周雪莲,赵正言,沈明,等. 肠内营养粉剂(AA-PKU1)对0~1岁苯丙酮尿症患儿治疗的有效性和安全性[J]. 中华实用儿科临床杂志,2014,29(20):1537-1542.
(收稿日期:2020-07-06)
- 钢琴调律及基准音组调律技术分析
- 传承广西北部湾海歌意义深远
- 绕而不扰
- 论戏曲音乐对民族声乐的影响
- 肖邦钢琴作品抒情性旋律的演奏技能分析
- 论体育舞蹈音乐的作用及美感的要素
- 舞蹈表演动作思维与创造力培养
- 诗歌中乐舞资料的搜集与分析
- 《大梦敦煌》对中国民族舞剧创作的新思考
- 用数学的方式思考动漫
- 美术造型艺术创作的形式美
- 从图像学浅析莫奈《睡莲》系列作品
- 我国艺术市场存在的问题探究
- 关于双林寺彩塑人物眼睛的研究
- 黄铁山水彩画的图像学解读
- 浅谈对康定斯基《论艺术的精神》的认知
- 地方民间艺术的品牌建设问题研究
- 图形创意在现代生活的应用
- 论刺绣在戏剧艺术中的创新及应用
- 黔东南苗族装饰符号与文化语言表述的艺术特征研究
- 在互联网时代下校园文创产品的销售发展与设计研究
- 舞台灯光的综合艺术性分析
- 从历史维度思考俄罗斯的改革
- 冷热媒介的选择对信息传播的影响
- 关于对永顺县双凤村土家族非物质文化遗产艺术的现状调查
- doctorships
- doctor's office
- doctor²
- doctor¹
- doctrine
- doctrines
- doctrinist
- document
- documentable
- documentably
- documental
- documentaries
- documentarily
- documentary
- documentary collection
- documentarycollection
- documentary credit
- documentarycredit
- documentation
- documentational
- documentation's
- documentations
- documented
- documenter
- documenters
- 马哥
- 马善被人骑,人善被人欺
- 马嘉理案
- 马嘎尔尼
- 马嘎尔尼使华
- 马嘶
- 马嘶人语
- 马嚼
- 马嚼子
- 马嚼子、马笼头
- 马嚼子两端露出嘴外的部分
- 马嚼子和马缰绳
- 马嚼子套在牛嘴上——胡勒
- 马嚼子或缰绳上的装饰品
- 马困人乏
- 马图
- 马圈
- 马圉
- 马在柔软的草地上易打前失,人在甜言中易栽跟斗
- 马在软地上打前失,人在好话里栽跟头
- 马场
- 马坊
- 马坎
- 马坑
- 马坦克车