
摘要:为了弥补教材实验的不足,利用三颈瓶、干燥管、一次性注射器等仪器或用品,设计了浓硝酸与碳反应的实验装置及实验方法,反应产牛的气体可以被验证且全部被吸收,既避免了气体产物对教学环境的污染,又能提高实验教学效果。
关键词:浓硝酸与碳反应;实验设计;化学实验探究
文章编号:1005 - 6629(2015)5 - 0072 - 03
中图分类号:G633.8
文献标识码:B
现行高中化学教材[1]“硝酸”一节在介绍硝酸的氧化性时,针对浓、稀硝酸与金属铜反应设计了课堂演示实验,效果很好,通过实验增强了学生的感性认识,以及对该知识点的理解和记忆,深受学生的欢迎。但在介绍硝酸与非金属反应,特别是浓硝酸与碳的反应时,教材中只给出了相应的化学反应方程式[2],没有相应的实验方法加以验证,因而缺乏说服力,不利于培养学生的观察能力和激发学生的学习兴趣,无助于学生对该知识点的掌握。因此,笔者认为在教学中应该增加浓硝酸与碳反应课堂演示实验。然而,做好该实验的关键不外乎有以下三点:其一,必须是炽热的碳与热的浓硝酸反应;其二,验证反应有二氧化碳气体生成(二氧化氮的特征颜色是红棕色气体,通过观察便知);其三,设法消除浓硝酸加热挥发出的酸蒸气和反应所产生的二氧化氮有毒气体对教学环境的污染。近些年来,尽管一些教师对浓硝酸与碳的反应实验进行了重新设计与改进,但有的比较麻烦,需要将浓硝酸内的水分吸收掉[3];有的没有考虑到加热浓硝酸时挥发出的硝酸蒸气和瞬间产生二氧化氮有毒气体对教学环境的污染[4];还有的仪器复杂难于制作和组装[5]。为此,我们对该反应实验进行了研究和设计,解决了实验现象不佳和环境污染等诸多问题,从而提高了教学效果。现将实验方法介绍如下。
1 实验仪器和用品
三颈瓶(250mL)1只;一次性注射器(20mL)2只;注射器针头(兽医用)1根;单球干燥管1支;1、2号橡胶塞各1个;2、3号单孔橡胶塞各1个;钢针1根;玻璃棒(15cm,略细,可插入玻璃管)1根;玻璃管(1Ocm,略粗)l根;酒精灯、酒精喷灯各1盏;铁架台、铁夹各1个;橡胶管(5cm)1段;小烧杯(50mL)2只;钢丝钳1把;火柴1盒
浓硝酸(69%);木炭(烤羊肉串专用木炭);碱石灰(颗粒状);新制备的澄清石灰水;蒸馏水;10%氢氧化钠溶液;凡士林
2 仪器的加工与组装
2.1 玻璃棒的加工
取1根钢针,用钳子剪断;用酒精喷灯将玻璃棒的一端加热,使其变软,然后将带尖的一段钢针(长2cm)尖端朝外镶嵌在玻璃棒内(如图1所示)。
2.2 橡胶塞的组装
取3号单孔橡胶塞,在孔内装入lOcm长的玻璃管后,在橡胶塞大头端的玻璃管上装上5cm长的一段乳胶管;在嵌有钢针的玻璃棒上涂上凡士林,然后从橡胶塞小头端的玻璃管内穿人(如图2所示)。
2.3 组装干燥管
取1个干燥管,在其细管上安装一个2号单孔橡胶塞,在干燥管内加入用蒸馏水润湿的碱石灰颗粒(如图3所示)。
3 实验装置
4 实验方法及其现象
将装置固定在铁架台上。
4.1 注入浓硝酸
取下带有玻璃棒的橡胶塞,向三颈瓶内加入1.5~2mL的浓硝酸。
4.2 加热木炭
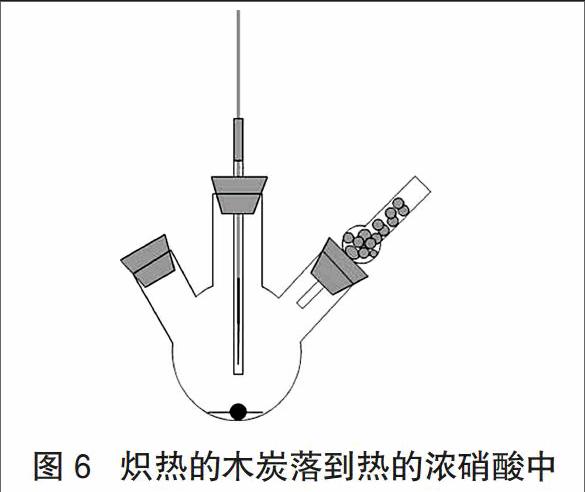
取1块木炭(要求直径比玻璃管内径大),扎在玻璃棒的钢针上后,用酒精灯的外焰加热木炭(如图5所示),当木炭被点燃后,迅速将带有玻璃棒的橡胶塞紧紧塞在三颈瓶的中间瓶口上(如图4所示)。此时,要求木炭距浓硝酸液面2cm左右。
4.3 加热浓硝酸
用酒精灯的外焰加热三颈瓶内的浓硝酸2~3s,当观察到三颈瓶内有白色的硝酸蒸气时,撤离酒精灯。
4.4 上提玻璃棒
迅速上提玻璃棒,使炽热的木炭掉人热的浓硝酸中(此时,钢针缩进到玻璃管内,如图6所示),可观察到木炭在浓硝酸中剧烈燃烧「C+4HN03(浓)=C02↑+4N02↑+2H20」,生成红棕色气体,说明有二氧化氮气体生成。
4.5 二氧化碳的检验
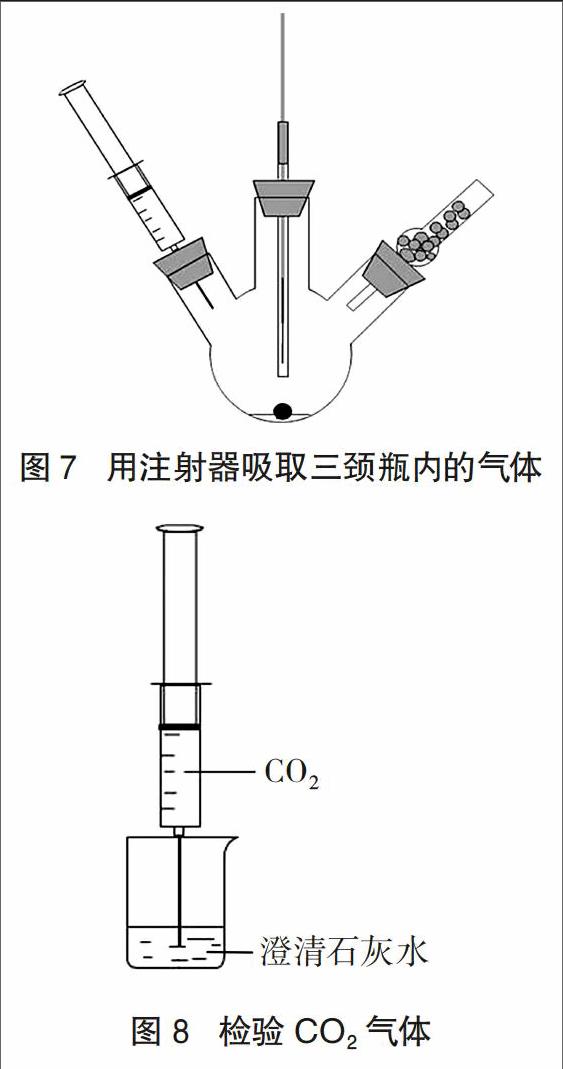
取1支一次性注射器(20mL),吸人2mL的蒸馏水,然后将注射器的针头插入到左侧橡胶塞内(如图7所示)。拉动注射器的活塞吸取三颈瓶内的气体18mL,取下注射器,在注射器的针头上扎上一个l号橡胶塞后,振荡注射器,使注射器管内的二氧化氮气体全部被水吸收掉( 3N02+H2O=2HN03+NO)。取下针头上的橡胶塞,将注射器管内的液体全部排入到一只空的小烧杯内。接着再将注射器管内的气体全部排入到盛有20mL澄清石灰水的小烧杯中(如图8所示),可观察到澄清的石灰水变浑「C02+Ca(OH)2=CaC03↓+H20」,由此说明碳与浓硝酸反应除生成二氧化氮气体以外,还生成了二氧化碳气体。
5 有害物质的处理
待三颈瓶冷却后,用一次性注射器吸取20mL的氢氧化钠溶液,通过左侧橡胶塞注入到三颈瓶内,反复振荡,使瓶内的有害气体和剩余的浓硝酸全部被吸收掉。
6 几点说明
6.1 反应器使用三颈瓶的原因 使用容积较大的三颈瓶作为反应器,可以保证容器内有充足的空气,使炭块在反应前始终处于燃烧或炽热状态;利用三颈瓶的一个瓶颈加入反应物(炽热的炭),一个瓶颈消除污染,调节压强,一个瓶颈吸取反应后的气体用作检验;实验现象可见度大,便于学生观察。
6.2 实验成功关键
通过反复实验发现,浓硝酸与炭容易发生反应的关键是热的浓硝酸(出现硝酸蒸气)和炽热或燃烧的炭,倘若二者中有一个温度不够,则会造成实验失败。所以,为了保障炭块在反应前始终处于燃烧或炽热状态,浓硝酸用量不能太大,一般1.5~2mL最为合适,在3~5s内,浓硝酸完全可以达到实验所需的温度。
6.3 钢针不会干扰实验
由于玻璃棒上镶嵌的钢针很短,在实验过程中,先是被炭块包裹,随后是缩进到玻璃管内,不会被腐蚀,也不会对整个实验造成干扰。
6.4 蒸馏水的作用
由于二氧化氮和二氧化碳在水中的溶解度不同,所以用蒸馏水吸收掉了二氧化氮气体(其与水反应生成的无色一氧化氮气体对二氧化碳的检验无干扰),而保留了大部分的二氧化碳气体(二氧化氮在水中的溶解度远大于二氧化碳在水中的溶解度)。
参考文献:
[1][2]课程教材研究所化学课程教材研究开发中心.全日制普通高级中学教科书·化学(必修加选修)(第二册)[M].北京:人民教育出版社,2003:16,17
[3]杨玉麟.碳与浓硝酸反应的补充实验[J].化学教育,2001,22(11):8
[4]贾绍明.碳与浓硝酸反应的实验创新设计[J].新课程研究(基础教育),2008,(5):38
[5]齐俊林.碳在浓硝酸里燃烧实验的新办法[J].实验教学与仪器,1994,(6):35
- 巧借分类思想,优化小学数学教学
- 浅议数学“问题”的设置
- 解析小学数学应用题建模教学
- 让学生走出“困”境
- 优化口算教学,提升计算能力
- 分层教学在小学数学课堂教学中的应用研究
- 试论小学高年级数学高效课堂的创建途径
- 小学数学教学中动手操作对培养学生思维作用
- 让“互动反馈系统”成为数学课堂的益友
- 优化知识结构 注重能力发展
- 运用数字故事开展小学数学课堂教学
- 试论如何培养小学数学教学中学生良好学习习惯
- 关于小学数学乘法教学新思路探究
- 立足校本课程,提升学生数学讲题能力
- 万丈高楼平地起
- 特色综合实践活动课程开发的几点思考
- 用“心”管理班级
- 普通高中班级工作存在的问题及对策
- 关于高中音乐教学艺术的深入思考
- 简述我国高校辅导员的历史变迁与角色定位
- 做个智慧型班主任
- 搭建“成功”的阶梯,享受“质疑”的快乐
- 在核心素养视野下高中体育健康专项教学内容的选择
- 探讨初中教学管理的优化策略
- 张扬个性,促进发展
- fends
- fend sb/sth off
- fend sb/sth ↔ off
- fendy
- feng shui
- fennel
- fennels
- fennel-seed
- feral
- ferally
- ferals
- ferment
- fermentabilities
- fermentability
- fermentation
- fermented
- fermenting
- ferments
- ferment²
- ferment¹
- fern
- fernier
- ferniest
- fernless
- fernlike
- 舆论调查问卷类型
- 舆论调查问卷设计
- 舆论调查问卷问题的编制
- 舆讼
- 舆评
- 舆词
- 舆诵
- 舆谈
- 舆谣
- 舆车
- 舆车手车
- 舆轮
- 舆轿
- 舆辂
- 舆辆
- 舆辇
- 舆金辇宝
- 舆金辇璧
- 舆隶
- 舆颂
- 舆颂载途
- 舆马
- 舆骑
- 與
- 與其