梅溪
【摘 要】对Na2S2O3和H2SO4进行不同的探究,通过浓度、温度对化学速率不同的影响,对中学化学中浓度和温度对化学反应速率的影响提供一定的参考资料。从而很好地掌握了影响化学反应速率的因素。
【关键词】温度;浓度;反应速率
一、问题的提出
人教版《化学》选修4《化学反应原理》中,影响化学反应速率的因素是一个非常重要的实验。教材中设计到的温度和浓度对化学反应速率的影响有两个实验,浓度对化学反应速率的影响是用0.01mol/L酸性KMnO4溶液分别与0.1mol/L的H2C2O4溶液和0.2mol/L的H2C2O4溶液反应来进行验证,结果表明加入较浓的H2C2O4溶液褪色更快。温度对化学反应速率的影响是用0.1mol/LNa2S2O3溶液和0.1mol/L的H2SO4溶液进行反应,一组放入热水中,另一组放入冷水中,记录出现浑浊的时间,结果显示,放入热水的这一组出现浑浊的时间要比放入冷水的时间短,实验表明,其他条件相同时,升高温度反应速率增大。但是在实际实验教学过程中按照教材上的方法进行实验显得有些繁琐,为了更加简便、直观的观察实验现象,对此实验进行了改进,只用0.1mol/LNa2S2O3溶液和0.1mol/L的H2SO4溶液进行反应,同时验证了浓度和温度对化学反应速率的影响,并得到了理想的实验效果。
二、研究目的和意义
(一)研究目的
为探究浓度、温度对化学反应速率的影响,对教材实验改进,用一个实验来证明温度、浓度对化学反应速率的影响,掌握实验的操作方法,并得到理想的实验结果。
(二)研究意义
“为探究浓度、温度对化学反应速率影响”的学生实验方面提供一些可借鉴的资料。
三、研究方法(实验法)
(一)试剂与仪器
0.1mol/LNa2S2O3溶液、0.1mol/LH2SO4溶液、蒸馏水、试管、烧杯、温度计、秒表、电子天平、容量瓶、玻璃棒、胶头滴管、洗瓶。
(二)实验方法
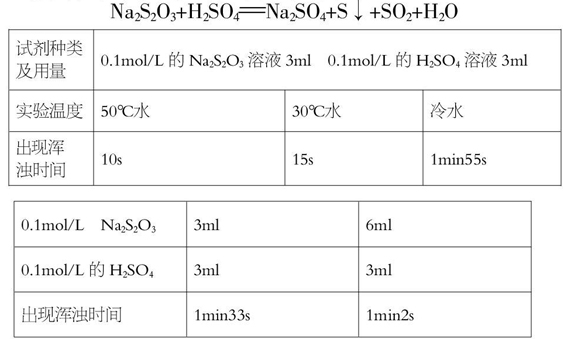
1.准确配置好0.1mol/L的Na2S2O3溶液和0.1mol/L的H2SO4溶液,在三个烧杯中装入不同温度的水,然后取三支大试管分别加入相同体积的反应物,将这三支试管放入不同温度水的烧杯中,观察实验现象,记录出现浑浊的时间。
2.室温下,取两支大试管,分别加入不同体积的反应物,观察实验现象,记录出现浑浊的时间。
Na2S2O3+H2SO4■Na2SO4+S↓+SO2+H2O
(三)实验结果与讨论
从第一组实验数据可以看出,用0.1mol/L的Na2S2O3溶液和0.1mol/L的H2SO4溶液各3ml进行反应,当温度越高时,出现浑浊的时间越短,从而得到结论:温度越高化学反应速率越快。从第二组实验数据可以看出,当用0.1mol/L的Na2S2O3溶液和0.1mol/L的H2SO4溶液各3ml进行反应,出现浑浊的时间为1分33秒,而当把0.1mol/L的Na2S2O3溶液改为6ml时,出现浑浊的时间要比原来的更短,从而得到结论:反应物的浓度越大化学反应速率越快。
(四)结论
通过实验证明得到结论:其他条件相同时,升高温度反应速率增大,降低温度反应速率减小。增大反应物浓度反应速率增大,减小反应物浓度反应速率减小。
四、应用
通过设计一个实验,对中学化学中浓度和温度对化学反应速率的影响提供一定的参考资料。从而很好地掌握了影响化学反应速率的因素。在日常生活中所用到的一些例子,如水结成冰,水变成汽,汽车加大油门,向炉膛鼓风,用煤粉代替煤块,把食物放在冰箱里等等,就是为了改变反应速率而采取的措施。
(作者单位:江苏省南京市第三高级中学)
- 30%超分子水杨酸与低浓度甘醇酸在轻中度寻常性痤疮治疗中的疗效评价
- 超分子水杨酸治疗痤疮的效果及对皮肤屏障的影响
- 寻常性痤疮诊断和治疗的新动向
- 丹银海绵对糖尿病大鼠皮肤溃疡创面愈合的影响
- 应用三维CT扫描重建技术对假体隆鼻术后位移精确测量的方法探讨
- 中药面膜辅助治疗黄褐斑临床疗效Meta分析及用药规律探讨
- Er:YAG激光在口腔种植二期手术中的应用及围手术期护理观察
- 牙科放大镜在前牙美学修复中的临床应用
- 口腔错牙合畸形与青少年特发性脊柱侧弯相互关系的临床研究
- 直丝弓矫治器和Begg矫治器治疗安氏Ⅱ类1分类错牙合畸形疗效比较
- 不同方法治疗近中阻生大学生第二或三磨牙远中龋齿的疗效分析
- 三种不同填充材料修复牙齿楔状缺损的疗效比较
- 不同铸造方法在三单位桥固定式义齿桥中的应用效果分析
- 三点式钛板坚固内固定治疗颧骨颧弓过高的临床研究
- 不同手术方式对颧骨复合体骨折的疗效比较
- 腭皱法与传统法比较正畸治疗前后上颌牙弓宽度变化的临床研究
- 构建基于网络信息化教学的整形美容外科住院医师规范化培训体系的探索与思考
- 研究生助教参与正畸学实验教学模式探讨
- 透明质酸在烧伤整形美容外科中的应用进展
- 黄褐斑的治疗新进展
- 皮肤擦伤后急诊治疗方式的研究进展
- 智慧医疗相关新兴技术在整形美容外科中的应用
- 蒙古族成年男性颅颌面三维结构测量研究现状
- 眶脂肪弓状缘释放联合眶肌筋膜韧带悬吊下睑袋整形术在面部年轻化中的应用
- 下睑眶隔脂肪疝的MSCT测量及相关因素分析
- experimentors
- experiments
- experiment with
- experiment ²
- experiment¹
- expert
- expert-at
- experted
- experting
- expertise
- expertised
- expertises'
- expertises
- expertising
- expertly
- expertness
- expertnesses
- experts
- expertsystem
- expert system
- expert-systems'
- expert systems
- expiration
- expirationdate
- expiration date
- 长臂猿
- 长至
- 长舅
- 长舌
- 长舌为斧
- 长舌之妇
- 长舌乱家,大斧破车
- 长舌头
- 长舌妇
- 长艾
- 长芦苇的池
- 长苔的石碑
- 长苞
- 长莽
- 长薄
- 长虑却顾
- 长虑后顾
- 长虑顾后
- 长虫
- 长虫吃了烟袋油——浑身哆嗦
- 长虫吃扁担——直杠一条
- 长虫吃蛤蟆——慢慢来
- 长虫吃鸡蛋——一点一点倒
- 长虫吞扁担——没法咽下去
- 长虫吞针