摘要:采用去卵巢骨质疏松大鼠模型,观察跑台运动、全身垂直振动、金雀异黄酮、雌激素和氯化锂5种干预疗法对去卵巢骨质疏松大鼠骨髓脂肪细胞数目和过氧化物酶体增殖激活物受体γ2(PPARγ2)蛋白表达水平的影响。方法:将80只3月龄雌性SD大鼠按体重分层后随机分为假手术组和去卵巢组,去卵巢10周后,将去卵巢组大鼠按体重分层后又随机分为去卵巢组、雌激素组、金雀异黄酮组、氯化锂组、跑台运动组和全身垂直振动组。去卵巢第11周时,不同组别的大鼠开始进行不同干预处理。干预8周后,用HE染色法观察左胫骨组织形态学和骨髓脂肪细胞空泡数目的变化;用Western blotting检测右胫骨近端骨组织PPARγ2蛋白表达水平的变化。结果:经雌激素、金雀异黄酮、跑台运动和氯化锂干预后,去卵巢骨质疏松大鼠胫骨松质骨骨小梁数目显著增加,脂肪空泡数目和PPARγ2蛋白表达水平显著下降,而经全身垂直振动干预后,去卵巢骨质疏松大鼠胫骨松质骨骨小梁数目显著增加,脂肪空泡数量显著减少,但PPARγ2蛋白表达水平无显著变化。结论:雌激素、金雀异黄酮、跑台运动和氯化锂可能是通过下调去卵巢骨质疏松大鼠骨组织PPARγ2蛋白的表达水平而抑制去卵巢骨质疏松大鼠骨髓细胞向脂肪细胞的分化。
关键词: 去卵巢大鼠;跑台运动;全身垂直振动;金雀异黄酮;PPARγ2
中图分类号: G 804.2 文章编号:1009783X(2016)03027004 文献标志码: A
Abstract:The aim of this study was to investigate the effects of five different intervention methods on the bone histology and the protein expression of peroxisomeproliferatoractivated receptorgamma2 (PPARγ2) in the ovariectomized osteoporosis rats.Methods:Eighty healthy female SD rats,aged 3 months,were randomly divided into the following two groups by body weight:shamoperation (Sham) and ovariectomized (OVX).After ten weeks,the OVX group rats were randomly divided into the following six groups by body weight:OVX;17βestradiol (E2);Genisteine (G);treadmill exercise (TE);Lithium chloride (LiCL);Wholebody vertical vibration (WBVV).Then the rats began to be treated with different intervention methods.At the end of 8 weeks intervention,during 3648 hours,the tibia was isolated.The morphological changes of the left tibia were observed by HE staining and the protein expression of PPARγ2 in right tibia were detected by western blot.Results:After treated with E2,treadmill exercise,wholebody vertical vibration,genistein and LiCL,the number of trabecular bone were significantly increased and the number of bone marrow adipocytes were significantly decreased than that of in OVX group.After treated with E2,treadmill exercise,genistein and LiCL,the protein expression of PPARγ2 were significantly lower than that of in OVX group.However,wholebody vertical vibration treatment had no significant difference.Conclusions:Treadmill exercise,E2,genistein and LiCL could inhibit the differentiation of bone marrow stromal cells to fat cells by inhibiting the protein expression of PPARγ2 in bones of OVX osteoporosis rats.
Keywords:ovariectomized osteoporosis rats;treadmill exercise;genistein;lithium chloride;PPARγ2
在人的一生中,骨骼都在持续经历着骨形成和骨吸收的重塑过程。在生长发育期和年轻时,骨平衡是正平衡,即骨形成大于骨吸收;但40岁以后,骨吸收则大于骨形成,骨量开始下降,随着年龄进一步增加会出现骨质疏松症状[1]。绝经后妇女体内雌激素的缺乏是引起骨量急剧下降、发生骨质疏松的主要原因[2]。虽然目前治疗绝经后骨质疏松的方法有激素替代疗法、双磷酸盐、植物雌激素等药物疗法,以及运动、电脉冲刺激等非药物疗法[37],但绝经后骨质疏松的防治仍具有挑战性。尽管人体和动物实验均已证明了跑台运动、金雀异黄酮、全身垂直振动、雌激素和氯化锂等不同疗法的骨质疏松治疗效应,但对其作用机制还不是很清楚。
随着年龄的增加,成骨发生的下降会伴随骨髓脂肪发生的增加,因为成骨细胞和脂肪细胞来源于共同的骨髓基质干细胞[8]。已有研究表明, 绝经后骨质疏松的发生与骨髓基质细胞向脂肪细胞方向分化的增加有关[9],因此,调节骨髓基质细胞向成骨细胞和脂肪细胞分化的平衡可能是骨质疏松防治的新策略。动物研究[10]表明,过氧化物酶体增殖激活物受体γ2(PPARγ2)能使骨髓细胞脂肪分化增加,导致骨丢失。鉴此,本文采用去卵巢骨质疏松大鼠模型,观察雌激素、全身垂直振动、跑台运动、金雀异黄酮和氯化锂5种干预疗法对去卵巢骨质疏松大鼠骨组织骨髓脂肪细胞数目和PPARγ2蛋白表达水平的影响。
1 材料与方法
1.1 材料
SD大鼠购自北京大学实验动物部(动物合格证号SCXK(京)20110012)。17βestradiol (E2)和金雀异黄酮购自Sigma公司。PPARγ2和βactin抗体购自SC公司。BCIP/NBT显色浓缩液和马抗小鼠IgG/碱磷酶标记抗体购自北京中杉金桥生物技术有限公司。SDSPAGE蛋白上样缓冲液和RIPA蛋白裂解液(强型)购自海门碧云天生物技术有限公司。Leica软组织切片机购自德国。研究级正置荧光显微镜购自日本尼康。DSPT202型大鼠跑台由杭州段氏制造厂生产。DYY7C型电泳仪购自北京六一仪器厂。垂直振动台由北京雅士林厂生产。
1.2 研究方法
1.2.1 实验分组
大鼠每天自由进食标准啮齿类饲料,自由饮用自来水,每笼5只分笼饲养。适应性喂养1周后,称量各只大鼠的体重,然后按体重分层后随机分为去卵巢手术组(68只)和假手术组(12只)。2组大鼠手术前均禁食12~18 h,腹腔注射10%水合氯醛(3 mL/kg)麻醉,从背部切除手术组大鼠双侧卵巢,而假手术组大鼠的卵巢不切除,只切除卵巢脂肪垫中与卵巢相当大的一块脂肪。无菌手术在北京大学医学部实验动物科学部进行[SYXK(京)20110039]。术后静养10周,第11周时称量去卵巢组大鼠体重并按体重分层后将其随机分为去卵巢组(11只)、金雀异黄酮组(10只)、雌激素组(9只)、跑台组(9只)、振动组(9只)、氯化锂组(9只)。实验过程中有11只大鼠先后死亡。
1.2.2 不同干预疗法处理方案
手术后第11周,不同组别的去卵巢大鼠分别进行不同的干预处理,具体干预方案同前期报道[11], 即雌激素组采用颈部皮下注射17β雌二醇,剂量为25 μg/kg体重,每周3次;金雀异黄酮组采用灌胃,剂量为1 mg/kg体重,每周7次;氯化锂组采用腹腔注射氯化锂,剂量为15 mg/kg体重,每周3次。跑台组每次进行速度18 m/min、坡度5°、时间40 min的跑台训练,每周4次;振动组每天进行2次时间15 min、频率90 Hz、振幅0.5 mm的振动训练,每周7次。
1.2.3 HE
将固定好的胫骨近端投入15%EDTA溶液中脱钙,脱钙后用常规石蜡包埋方法进行处理,用Leica软组织切片机将骨标本切成5 μm切片。切片经二甲苯脱蜡、梯度乙醇脱水、常规苏木素伊红染色、中性树脂封片后,在显微镜下观察拍照计数脂肪空泡数目。
1.2.4 Western blot
Western blot方法参照前期报道[11]。将称量的200 mg骨组织放入研磨器中,加入液氮迅速研磨成粉末后移入1.5 mL离心管,加入1 mL组织裂解液,放入低温离心机中作用1 h后,12 000 r/min、4 ℃离心30 min,取上清,留一部分检测蛋白质浓度,其余蛋白样品与SDSPAGE蛋白上样缓冲液(5X)按照4∶1的比例混匀,沸水变性5 min,分装后冻入-80 ℃冰箱。取10~15 μL蛋白样品上样,80 V电压电泳约2 h后,再以80 V电压转移2 h。取出PVDF膜,放入5%脱脂奶粉溶液中室温封闭1 h,加入一抗4 ℃过夜,次日用TBST缓冲液洗4次,每次10 min,分别加马抗小鼠Ig/G碱磷酶标记二抗,室温孵育2 h,用TBST缓冲液洗4次,每次10 min,然后将PVDF膜放入BCIP/NBT显色液中避光显色至条带出现,将膜捞出放入水中以终止显色,用数码相机拍照,用Quantity One软件扫描计算各条带的灰度值。
1.3 统计学分析
采用SPSS 19.0软件对实验数据进行统计学分析,实验结果以均值±标准差表示,用单因素方差进行分析。若方差齐时,用LSD posthoc检验;若方差不齐时,用Tamhane posthoc检验。P<0.05为显著性差异,P<0.01为极显著性差异。
2 结果
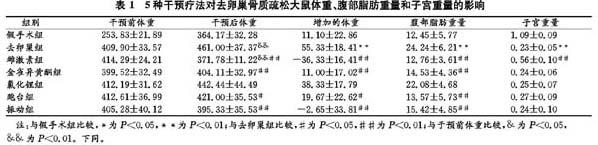
2.1 5种干预疗法对去卵巢骨质疏松大鼠体重、腹部脂肪重量和子宫重量的影响
干预8周后,与假手术组大鼠比较,去卵巢组大鼠体重和腹腔脂肪重量显著增加,而子宫重量显著降低,见表1。与去卵巢组大鼠比较,雌激素组、金雀异黄酮组、跑台组和振动组大鼠体重和腹腔脂肪重量均显著下降,而氯化锂组大鼠未见显著性差异。与去卵巢组大鼠比较,只有雌激素组大鼠子宫重量显著增加,其余各组未见显著性差异。与干预前体重比较,去卵巢组显著增加,雌激素组显著下降,而其余4组未见显著性差异。与去卵巢组比较,雌激素组、金雀异黄酮组、跑台组和振动组干预前后体重的变化量均显著降低,而氯化锂组未见显著性差异。
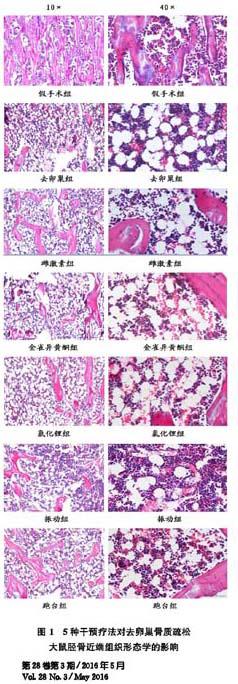
2.2 5种干预疗法对去卵巢骨质疏松大鼠胫骨近端骨组织形态学和脂肪空泡数目的影响
如图1和图2所示,假手术组大鼠胫骨近端骨小梁致密,排列整齐,大鼠去卵巢后骨小梁明显变得稀疏,出现断裂、消失,骨髓腔内脂肪空泡数目显著增加,经雌激素、金雀异黄酮、氯化锂、跑台运动和全身垂直振动干预8周后,骨小梁增加,骨髓腔内脂肪空泡数目显著减少。
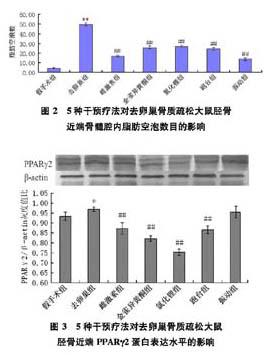
2.3 不同干预疗法对去卵巢骨质疏松大鼠胫骨近端PPARγ2蛋白表达水平的影响
与假手术组大鼠比较,去卵巢组大鼠胫骨近端PPARγ2蛋白表达水平显著增加;与去卵巢组比较,雌激素组、金雀异黄酮组、氯化锂组和跑台组胫骨近端PPARγ2蛋白表达水平均显著降低,振动组胫骨近端PPARγ2蛋白表达水平未见显著变化。
3 讨论
随着年龄的增加,众多妇女绝经后不仅骨量急剧下降,腹部脂肪也随之增加,易发生骨质疏松和代谢综合征[12]。本研究中,大鼠去卵巢后体重和腹腔内脂肪重量显著增加,经雌激素、金雀异黄酮、跑台运动和全身垂直振动干预后,体重和腹腔内脂肪重量均显著下降,而经氯化锂干预后,体重和腹腔内脂肪重量均未见显著变化。结果提示:除氯化锂外,雌激素、金雀异黄酮、跑台运动和全身垂直振动干预处理均能显著抑制大鼠由去卵巢导致的肥胖。
骨髓脂肪增加和骨量下降的相关性有助于更好地理解骨丢失的病理及绝经后骨质疏松的预防和治疗[13]。有研究表明,去卵巢大鼠骨髓脂肪增加伴随骨量下降[14]。Somjen等[15]的研究表明,天然的和人工合成的雌激素均能逆转由去卵巢诱导的骨髓脂肪发生。我们的前期研究表明,跑台运动能抑制去卵巢大鼠骨髓脂肪数目的增加[16]。已有研究表明,氯化锂不仅可产生抗成脂发生的效应[17],且具有促进成骨发生的效应[18]。本研究中,雌激素、金雀异黄酮、跑台运动、全身振动和氯化锂干预8周均能显著抑制去卵巢骨质疏松大鼠骨髓脂肪细胞数量的增加。结果提示:雌激素、金雀异黄酮、跑台运动、全身振动和氯化锂对去卵巢骨质疏松大鼠的干预效应与其抗骨髓脂肪发生有关。至于干预效应是否和促进成骨发生有关,还有待实验证实。
骨髓脂肪细胞的分化受核受体家族PPAR的调节。转录因子PPARγ的缺乏能减少小鼠骨髓脂肪含量,加强成骨发生[19]。相反,成骨细胞过表达PPARγ能加快由去卵巢导致的骨质疏松的发生[20]。为了探讨雌激素、金雀异黄酮、跑台运动、全身垂直振动和氯化锂减少去卵巢骨质疏松大鼠骨髓脂肪数目的机制,本文采用免疫印迹方法检测PPARγ2蛋白表达水平的变化。结果表明:雌激素、金雀异黄酮、跑台运动和氯化锂干预均能抑制去卵巢骨质疏松大鼠胫骨近端PPARγ2蛋白的表达水平,而全身垂直振动却无此抑制效应。
4 结论
结果表明,雌激素、跑台运动、金雀异黄酮和氯化锂干预均可能通过抑制去卵巢骨质疏松大鼠骨组织PPARγ2蛋白表达水平而抑制去卵巢骨质疏松大鼠骨髓基质细胞向脂肪细胞的分化,而全身垂直振动对去卵巢骨质疏松大鼠骨髓基质细胞向脂肪细胞分化的抑制效应可能与PPARγ2蛋白表达水平无关。
参考文献:
[1]JEREMIAH M P,UNWIN B K,GREENAWALD M H,et al.Diagnosis and management of osteoporosis[J].Am Fam Physician,2015,92(4):263.
[2]MAEDA S S,LAZARETTICASTRO M.An overview on the treatment of postmenopausal osteoporosis[J].Arq Bras Endocrinol Metabol,2014,58(2):168.
[3]MARAKA S,Kennel K A.Bisphosphonates for the prevention and management of postmenopausal osteoporosis[J].BMJ,2015,351:3783.
[4]WEBERRAJEK M,MIESZKOWSKI J,NIESPODZIRKI B,et al.Wholebody vibration exercise in postmenopausal osteoporosis[J].Prz Menopauzalny,2015,14(1):44.
[5]LIU H,LIU Y,YANG L,et al.Curative effects of pulsed electromagnetic fields on postmenopausal osteoporosis[J].Journal of Biomedical Engineering,2014,31(1):50.
[6]BERNABEI R,MARTONE A M,ORTOLANI E,et al.Screening,diagnosis,and treatment of osteoporosis:a brief review[J].Clin Cases Miner Bone Metab,2014,11(3):204.
[7]WEBERRAJEK M,MIESZKOWSKI J,NIESPODZISKI,et al.New antiresorptive therapies for postmenopausal osteoporosis[J].J Menopausal Med,2015,21(1):6.
[8]KUSHWAHA P,KHEDGIKAR V,GAUTAM J,et al.A novel therapeutic approach with aviuninbased isoflavonoid that en routes bone marrow cells to bone formation via BMP2/Wntβcatenin signaling[J].Cell Death Dis,2014(5):1422.
[9]FAN J Z,WANG Y,MENG Y,et al.Panax notoginseng saponins mitigate ovariectomyinduced bone loss and inhibit marrow adiposity in rats[J] .Menopause,2015,22(12):1347.
[10]ZHUANG H,ZHANG X,ZHU C,et al.Molecular Mechanisms of PPARγ Governing MSC Osteogenic and Adipogenic Differentiation[J].Curr Stem Cell Res Ther,2016,11(3):255.
[11]郭盖,卜淑敏,韩天雨.不同干预疗法对去卵巢骨质疏松大鼠子宫GSK3β蛋白表达的影响[J].中国实验动物学报,2014,22(5):54.
[12]JUNG S R,KIM S H,AHN N Y,et al.A novel therapeutic approach with Caviuninbased isoflavonoid that en routes bone marrow cells to bone formation via BMP2/Wntβcatenin signaling[J].Cell Death Dis,2014(5):1422.
[13]LI G W,XU Z,CHANG S X,et al.Influence of early zoledronic acid administration on bone marrow fat in ovariectomized rats[J].Endocrinology,2014,155(12):4736.
[14]YAN G F,YUAN P W,HAO Y Q,et al.Emodin enhances osteogenesis and inhibits adipogenesis[J].BMC Complement Altern Med,2014(14):74.
[15]SOMJEN D,KATZBURG S,KOHEN F,et al.The effects of native and synthetic estrogenic compounds as well as vitamin D lesscalcemic analogs on adipocytes content in rat bone marrow[J].J Endocrinol Invest,2011,34(2):108.
[16]CHEN Y,WANG S,BU S,et al.Treadmill training prevents bone loss by inhibition of PPARγ expression but not promoting of Runx2 expression in ovariectomized rats[J].Eur Appl Physiol,2011,111(8):1764.
[17]MAI Y,ZHANG Z,YANG H,et al.BMP and activin membranebound inhibitor(BAMBI) inhibits the adipogenesis of porcine preadipocytes through Wnt/βcatenin signaling pathway[J].Biochem Cell Biol,2014,92(3):179.
[18]GALLI C,PIEMONTESE M,LUMETTI S,et al.GSK3binhibitor lithium chloride enhances activation of Wnt canonical signaling and osteoblast differentiation on hydrophilic titanium surfaces[J].Clin Oral Implants Res,2013,24(8):925.
[19]ZHAO X Y,CHEN X Y,ZHANG Z J,et al.Expression patterns of transcription factor PPARγ and C/EBP family members during in vitro adipogenesis of human bone marrow mesenchymal stem cells[J].Cell Biol Int,2015,39(4):462.
[20]CHO S W,YANG J Y,HER S J,et al.Osteoblasttargeted overexpression of PPARγ inhibited bone mass gain in male mice and accelerated ovariectomyinduced bone loss in female mice[J].J Bone Miner Res,2011,26(8):1949.
[21]TANG L,CHEN Y,PEI F,et al.Lithium Chloride Modulates Adipogenesis and Osteogenesis of Human Bone MarrowDerived Mesenchymal Stem Cells[J].Cell Physiol Biochem,2015,37(1):150.
[22]ZHANG Y,MA C,LIU X,et al.Epigenetic landscape in PPARγ2 in the enhancement of adipogenesis of mouse osteoporotic bone marrow stromal cell[J].Biochim Biophys Acta,2015,1852(11):2514.
- 浅谈寓德育于语文课堂教学中
- 论语文教师专业化发展的内在动力与实现途径
- 惜花伤春的无限心曲
- 孤独的旷世奇才:苏轼
- 戏解《将进酒》另眼看太白
- 浅析陶渊明诗歌语言真
- 尊重的艺术
- 温情话民生 儒雅显风范
- 只有爱是远远不够的
- 有心无意教语文
- 课堂教学的预设和生成
- 肯定
- 教育是爱的共鸣
- 漫谈中学生的学、练、考
- 语文教师的“五福宝地”
- 古代诗歌鉴赏的四维能力训练方法
- 和青年教师谈课程改革
- 把学生学习的权利还给学生
- 新课程中学生角色转变的探索
- 语文的发现学习与接受学习
- 自主探究教学必须注重的“六性”
- 论语文教学中口语交际能力的培养
- 浅谈新课程背景下语文教学中的情感因素
- 对语文教学行为正当有效的几个追求
- 为有枝头“暗香”来
- underutilised
- underutilization
- underutilized
- undervalue
- undervalued
- undervaluer
- undervalues
- undervaluing
- undervalve
- undervalves
- under-vassal
- undervaulted
- undervegetation
- undervegetations
- underventilate
- underventilated
- underventilates
- underventilating
- underverse
- underverses
- undervicar
- yakkers
- yakking
- yaks
- yak²
- 饣
- 饣亶粥
- 饣亶酏
- 饣亶食
- 饣亶麋
- 饤
- 饤坐梨
- 饤坐男
- 饤坐黎
- 饤座
- 饤座梨
- 饤座男
- 饤饾
- 饥
- 饥一顿,饱一顿
- 饥不及餐
- 饥不可食,寒不可衣
- 饥不可食, 寒不可衣。
- 饥不择食
- 饥不择食,寒不择衣
- 饥不择食,寒不择衣,慌不择路,贫不择妻
- 饥不择食, 寒不择衣, 慌不择路, 贫不择妻。
- 饥不暇食
- 饥不泽食
- 饥不遑食