王迪 左伟伟
摘? ? ? 要: 膦-醛分子是合成手性氮膦配体的重要原料,但由于膦-醛的两性结构,很难获得高的产率和纯度。使用稳定的鏻盐作为前体和碱反应是合成膦-醛分子的有利方法。通过二苯基膦钾和2-甲磺酸甲酯-6-二甲氧基甲基吡啶3反应获得含磷基的缩醛,在酸催化下合成吡啶基鏻盐[-PPh2CH2C5H3NCHOH)]4(Cl)4 4。根据核磁和X射线单晶衍射发现,该化合物是4缩聚形成的24元大环结构,且和碱反应可成功获得含有氮活性位點的不稳定的膦醛分子PPh2CH2C5H3NCHO 5。
关? 键? 词:鏻盐;膦-醛结构;氮活性位点
中图分类号:TQ 031.2? ? ? ?文献标识码: A? ? ? ?文章编号: 1671-0460(2019)09-2025-04
Abstract: Phosphine-aldehyde molecules are important raw materials for the synthesis of chiral N/P ligands. Due to the amphoteric structure, it is difficult to obtain high yields and purity of phosphine-aldehydes. A solution way is to use stable sulfonium salts as a precursor, it reacts with base to produce the phosphine-aldehyde molecules. A new pyridylphosphonium salt [-PPh2CH2C5H3NCHOH)]4(Cl)4 4 is obtained from the reaction of phosphine-aldehydes with acid. According to the nuclear magnetic resonance and X-ray single crystal diffraction, the compound 4 is a 24-membered macrocyclic structure formed by 4-condensation, and the reaction with a base can successfully obtain unstable phosphine-aldehydes PPh2CH2C5H3NCHO 5 containing nitrogen active sites.
Key words: Phosphonium salts; Phosphine-aldehyde structures; Nitrogen active site
鏻盐作为多种有机膦化合物的重要原料,在离子液体[1]、抗肿瘤剂[2]、抗菌剂[3]以及多种生物[4,5]和化工原料[6-9]的合成中有广泛的应用。另外,随着手性现象的发现,作为叶立德和受抑的lewis对的前体,鏻盐衍生物在有机和不对称合成中的应用逐渐增加[10-12],尤其是作为手性氮磷配体的原料受到广泛关注。其中磷原子是相对较“软”的π受体,可以在P,P或N,N配体中稳定金属中心,而氮原子是较“硬”的σ供体,与金属中心产生较弱的配位,容易在溶液中解离以提供用于底物配位的空位[13]。
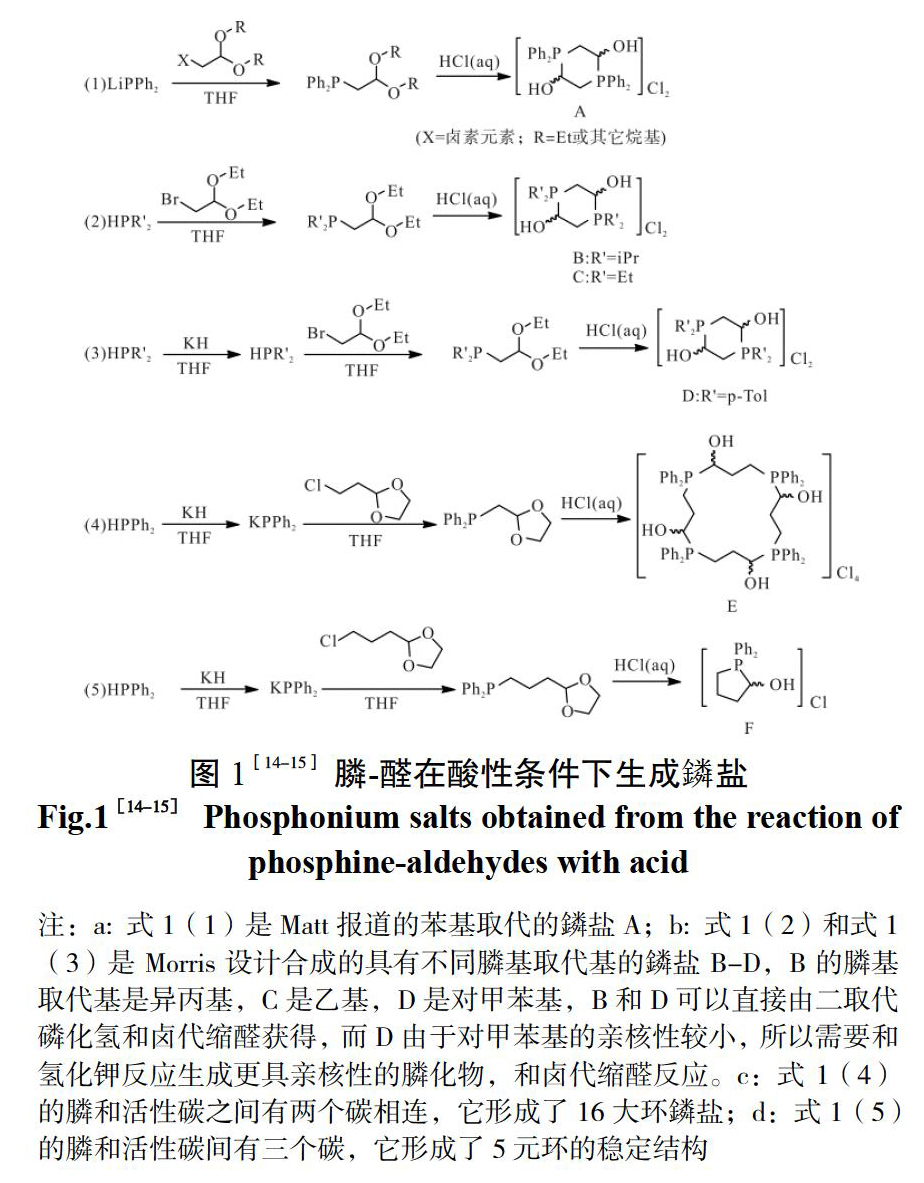
含有膦基和亲电基团的如醛基的分子是合成氮磷配体的重要原料,但由于膦带有孤对电子,可和亲电基团发生亲电加成形成CP键,从而发生非选择性聚合,难以获得良好的收率和纯度。Matt及其同事[14]发现,二苯基膦锂和卤代的缩乙醛反应获得的2-二苯基膦基缩乙醛在盐酸催化下,可获得稳定的鏻二聚体A,而不会发生非选择性聚合,如图1(1)所示。
根据这一现象,Morris等[15]通过改变膦上取代基和膦与活性碳之间碳原子的数目,合成了具有不同结构的鏻盐B-E,。其中A-C可作为膦-醛结构的前体,和碱反应后,可以和对映体纯的胺或二胺发生Schiff碱缩合反应,是合成手性PNNP和PNN配体的重要原料[16-20]。
谈雪峰等[21]报道了一篇有关钌的催化剂,在配体合成过程中,使用了含吡啶基的膦-醛结构作为反应中间体,最后合成了四齿钌催化剂,可用于脂类还原,特别是对于脂肪酸酯的加氢拥有高的活性。
结合上述的酸催化鏻盐合成的途径,设计合成了骨架上具有吡啶基的鏻盐,和碱反应可获得含有吡啶氮作为活性位点的膦-醛化合物,可用于氮磷配体及其催化剂的合成。
1? 吡啶基鏻盐的制备
1.1? 仪器和试剂
涉及空气敏感物质的操作均在氩气或氮气条件下使用Schlenk技术或具有N2(g)的手套箱进行。
所有溶剂在使用前使用标准程序脱气并干燥(THF使用钠干燥;CH2Cl2和MeOH使用氢化钙干燥)。先前已经报道的2-甲磺酸甲酯-6-二甲氧基甲基吡啶3根据文献合成[21,22]。所有试剂均通过商业方法购买并无需进一步纯化即可使用。使用Bruker 600 MHz光谱仪在环境温度和压力下记录NMR光谱(1H为600 MHz,13C为151 MHz,31P为243 MHz)。使用具有MoKα辐射(λ = 0.710 73)的Nonius Kappa-CCD衍射仪收集单晶X射线衍射数据。使用SHELXTL V6.1解析和细化结构。
1.2? 合成方法
在氮气的手套箱中,称量1 g的二苯基膦(5.4 mmol)倒入200 mL的Schlenk瓶中并用100 mL的四氢呋喃溶解,搅拌条件下慢慢加入氢化钾(0.24 g,5.9 mmol),发现溶液从无色逐渐变为深红色。反应1 h后,称量2-甲磺酸甲酯-6-二甲氧基甲基吡啶(1.40 g,5.4 mmol)于200 mL圆底瓶中,并在搅拌条件下慢慢将200 mL的Schlenk瓶的溶液滴加到圆底瓶中,最后溶液的颜色为浅黄色。滴加完后,搅拌5 min后,用橡皮塞密封,拿出手套箱,并加入用水稀释一倍的浓盐酸(0.9 mL,10.8 mmol),搅拌过夜,发现白色沉淀逐渐析出。产率:1.85 g,77%。1H NMR (600 MHz, MeOD) δ 8.34 (t, JHH=7.81 Hz, 1H, ArH), 7.92 (d, JHH = 7.9 Hz, 1 H, ArH), 7.49~7.40 (m, 11H, ArH), 5.77 (s, 1H, CHOH), 4.06 (s, 2H, CH2),13C NMR (151 MHz, MeOD) δ 155.31 (s, ArC), 147.52 (s, ArC), 136.72 (d, JCP = 15.0 Hz, ArC), 133.99 (d, JCP = 20.1 Hz, ArC), 130.97 (s, ArC), 130.04 (d, JCP = 7.0 Hz, ArC), 128.67 (d, JCP =5.56 Hz, ArC), 123.24 (s, ArC), 93.83 (s, CHOH), 34.65 (d, JCP =23.0 Hz, CH2),31P NMR (243 MHz, MeOD) δ 32.41, -1.86。
2? 结果与讨论
2.1? 吡啶基鏻盐及膦-醛结构的合成方案探讨
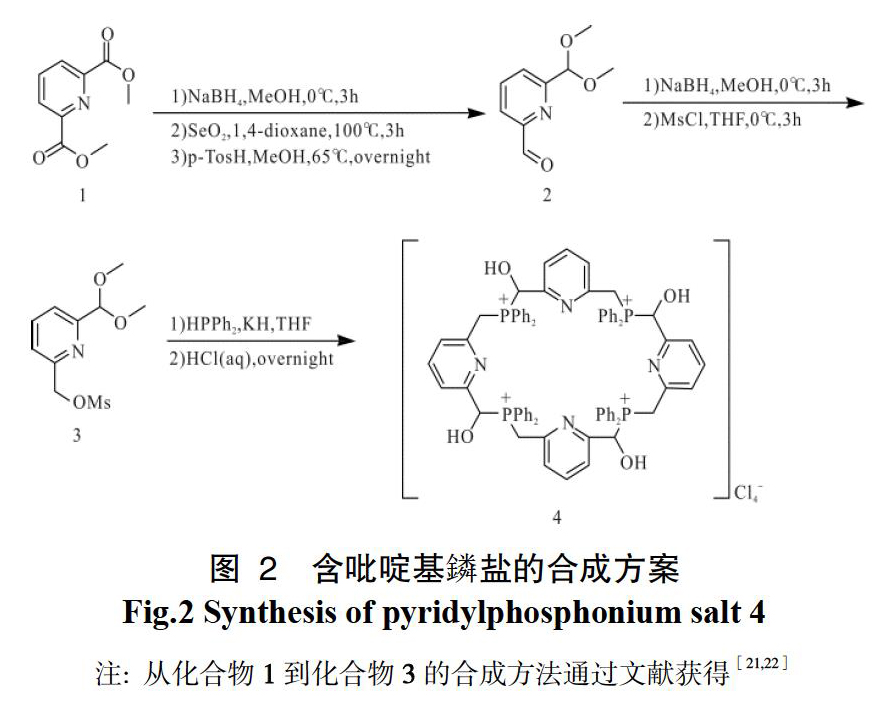
吡啶基的鏻盐的前体和膦-醛结构的合成方案如图2所示。以2,6-吡啶二甲酸二甲酯为原料,通过文献方法合成2-甲磺酸甲酯-6-二甲氧基甲基吡啶3[21,22]。二苯基膦和氢化钾反应生成的亲核性更强的二苯基膦钾和甲磺酸酯基发生亲核取代,生成2-二苯基膦甲基-6-二甲氧基甲基吡啶,是膦-缩醛的结构,以盐酸作为催化剂,可获得白色固体状的鏻盐4。该化合物对空气稳定,放置较长时间不会发生变质。
2.2? 鏻盐的核磁表征
从核磁共振膦谱上可看出,主要有两个单峰,膦的化学位移位32.41 ppm和-1.86 ppm,其中-1.86 ppm的峰是主要峰。为确定两个膦峰代表的化合物是否是鏻盐的异构体,在手套箱中将鏻盐和等当量的甲醇钠在甲醇中反应,通过核磁共振膦谱发现只有一个尖峰,化学位移为-9.64 ppm。
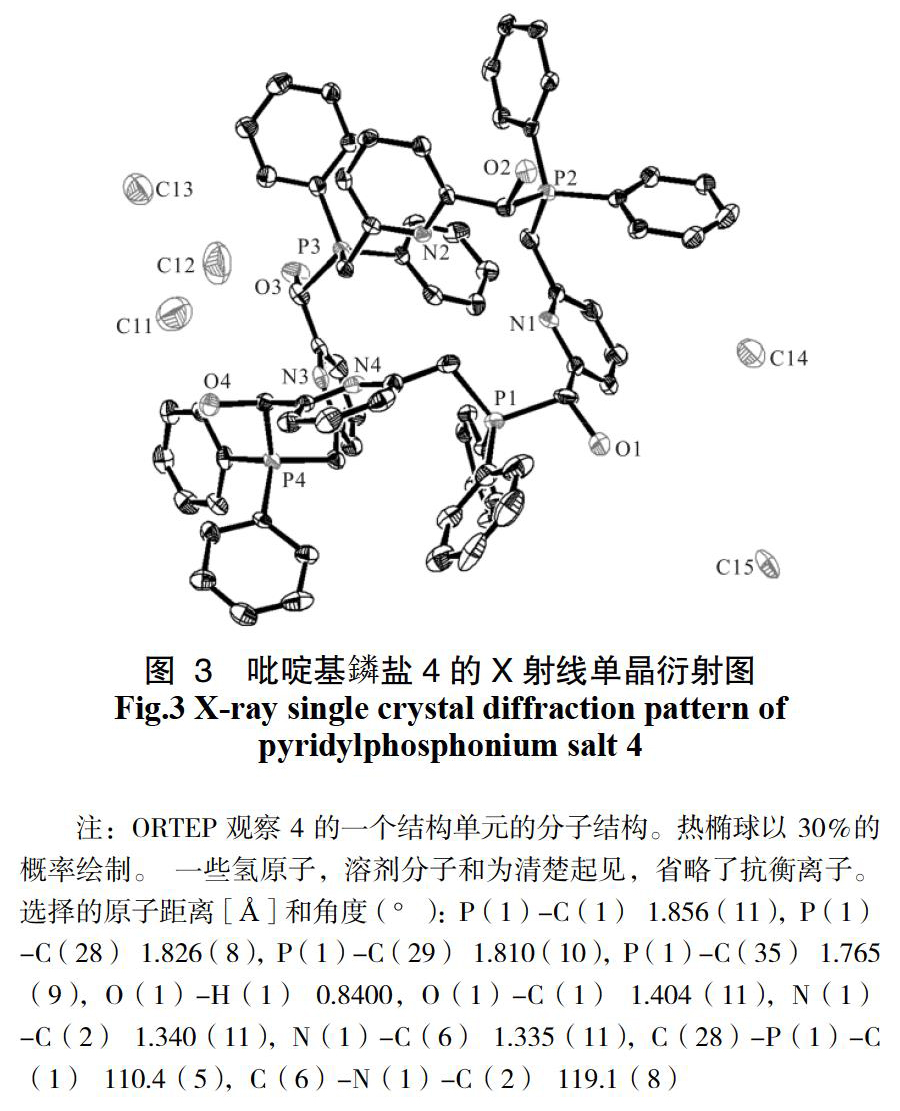
2.3? 鏻盐的X-射线单晶衍射表征
为了确定鏻盐的立体结构,以甲醇为良溶剂,乙醚为不良溶剂进行扩散结晶,并通过X射线单晶衍射获得,含吡啶基鏻盐4的单晶结构如图3所示。从图3中,可发现氧和氢的峰,说明该化合物确实有羟基生成。另外,吡啶基鏻盐的P1C1的键长和鏻盐B和C相同位置的键长相似[15],且相比于和P1相连的其他碳的键长,P1C1的键长稍大,这可能是因为相邻氧原子的吸电子效应。且根据图3可知,手性碳C2、C8和C15均为R构型,而C22为S构型。
另外,从图3中可以看出,吡啶基鏻盐是四缩聚形成的24大环分子,这可能是因为吡啶环的存在使得形成环状鏻盐的空间位阻增加,从而形成了四聚体的结构。另外,从图3中发现,虽然加入了过量的盐酸,但吡啶基的氮没有和氢配位,这可能是因为首先发生的是鏻盐的合成,由于鏻盐从四氢呋喃溶液中析出导致氮和氢无法发生配位,具体的原因还需进一步探索。
3? 鏻盐和碱反应生成膦-醛分子
吡啶基鏻盐4在碱的作用下可重新生成6-二苯基膦甲基吡啶-2-甲醛5,推测的机理是强碱拔去羟基的氢,使得氧带负电荷,进攻相邻碳原子,最后负电荷传递到膦上,发生碳膦键的断裂,获得膦-醛结构。需要注意的是,因为膦是亲核基团,醛基是亲电基团,故膦-醛分子5不稳定,膦会进攻醛基带正电荷的碳变质,可从核磁共振膦谱上观察到在-10 ppm左右有多个尖峰,且核磁共振氢谱上9-10 ppm處醛的活泼氢的峰消失(图4)。
4? 结 论
因为膦基是亲核试剂,而醛基是亲电试剂,所以膦-醛分子为两性分子,易于发生非选择性聚合而不稳定。通过形成稳定鏻盐前体的方法可以对它进行保存,且和强碱反应又可生成膦-醛的结构。本文通过含吡啶基的卤代缩醛和二苯基膦钾反应获得的膦-缩醛结构可在酸性条件下生成相应的鏻盐4,是四缩聚形成的24元大环的结构,在空气中稳定,且通过核磁和X射线单晶衍射确定了它的结构,可用于氮膦配体及其催化剂的合成。
参考文献:
[1] Ermolaev V, Gerasimova T, Kadyrgulova L, et al. Ferrocene -Containing Sterically Hindered Phosphonium Salts[J]. Molecules, 2018, 23(11): 2773.
[2] Basova N E, Rozengart E V, Suvorov A A. Phosphonium reversible inhibitors of cholinesterases of different animals[C].Doklady Biochemistry and Biophysics. SP MAIK Nauka/Interperiodica, 2010, 434(1): 245-249.
[3] Kagan V E, Wipf P, Stoyanovsky D, et al. Mitochondrial targeting of electron scavenging antioxidants: regulation of selective oxidation vs random chain reactions[J]. Advanced drug delivery reviews, 2009, 61(14): 1375-1385.
[4] Bernard J, Malacea-Kabbara R, Clemente G S, et al. o-Boronato-and o-Trifluoroborato–Phosphonium Salts Supported by l-α-Amino Acid Side Chain[J]. The Journal of organic chemistry, 2015, 80(9): 4289-4298.
[5] Dyapa R, Dockery L T, Walczak M A. Dehydrative glycosylation with cyclic phosphonium anhydrides[J]. Organic & biomolecular chemistry, 2017, 15(1): 51-55.
[6] Tsymbal A V, Levin V V, Struchkova M I, et al. Reductive silylation of gem-difluorinated phosphonium salts[J]. Journal of Fluorine Chemistry, 2018, 205: 58-61.
[7] Veinot A J, Todd A D K, Robertson K N, et al. A reinvestigation of mono-and bis-ethynyl phosphonium salts: structural and computational studies and new reactivity[J]. Canadian Journal of Chemistry, 2017, 96(1): 8-17.
[8] Lavigne F, Kazzi A E, Escudié Y, et al. Azavinylidenephosphoranes: A Class of Cyclic Push-Pull Carbenes[J]. Chemistry–A European Journal, 2014, 20(39): 12528-12536.
[9]Jennings E V, Nikitin K, Ortin Y, et al. Degenerate nucleophilic substitution in phosphonium salts[J]. Journal of the American Chemical Society, 2014, 136(46): 16217-16226.
[10]Golandaj A, Ahmad A, Ramjugernath D. Phosphonium Salts in Asymmetric Catalysis: A Journey in a Decade's Extensive Research Work[J]. Advanced Synthesis & Catalysis, 2017, 359(21): 3676- 3706.
[11]Kizas O A, Moiseev S K, Chaschin I S, et al. Phosphonium salts derived from α-ferrocenylvinyl cation in situ generated in sc-CO2 from ethynylferrocene by Nafion film[J]. The Journal of Supercritical Fluids, 2018, 131: 117-123.
[12]Herbay R, Bagi P, Fogassy E, et al. Preparation of P-heterocyclic phosphine boranes and optically active phosphine oxides via phosphonium salts[J]. Phosphorus, Sulfur, and Silicon and the Related Elements, 2016, 191(11-12): 1656-1657.
[13] Morris R H. Exploiting metal–ligand bifunctional reactions in the design of iron asymmetric hydrogenation catalysts[J]. Accounts of chemical research, 2015, 48(5): 1494-1502.
[14] Matt D, Ziessel R, De Cian A, et al. Synthesis of Ph2CH2C(O)H: a reinvestigation. Molecular structure of Ph2PCH(OH) CH2PPh2CH(OH) CH2Cl2. Compared coordinative properties of Ph2PCH2C(O)H and Ph2PCH2C(O)NMe2[J]. New journal of chemistry, 1996, 20(12): 1257-1263.
[15]Mikhailine A A, Lagaditis P O, Sues P E, et al. New cyclic phosphonium salts derived from the reaction of phosphine- aldehydes with acid[J]. Journal of Organometallic Chemistry, 2010, 695(14): 1824-1830.
[16]Lagaditis P O, Lough A J, Morris R H. Iron complexes for the catalytic transfer hydrogenation of acetophenone: steric and electronic effects imposed by alkyl substituents at phosphorus[J]. Inorganic chemistry, 2010, 49(21): 10057-10066.
[17] Sues P E, Lough A J, Morris R H. Stereoelectronic factors in iron catalysis: synthesis and characterization of aryl-substituted iron (II) carbonyl p–n–n–p complexes and their use in the asymmetric transfer hydrogenation of ketones[J]. Organometallics, 2011, 30(16): 4418-4431.
[18]Smith S A M, Morris R H. An Unsymmetrical Iron Catalyst for the Asymmetric Transfer Hydrogenation of Ketones[J]. Synthesis, 2015, 47(12): 1775-1779.
[19]Smith S A M, Prokopchuk D E, Morris R H. Asymmetric Transfer Hydrogenation of Ketones Using New Iron (II)(P‐NH‐N‐P′) Catalysts: Changing the Steric and Electronic Properties at Phosphorus P′[J]. Israel Journal of Chemistry, 2017, 57(12): 1204-1215.
[20] Zuo W, Lough A J, Li Y F, et al. Amine (imine) diphosphine iron catalysts for asymmetric transfer hydrogenation of ketones and imines[J]. Science, 2013, 342(6162): 1080-1083.
[21]Tan X, Wang Y, Liu Y, et al. Highly efficient tetradentate ruthenium catalyst for ester reduction: especially for hydrogenation of fatty acid esters[J]. Organic letters, 2015, 17(3): 454-457.
[22]Platas‐Iglesias C, Mato‐Iglesias M, Djanashvili K, et al. Lanthanide chelates containing pyridine units with potential application as contrast agents in magnetic resonance imaging[J]. Chemistry–A European Journal, 2004, 10(14): 3579-3590.
- 关于开展教师心理健康教育的几点思考
- 幼儿园多元文化音乐教育实施的现状问题与对策研究
- 幼儿园中动画片辅助音乐教学的现状分析与对策研究
- 浅谈幼儿园音乐情境教学建构的方法
- 如何在幼儿教育中开展德育教学
- 浅谈小学数学学习方法的指导
- 探讨数学思维与小学数学教学
- 手指游戏在幼儿园小班一日生活中的运用现状及对策研究
- 趣味教学在中学体育田径教学中的应用分析
- 音乐听觉在小学音乐课堂教学中的实践策略分析
- 小学“道德与法治”教学的有效策略
- 新课程背景下小学德育的思考
- 小学数学应用题数学情境的创设
- 现代学生观视域下小学班级管理的思考与探索
- 新冠疫情下,中学公共安全教育的策略与方法
- 中职学校职业生涯规划教育存在问题及对策
- 浅析中职留守生存在的问题及对策
- 初中数学课堂情景导入策略实践探究
- 小学英语绘本故事教学与信息技术有效整合方法探析
- 中职信息技术课程中的因材施教
- 初中语文多种文本散文阅读教学方法
- 浅谈对口高考数学高效复习的教学模式
- 中职生心理健康问题与教育举措
- 信息技术背景下微课在初中数学教学中的运用研究
- 词块教学在高中英语教学中的实施策略解读
- grit your teeth
- grit²
- grit¹
- groan
- groaned
- groaner
- groanful
- groaning
- groaningly
- groans
- grocer
- grocerdom
- groceries
- grocering
- grocers
- grocery
- grocery store
- groggier
- groggiest
- groggified
- groggily
- grogginess
- grogginesses
- groggy
- groin
- 堕甑不顾
- 堕突
- 堕簪遗珥
- 堕胎
- 堕节
- 堕落
- 堕落俗坑
- 堕落烟花
- 堕落风尘
- 堕裀
- 堕负
- 堕败
- 堕颓
- 堕马
- 堕驹子
- 堕鸢水
- 堗
- 堘
- 堙
- 堙井
- 堙倾没
- 堙厄
- 堙圮
- 堙坠
- 堙埋