超高效液相色谱串联质谱法同时快速检验全血中扎来普隆及其代谢产物
徐多麒+张蕾萍+王继芬+黄健+郭震+林宽
摘要 建立了全血中扎来普隆及其代谢产物5-氧扎来普隆和脱乙基扎来普隆超高效液相色谱-三重四级杆质谱(UPLC-TQ/MS)快速检验方法。采用改良后的QuEChERS前处理方法,全血样品用0.1%甲酸-乙腈提取,经无水MgSO4脱水净化,Waters BEH C18色谱柱分离,0.1%甲酸和0.1%甲酸-乙腈进行梯度洗脱。采用电喷雾电离,正离子(ESI+)模式扫描,多反应监测(MRM)模式检测。扎来普隆及其代谢产物在0.5~100 ng/mL范围内线性关系良好(R2≥0.997),回收率为92.0%~100.1%,相对标准偏差为1.9%~5.3%,方法检出限(S/N=3)均为0.05 ng/mL,定量限(S/N=10)在0.1~0.5 ng/mL范围内。
关键词 扎来普隆;5-氧扎来普隆;脱乙基扎来普隆;QuEChERS方法;超高效液相色谱串联质谱法
2016-01-13 收稿 ;2016-04-14接受
本文系公安部重点研究计划项目(No.201302ZDYJ002)、公安技术交流培训计划项目(No.B2014004A)和2015年北京市教委科学研究与研究生共建项目资助
E-mail:zlpbjft@sohu.com ,wangjifen58@126.com
1 引 言
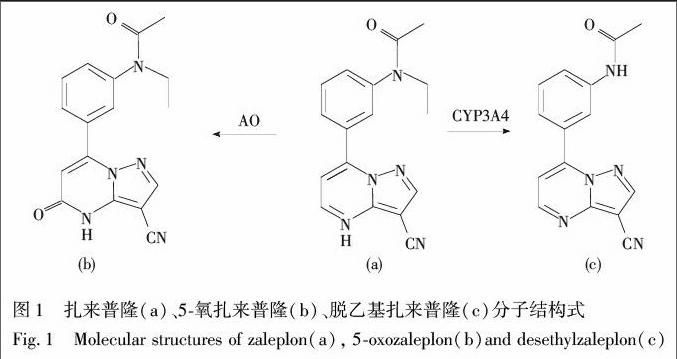
扎来普隆(Zaleplon)又名曲宁,化学名称为3-[3-氰基吡唑(1,5-a)并嘧啶-7]-N-乙基乙酰苯胺,分子式为C17H15N5O。扎来普隆为新一代非苯二氮卓类镇静催眠药的代表,与苯二氮卓类镇静催眠药相比,具有高效、低毒、成瘾性小等特点,并且半衰期短,不会产生次日的宿醉现象。该药上市后得到广泛认可,目前已广泛用于治疗失眠症。但与此同时,有不法分子利用此类药物实施麻醉抢劫、迷奸、毒驾等犯罪行为,也有将该类药物与其它毒品混合使用的案件发生[1,2]。扎来普隆主要在肝脏经醛氧化酶作用形成5-氧扎来普隆,少数经CYP3A4作用形成脱乙基扎来普隆(图1)[3]。单剂量服用扎来普隆,口服吸收快,代谢迅速,活性代谢物浓度低,且化学性质不稳定[4,5]。因此,在刑事案件中,对扎来普隆原药及其代谢物同时定性与定量检测,有利于还原案件客观情况。目前检测生物样品中扎来普隆原体的方法主要有气相色谱法[6]、液相色谱法[7]、气相色谱-质谱联用法[8]、液相色谱-质谱联用法[9~11]。但还未见同时检测扎来普隆及其两种代谢产物的报道。因此,建立一种快速、简便、高灵敏度的分析方法具有重要意义。
2002年,Anastassiades 等[12]首次提出了QuEChERS快速样品前处理方法,因其具有快速、简单、廉价、有效、可靠及安全(Quick, Easy, Cheap, Effective, Rugged and Safe)的特点而迅速成为研究热点[13]。QuEChERS前处理技术多用于农药残留检测[14~16]、临床医学[17]、兽药及医药残留[18]等领域。在法庭科学中应用鲜见报道。
本实验采用QuEChERS 前处理方法并进行了改进,超高效液相色谱-质谱联用法进行检测,建立了同时检测全血中扎来普隆及其两种代谢产物5-氧扎来普隆和脱乙基扎来普隆QuEChERS- UPLC-TQ/MS方法。在30 s内可以完成样品的测定,满足了办案中快速准确获得定性与定量分析数据的要求。
2 实验部分
2.1 仪器与试剂
Shimadzu 30A-LC超高效液相色谱仪和Shimadzu 30A 自动进样器(日本 Shimadzu 公司);API 5500 QTrap三重四级杆串联质谱仪(美国AB Sciex公司);Milli-Q去离子水发生器(美国Millipore 公司);Eyela Cute Mixer CM100高速振荡器(日本Eyela公司);高速离心机(美国Thero公司);96孔去磷酯板ISOLUTE PLD+ 50mg 96孔板(瑞典Biotage公司);PSA萃取柱SEP-Pak Vac PSA 1mL(Waters公司)。
标准品: 扎来普隆、5-氧-扎来普隆、脱乙基扎来普隆(加拿大Toronto公司);乙腈、0.1%甲酸-乙腈、甲酸、乙醇(色谱纯,Thermo Fisher公司);无水Na2SO4(分析纯,国药集团化学试剂有限公司);无水MgSO4(分析纯,北京百灵威科技有限公司)。空白血样取自北京复兴医院。
标准溶液的制备: 分别准确称取10 mg(精确到0.01 mg)的扎来普隆、5-氧扎来普隆、脱乙基扎来普隆标准品,用乙腈溶解并定容至10 mL,配制成1.0 mg/mL的标准储备液。分别吸取适量单标储备液,用乙腈逐级稀释为1.0 μg/mL的混合标准溶液,密封,于 10℃保存。使用前,用乙腈稀释至所需要的混合标准工作液。
2.2 样品制备
取0.5 mL空白血液样品置于15 mL塑料离心管中,添加200 μL混合标准品,振荡10 s,混匀后加入300 mg无水MgSO4,并加入1.3 mL 0.1%甲酸-乙腈,振荡5 min,充分混匀。使用离心机8000 r/min离心10 min。取部分上清液经0.22 μm有机膜过滤,滤液供UPLC-MS/MS分析。
2.3 检测条件
2.3.1 超高效液相色谱条件 选用Waters ACQUITY UPLC BEH C18(150 mm× 2.1 mm,1.7 μm)色谱柱; 柱温40℃; 进样量1 μL; 0.1%甲酸(A相)和0.1%甲酸-乙腈(B相)作为流动相,流速0.4 mL/min。采用4 min梯度洗脱模式: 0~0.5 min,10% B; 0.5~0.51 min,10%~50% B; 0.51~1.6 min, 50% B; 1.6~1.7 min,50%~10% B; 1.7~4.0 min, 10% B。
2.3.2 质谱条件 采用电喷雾离子源正离子扫描模式(ESI+),多反应监测扫描模式(MRM); 离子源电压(IS): 5500 V; 源温度(TEM): 600℃; 气帘气(CUR): 0.20 MPa; 喷雾气(GSI): 0.38 MPa; 辅助气(GS2): 0.34 MPa; 碰撞气(CAD): High。
3 结果与讨论
3.1 色谱条件的优化
比较了Waters ACQUITY UPLC BEH C18(150 mm×2.1 mm,1.7 μm)和ZORBAX Eclipse PlusC18(150 mm×2.1 mm,1.8 μm)两种色谱柱,前者对目标物分离效果更好,且呈现更好的峰形,因此选用Waters ACQUITY UPLC BEH C18色谱柱。
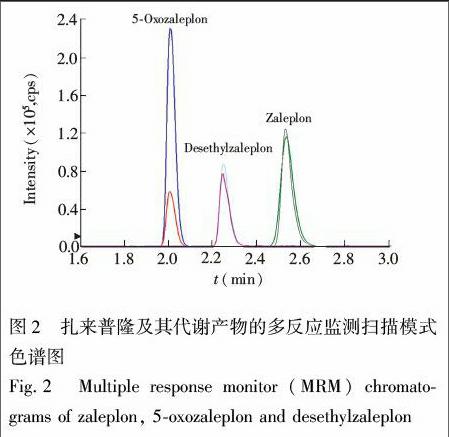
从选择性、分离效果及灵敏度角度考虑,流动相的有机相选择乙腈比甲醇更理想。从目标物分子结构分析,目标物具有氰基,能够电离吸收电子。流动相中加入适当甲酸,可以提高离子化效率。优化实验表明,使用水(A)和乙腈(B)作为流动相,3种目标物保留时间集中,无法分离。使用0.1%甲酸(V/V)(A)和0.1%甲酸-乙腈(V/V)(B)作为流动相,扎来普隆及其两种代谢产物可以实现很好的分离(图2)。
比较了3种洗梯度脱程序对目标的分离效果: (1) 0~1.0 min, 10% B; 1.0~1.1 min, 10%~90% B; 1.1~2.0 min, 90% B; 2.0~2.1 min, 90%~10% B; 2.1.0~4.0 min, 10% B。(2) 0~1.0 min, 10% B; 1.0~1.1 min, 10%~50% B; 1.1~2.0 min, 50% B; 2.0~2.1 min, 50%~10% B; 2.1~4.0 min, 10% B。(3) 0~0.5 min, 10% B; 0.5~0.51 min, 10%~50% B; 0.51~1.6 min, 50% B; 1.6~1.7 min, 50%~10% B; 1.7~4 min, 10% B。实验结果表明,第3种洗脱程序对目标物的分离效果最佳。
3.2 质谱条件的优化
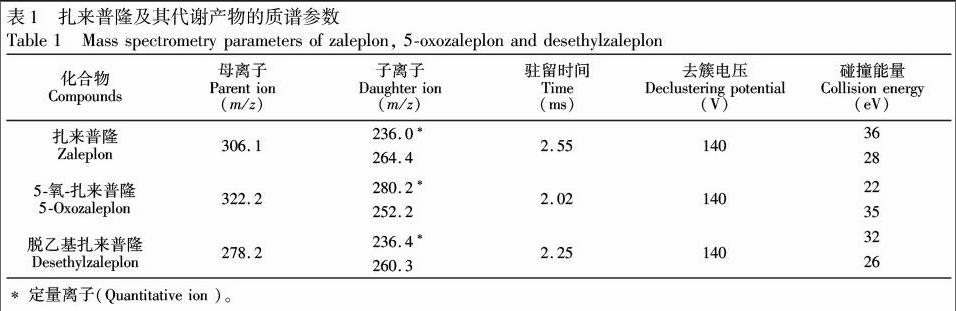
选择ESI+电离模式,使用注射针泵分别注入扎来普隆及其代谢物标准品。在m/z 100~350范围内进行母离子扫描,在一级全扫描质谱中得到母离子质量数 +。调节仪器参数,选择+作为母离子进行二级质谱裂解分析,不断增加碰撞能,子离子碎片逐渐增多。最终选定强度最高的两对子离子与母离子组成两对离子对,作为定性分析离子,并以最强的离子对作为定量分析离子。同时,对去簇电压、碰撞能量等参数进行优化。结果表明,在选定的条件下,扎来普隆及其代谢产物均有良好的色谱峰(表1)。
3.3 前处理提取溶剂的优化
基质效应是指在样品测定过程中,待测物以外的其它物质直接或间接影响待测物响应的现象[19]。随着QuEChERS方法应用范围拓宽,实验人员可根据具体实验情况对样品提取溶剂[20]、样品净化过程[21]、提取液浓缩过程[22]等进行优化,以达到降低基质效应的作用。血液样品中基质成分非常复杂,主要是内源性的磷脂、脂肪、胆固醇、甘油三酯和蛋白质[23,24]。为避免复杂的基质成分在液质检测中产生基质效应,影响定量检测,实验选用有机溶剂提取。根据文献 [24] 报道,甲酸可沉淀蛋白质和脂肪。本研究发现,在有机溶剂中添加适量甲酸(0.1%, V/V)可提高蛋白沉淀效果。因此优化前处理条件后,选择0.1%甲酸-乙腈(V/V)作为提取溶剂
为避免缓冲盐对质谱检测造成基质效应,在提取过程中未使用缓冲溶液。实验选用无水MgSO4作为脱水用盐,同时对比无水Na2SO4脱水效果。结果表明,Na2SO4遇水易板结,不易在血液中充分混匀,与文献[25]一致。
3.4 前处理净化方法的优化
样品净化的目标是要尽可能除去生物样品中的杂质,同时最大限度保留目标物,降低基质效应的同时,保证较高回收率。
考察了3种净化方法: 方法(1)为传统QuEChERS方法,将离心后的提取液过PSA(乙二胺-N-丙基)固相萃取柱,并用0.1%甲酸-乙腈洗脱、定容。PSA用于去除有机酸、酚类和少量的色素等,在农残检测中有效消除有机酸和色素等干扰,从而降低了基质效应; 方法(2)是将离心后的提取液过96 孔去磷酯板 ISOLUTE PLD,以便有效除去血液中磷脂成分,从而降低基质效应对实验的影响; 方法(3)为省略净化过程,将离心后的提取液直接经0.22 μm有机膜过滤,滤液供LC/MS分析。
采用国际上通行的 Matuszewski方法[26],比较不同条件下的峰面积平均值。考察基质效应(ME)和回收率(RE)。
A组: 标准品溶液进样分析所得峰面积; B组: 经前处理方法提取后添加标准品溶液样品,分析所得峰面积; C组: 全血中加入混合标准品溶液后经前处理方法提取所得峰面积。
3种净化方法对目标物的回收率及基质效应的影响见图3。结果表明,3种前处理方法均有效降低了基质效应,同时回收率均达到90%以上,均满足实际办案要求。综合考虑,方法(3)的回收率最高,同时简化了净化过程,一步完成萃取净化,节省了时间,减少了耗材。因此,本实验选用第3种净化方法。
3.5 方法评价
3.5.1 方法的线性范围、检出限和定量限 在优化的实验条件下进行方法学的考察。取空白全血5份各0.5 mL。分别配制成0.5, 1.0, 5.0, 10, 50和100 ng/mL标准品。按2.3节方法进行前处理后,再进行仪器分析。以不同浓度目标物的峰面积进行线性回归,结果表明,扎来普隆及其代谢产物在0.5~100 ng/mL范围内有良好线性关系,相关系数为0.9975~0.9987,以3倍信噪比(S/N)对应的添加水平作为检出限(LOD),10倍信噪比(S/N)对应的添加作为定量限(LOQ),结果见表2。
3.5.2 方法回收率和精密度 方法采用空白血样添加标准混合目标物方式,在空白血样中分别添加0.5, 5和50 ng/mL标准品,每个浓度血样平行配制3份样品, 按照2.3节的方法进行处理。通过对比峰面积计算回收率(见表3),结果令人满意。
4 结 论
采用QuEChERS方法处理样品,以超高效液相色谱-质谱法对血液中的扎来普隆及其代谢产物进行分析。通过对色谱、质谱条件和前处理方法的优化,建立了同时检测全血中扎来普隆及其代谢产物5-氧扎来普隆和脱乙基扎来普隆QuEChERS-UPLC-TQ/MS分析方法。优化的QuEChERS前处理方法综合了除蛋白方法简便快速和固相萃取方法低基质效应的优势,在有效降低基质效应的同时,保证了较高的回收率。本方法快速灵敏、回收率高,能够满足实际办案的需求。
References
1 Gunja N. Journal of Medical Toxicology, 2013, 9(2): 155-162
2 Moore K A, Zemrus T L, Ramcharitar V, Levine B, Fowler D R. Forensic Science International, 2003, 134(2-3): 120-122
3 WEN Yu-Guan, MA Cui, QIU Chang, HOU Jing, LU Xin-Qiao. Pharmaceutical Journal of Chinese People′s Liberation Army, 2004, 20(1): 24-26
温预关, 马 崔, 邱 畅, 侯 静, 陆欣乔. 解放军药学学报, 2004, 20(1): 24-26
4 Weitzel K W, Wickman J M, Augustin S G, Strom J G. Clinical Therapeutics, 2000, 22(11): 1254-1267
5 Beer B, Ieni J R, Wu WH, Clody D, Amorusi P, Rose J, Mant T, Gaudreault J, Cato A, Stern W. J. Clin. Pharmacol., 1994, 34(4): 335-344
6 ZHANG Lei-Ping, YU Zhong-Shan, HE Yi, CHANG Jing. Forensic Science and Technology, 2011, (1): 13-15
张蕾萍, 于忠山, 何 毅, 常 靖. 刑事技术, 2011, (1): 13-15
7 DENG Ming, ZHANG Su-Fen, LIU Jian-Fang, LIU Hui-Chen. Chinese Journal of Pharmaceutical Analysis, 2004, 24(6): 611-613
邓 鸣, 张素芬, 刘建芳, 刘会臣. 药物分析杂志, 2004, 24(6): 611-613
8 Karlonas N, Ramanavicius A, Ramanaviciene A. J. Sep. Sci., 2014, 37(5): 551-557
9 Montenarh D, Hopf M, Maurer H H, Schmidt P, Ewald A H. Biotechnol. Pro., 2014, 406(3): 803-818
10 ZHANG Lei-Ping, HUANG Shuang, SHU Cui-Xia. Forensic Science and Technolog, 2015, 40(1): 122-126
张蕾萍, 黄 霜, 舒翠霞. 刑事技术, 2015, 40(1): 122-126
11 MA Ren-Ling, ZHOU Hong-Hua, LIU Wen-Hua, ZHANG Xi-Yue, FAN Yu. Journal of China Pharmaceutical University, 2003, 34(4): 330-333
马仁玲, 周红华, 刘文华, 张曦岳, 范 瑜. 中国药科大学学报, 2003, 34(4): 330-333
12 Anastassiades M, Lehotay S J, Stajnbaher D, Schenck F J. J. AOAC Int., 2003, 86(2): 412-431
13 LIU Man-Man, KANG Shu, YAO Cheng. Chinese Journal of Pesticide Science, 2013, 15(1): 8-22
刘满满, 康 澍, 姚 成. 农药学学报, 2013, 15(1): 8-22
14 DONG Mao-Feng, BAI Bing, TANG Hong-Xia, WANG Wei-Min, ZHAO Zhi-Hui, HAN Zheng, SONG Wei-Guo. Chinese J. Anal. Chem., 2015, 43(5): 663-668
董茂锋, 白 冰, 唐红霞, 王伟民, 赵志辉, 韩 铮, 宋卫国. 分析化学, 2015, 43(5): 663-668
15 ZHANG Chi, SONG Ying, PAN Jia-Rong, JIAO Bi-Ning, SUI Ke, LIANG Shi-Zheng, FENG Tao, FU Li-Li. Chinese J. Anal. Chem., 2015, 43(8): 1154-1161
张 弛, 宋 莹, 潘家荣, 焦必宁, 睢 珂, 梁世正, 冯 涛, 付丽丽. 分析化学, 2015, 43(8): 1154-1161
16 LUO Yan-Bo, ZHENG Hao-Bo, JIANG Xing-Yi, LI Xue, ZHANG Hong-Fei, ZHU Feng-Peng, PANG Yong-Qiang, FENG Yu-Qi. Chinese J. Anal. Chem., 2015, 43(10): 1538-1544
罗彦波, 郑浩博, 姜兴益, 李 雪, 张洪非, 朱风鹏, 庞永强, 冯钰锜. 分析化学, 2015, 43(10): 1538-1544
17 Usui K, Hayashizaki Y, Hashiyada M, Funayama M. Legal Med., 2012, 14(6): 286-296
18 Lopes R P, Reyes R C, Romero-González R, Vidal J L, Frenich A G. J. Chromatogr. B, 2012, s895-s896(3): 39-47
19 WANG Peng, JIANG Xue-Hua, WANG Ling. Chinese Journal of New Drugs, 2011, (20): 1953-1956
王 鹏, 蒋学华, 王 凌. 中国新药杂志, 2011, (20): 1953-1956
20 Lee S W, Choi J H, Cho S K, Yu H A, Abd EI-Aty A M, Shimb J H. J. Chromatogr. A, 2011, 1218(28): 4366-77
21 Cajka T, Sandy C, Bachanova V, Drabova L, Kalachova K, Pulkrabova J, Hajslova J. Anal. Chim. Acta, 2012, 743(18): 51-60
22 Ewa C, Anna S R, Ruiz J M M, Magdalena S Z. Food Chem., 2011, 125(2): 773-778
23 YAO Meng-Kan, MA Bing-Liang, MA Yue-Ming. Chin. J. Pharm. Anal., 2010, 30(12): 2436-2439
姚梦侃, 马秉亮, 马越鸣. 药物分析杂志, 2010, 30( 2): 2436-2439
24 Dmitrovic J, Chan S C, Chan S H Y. Toxicol. Lette., 2002, 134(s 1–3): 253-258
25 GUO Zhen, CHANG Jing, YANG Rui-Qin, LUAN Yu-Jing, WANG Fang-Lin, YU Zhong-Shan. Journal of Instrumental Analysis, 2015, 34(9): 986-992
郭 震, 常 靖, 杨瑞琴, 栾玉静, 王芳琳, 于忠山. 分析测试学报, 2015, 34(9): 986-992
26 Matuszewski B K, Constanzer M L, Chavez-Eng C M. Anal. Chem., 2003, 75(13): 3019-3030
Abstract A fast testing method was established for the determination of zaleplon and its two metabolites, 5-oxozaleplon and desethylzaleplon, in blood by ultra performance liquid chromatography tandem electrospray ionization triple quadrapole-mass spectrometry (UPLC-TQ/MS). The optimized QuEChERS (Quick, Easy, Cheap, Effective, Rugged and Safe) method was used for sample preparation. The blood samples were extracted with 0.1% acetic acid and dehydrated by adding anhydrous magnesium sulfate. The targets were separated on a Waters BEH C18 column by gradient elution with 0.1% formic acid-0.1% formic acid/acetonitrile as mobile phase, ionized with positive electrospray (ESI+), and detected under multiple reaction monitoring (MRM) mode. As a result, zaleplon and its two metabolites displayed excellent linearity in the concentration of 0.5-100 ng/mL (R2>0.997). The average recoveries ranged from 92.0% to 100.1%. The RSD were in the range of 1.9%-5.3%. Besides, the limit of detection(LOD)of this method for target drugs was 0.05 ng/mL (S/N=3), while limits of quantification (LOQ) were in the range of 0.1-0.5 ng/mL (S/N=10) . This method can meet the demand of rapidity and accuracy in the analysis of actual cases.
Keywords Zaleplon; 5-Oxozaleplon; Desethylzaleplon; QuEChERS; Ultra performance liquid chromatography-mass spectrometry



摘要 建立了全血中扎来普隆及其代谢产物5-氧扎来普隆和脱乙基扎来普隆超高效液相色谱-三重四级杆质谱(UPLC-TQ/MS)快速检验方法。采用改良后的QuEChERS前处理方法,全血样品用0.1%甲酸-乙腈提取,经无水MgSO4脱水净化,Waters BEH C18色谱柱分离,0.1%甲酸和0.1%甲酸-乙腈进行梯度洗脱。采用电喷雾电离,正离子(ESI+)模式扫描,多反应监测(MRM)模式检测。扎来普隆及其代谢产物在0.5~100 ng/mL范围内线性关系良好(R2≥0.997),回收率为92.0%~100.1%,相对标准偏差为1.9%~5.3%,方法检出限(S/N=3)均为0.05 ng/mL,定量限(S/N=10)在0.1~0.5 ng/mL范围内。
关键词 扎来普隆;5-氧扎来普隆;脱乙基扎来普隆;QuEChERS方法;超高效液相色谱串联质谱法
2016-01-13 收稿 ;2016-04-14接受
本文系公安部重点研究计划项目(No.201302ZDYJ002)、公安技术交流培训计划项目(No.B2014004A)和2015年北京市教委科学研究与研究生共建项目资助
E-mail:zlpbjft@sohu.com ,wangjifen58@126.com
1 引 言
扎来普隆(Zaleplon)又名曲宁,化学名称为3-[3-氰基吡唑(1,5-a)并嘧啶-7]-N-乙基乙酰苯胺,分子式为C17H15N5O。扎来普隆为新一代非苯二氮卓类镇静催眠药的代表,与苯二氮卓类镇静催眠药相比,具有高效、低毒、成瘾性小等特点,并且半衰期短,不会产生次日的宿醉现象。该药上市后得到广泛认可,目前已广泛用于治疗失眠症。但与此同时,有不法分子利用此类药物实施麻醉抢劫、迷奸、毒驾等犯罪行为,也有将该类药物与其它毒品混合使用的案件发生[1,2]。扎来普隆主要在肝脏经醛氧化酶作用形成5-氧扎来普隆,少数经CYP3A4作用形成脱乙基扎来普隆(图1)[3]。单剂量服用扎来普隆,口服吸收快,代谢迅速,活性代谢物浓度低,且化学性质不稳定[4,5]。因此,在刑事案件中,对扎来普隆原药及其代谢物同时定性与定量检测,有利于还原案件客观情况。目前检测生物样品中扎来普隆原体的方法主要有气相色谱法[6]、液相色谱法[7]、气相色谱-质谱联用法[8]、液相色谱-质谱联用法[9~11]。但还未见同时检测扎来普隆及其两种代谢产物的报道。因此,建立一种快速、简便、高灵敏度的分析方法具有重要意义。
2002年,Anastassiades 等[12]首次提出了QuEChERS快速样品前处理方法,因其具有快速、简单、廉价、有效、可靠及安全(Quick, Easy, Cheap, Effective, Rugged and Safe)的特点而迅速成为研究热点[13]。QuEChERS前处理技术多用于农药残留检测[14~16]、临床医学[17]、兽药及医药残留[18]等领域。在法庭科学中应用鲜见报道。
本实验采用QuEChERS 前处理方法并进行了改进,超高效液相色谱-质谱联用法进行检测,建立了同时检测全血中扎来普隆及其两种代谢产物5-氧扎来普隆和脱乙基扎来普隆QuEChERS- UPLC-TQ/MS方法。在30 s内可以完成样品的测定,满足了办案中快速准确获得定性与定量分析数据的要求。
2 实验部分
2.1 仪器与试剂
Shimadzu 30A-LC超高效液相色谱仪和Shimadzu 30A 自动进样器(日本 Shimadzu 公司);API 5500 QTrap三重四级杆串联质谱仪(美国AB Sciex公司);Milli-Q去离子水发生器(美国Millipore 公司);Eyela Cute Mixer CM100高速振荡器(日本Eyela公司);高速离心机(美国Thero公司);96孔去磷酯板ISOLUTE PLD+ 50mg 96孔板(瑞典Biotage公司);PSA萃取柱SEP-Pak Vac PSA 1mL(Waters公司)。
标准品: 扎来普隆、5-氧-扎来普隆、脱乙基扎来普隆(加拿大Toronto公司);乙腈、0.1%甲酸-乙腈、甲酸、乙醇(色谱纯,Thermo Fisher公司);无水Na2SO4(分析纯,国药集团化学试剂有限公司);无水MgSO4(分析纯,北京百灵威科技有限公司)。空白血样取自北京复兴医院。
标准溶液的制备: 分别准确称取10 mg(精确到0.01 mg)的扎来普隆、5-氧扎来普隆、脱乙基扎来普隆标准品,用乙腈溶解并定容至10 mL,配制成1.0 mg/mL的标准储备液。分别吸取适量单标储备液,用乙腈逐级稀释为1.0 μg/mL的混合标准溶液,密封,于 10℃保存。使用前,用乙腈稀释至所需要的混合标准工作液。
2.2 样品制备
取0.5 mL空白血液样品置于15 mL塑料离心管中,添加200 μL混合标准品,振荡10 s,混匀后加入300 mg无水MgSO4,并加入1.3 mL 0.1%甲酸-乙腈,振荡5 min,充分混匀。使用离心机8000 r/min离心10 min。取部分上清液经0.22 μm有机膜过滤,滤液供UPLC-MS/MS分析。
2.3 检测条件
2.3.1 超高效液相色谱条件 选用Waters ACQUITY UPLC BEH C18(150 mm× 2.1 mm,1.7 μm)色谱柱; 柱温40℃; 进样量1 μL; 0.1%甲酸(A相)和0.1%甲酸-乙腈(B相)作为流动相,流速0.4 mL/min。采用4 min梯度洗脱模式: 0~0.5 min,10% B; 0.5~0.51 min,10%~50% B; 0.51~1.6 min, 50% B; 1.6~1.7 min,50%~10% B; 1.7~4.0 min, 10% B。
2.3.2 质谱条件 采用电喷雾离子源正离子扫描模式(ESI+),多反应监测扫描模式(MRM); 离子源电压(IS): 5500 V; 源温度(TEM): 600℃; 气帘气(CUR): 0.20 MPa; 喷雾气(GSI): 0.38 MPa; 辅助气(GS2): 0.34 MPa; 碰撞气(CAD): High。
3 结果与讨论
3.1 色谱条件的优化
比较了Waters ACQUITY UPLC BEH C18(150 mm×2.1 mm,1.7 μm)和ZORBAX Eclipse PlusC18(150 mm×2.1 mm,1.8 μm)两种色谱柱,前者对目标物分离效果更好,且呈现更好的峰形,因此选用Waters ACQUITY UPLC BEH C18色谱柱。
从选择性、分离效果及灵敏度角度考虑,流动相的有机相选择乙腈比甲醇更理想。从目标物分子结构分析,目标物具有氰基,能够电离吸收电子。流动相中加入适当甲酸,可以提高离子化效率。优化实验表明,使用水(A)和乙腈(B)作为流动相,3种目标物保留时间集中,无法分离。使用0.1%甲酸(V/V)(A)和0.1%甲酸-乙腈(V/V)(B)作为流动相,扎来普隆及其两种代谢产物可以实现很好的分离(图2)。
比较了3种洗梯度脱程序对目标的分离效果: (1) 0~1.0 min, 10% B; 1.0~1.1 min, 10%~90% B; 1.1~2.0 min, 90% B; 2.0~2.1 min, 90%~10% B; 2.1.0~4.0 min, 10% B。(2) 0~1.0 min, 10% B; 1.0~1.1 min, 10%~50% B; 1.1~2.0 min, 50% B; 2.0~2.1 min, 50%~10% B; 2.1~4.0 min, 10% B。(3) 0~0.5 min, 10% B; 0.5~0.51 min, 10%~50% B; 0.51~1.6 min, 50% B; 1.6~1.7 min, 50%~10% B; 1.7~4 min, 10% B。实验结果表明,第3种洗脱程序对目标物的分离效果最佳。
3.2 质谱条件的优化
选择ESI+电离模式,使用注射针泵分别注入扎来普隆及其代谢物标准品。在m/z 100~350范围内进行母离子扫描,在一级全扫描质谱中得到母离子质量数 +。调节仪器参数,选择+作为母离子进行二级质谱裂解分析,不断增加碰撞能,子离子碎片逐渐增多。最终选定强度最高的两对子离子与母离子组成两对离子对,作为定性分析离子,并以最强的离子对作为定量分析离子。同时,对去簇电压、碰撞能量等参数进行优化。结果表明,在选定的条件下,扎来普隆及其代谢产物均有良好的色谱峰(表1)。
3.3 前处理提取溶剂的优化
基质效应是指在样品测定过程中,待测物以外的其它物质直接或间接影响待测物响应的现象[19]。随着QuEChERS方法应用范围拓宽,实验人员可根据具体实验情况对样品提取溶剂[20]、样品净化过程[21]、提取液浓缩过程[22]等进行优化,以达到降低基质效应的作用。血液样品中基质成分非常复杂,主要是内源性的磷脂、脂肪、胆固醇、甘油三酯和蛋白质[23,24]。为避免复杂的基质成分在液质检测中产生基质效应,影响定量检测,实验选用有机溶剂提取。根据文献 [24] 报道,甲酸可沉淀蛋白质和脂肪。本研究发现,在有机溶剂中添加适量甲酸(0.1%, V/V)可提高蛋白沉淀效果。因此优化前处理条件后,选择0.1%甲酸-乙腈(V/V)作为提取溶剂
为避免缓冲盐对质谱检测造成基质效应,在提取过程中未使用缓冲溶液。实验选用无水MgSO4作为脱水用盐,同时对比无水Na2SO4脱水效果。结果表明,Na2SO4遇水易板结,不易在血液中充分混匀,与文献[25]一致。
3.4 前处理净化方法的优化
样品净化的目标是要尽可能除去生物样品中的杂质,同时最大限度保留目标物,降低基质效应的同时,保证较高回收率。
考察了3种净化方法: 方法(1)为传统QuEChERS方法,将离心后的提取液过PSA(乙二胺-N-丙基)固相萃取柱,并用0.1%甲酸-乙腈洗脱、定容。PSA用于去除有机酸、酚类和少量的色素等,在农残检测中有效消除有机酸和色素等干扰,从而降低了基质效应; 方法(2)是将离心后的提取液过96 孔去磷酯板 ISOLUTE PLD,以便有效除去血液中磷脂成分,从而降低基质效应对实验的影响; 方法(3)为省略净化过程,将离心后的提取液直接经0.22 μm有机膜过滤,滤液供LC/MS分析。
采用国际上通行的 Matuszewski方法[26],比较不同条件下的峰面积平均值。考察基质效应(ME)和回收率(RE)。
A组: 标准品溶液进样分析所得峰面积; B组: 经前处理方法提取后添加标准品溶液样品,分析所得峰面积; C组: 全血中加入混合标准品溶液后经前处理方法提取所得峰面积。
3种净化方法对目标物的回收率及基质效应的影响见图3。结果表明,3种前处理方法均有效降低了基质效应,同时回收率均达到90%以上,均满足实际办案要求。综合考虑,方法(3)的回收率最高,同时简化了净化过程,一步完成萃取净化,节省了时间,减少了耗材。因此,本实验选用第3种净化方法。
3.5 方法评价
3.5.1 方法的线性范围、检出限和定量限 在优化的实验条件下进行方法学的考察。取空白全血5份各0.5 mL。分别配制成0.5, 1.0, 5.0, 10, 50和100 ng/mL标准品。按2.3节方法进行前处理后,再进行仪器分析。以不同浓度目标物的峰面积进行线性回归,结果表明,扎来普隆及其代谢产物在0.5~100 ng/mL范围内有良好线性关系,相关系数为0.9975~0.9987,以3倍信噪比(S/N)对应的添加水平作为检出限(LOD),10倍信噪比(S/N)对应的添加作为定量限(LOQ),结果见表2。
3.5.2 方法回收率和精密度 方法采用空白血样添加标准混合目标物方式,在空白血样中分别添加0.5, 5和50 ng/mL标准品,每个浓度血样平行配制3份样品, 按照2.3节的方法进行处理。通过对比峰面积计算回收率(见表3),结果令人满意。
4 结 论
采用QuEChERS方法处理样品,以超高效液相色谱-质谱法对血液中的扎来普隆及其代谢产物进行分析。通过对色谱、质谱条件和前处理方法的优化,建立了同时检测全血中扎来普隆及其代谢产物5-氧扎来普隆和脱乙基扎来普隆QuEChERS-UPLC-TQ/MS分析方法。优化的QuEChERS前处理方法综合了除蛋白方法简便快速和固相萃取方法低基质效应的优势,在有效降低基质效应的同时,保证了较高的回收率。本方法快速灵敏、回收率高,能够满足实际办案的需求。
References
1 Gunja N. Journal of Medical Toxicology, 2013, 9(2): 155-162
2 Moore K A, Zemrus T L, Ramcharitar V, Levine B, Fowler D R. Forensic Science International, 2003, 134(2-3): 120-122
3 WEN Yu-Guan, MA Cui, QIU Chang, HOU Jing, LU Xin-Qiao. Pharmaceutical Journal of Chinese People′s Liberation Army, 2004, 20(1): 24-26
温预关, 马 崔, 邱 畅, 侯 静, 陆欣乔. 解放军药学学报, 2004, 20(1): 24-26
4 Weitzel K W, Wickman J M, Augustin S G, Strom J G. Clinical Therapeutics, 2000, 22(11): 1254-1267
5 Beer B, Ieni J R, Wu WH, Clody D, Amorusi P, Rose J, Mant T, Gaudreault J, Cato A, Stern W. J. Clin. Pharmacol., 1994, 34(4): 335-344
6 ZHANG Lei-Ping, YU Zhong-Shan, HE Yi, CHANG Jing. Forensic Science and Technology, 2011, (1): 13-15
张蕾萍, 于忠山, 何 毅, 常 靖. 刑事技术, 2011, (1): 13-15
7 DENG Ming, ZHANG Su-Fen, LIU Jian-Fang, LIU Hui-Chen. Chinese Journal of Pharmaceutical Analysis, 2004, 24(6): 611-613
邓 鸣, 张素芬, 刘建芳, 刘会臣. 药物分析杂志, 2004, 24(6): 611-613
8 Karlonas N, Ramanavicius A, Ramanaviciene A. J. Sep. Sci., 2014, 37(5): 551-557
9 Montenarh D, Hopf M, Maurer H H, Schmidt P, Ewald A H. Biotechnol. Pro., 2014, 406(3): 803-818
10 ZHANG Lei-Ping, HUANG Shuang, SHU Cui-Xia. Forensic Science and Technolog, 2015, 40(1): 122-126
张蕾萍, 黄 霜, 舒翠霞. 刑事技术, 2015, 40(1): 122-126
11 MA Ren-Ling, ZHOU Hong-Hua, LIU Wen-Hua, ZHANG Xi-Yue, FAN Yu. Journal of China Pharmaceutical University, 2003, 34(4): 330-333
马仁玲, 周红华, 刘文华, 张曦岳, 范 瑜. 中国药科大学学报, 2003, 34(4): 330-333
12 Anastassiades M, Lehotay S J, Stajnbaher D, Schenck F J. J. AOAC Int., 2003, 86(2): 412-431
13 LIU Man-Man, KANG Shu, YAO Cheng. Chinese Journal of Pesticide Science, 2013, 15(1): 8-22
刘满满, 康 澍, 姚 成. 农药学学报, 2013, 15(1): 8-22
14 DONG Mao-Feng, BAI Bing, TANG Hong-Xia, WANG Wei-Min, ZHAO Zhi-Hui, HAN Zheng, SONG Wei-Guo. Chinese J. Anal. Chem., 2015, 43(5): 663-668
董茂锋, 白 冰, 唐红霞, 王伟民, 赵志辉, 韩 铮, 宋卫国. 分析化学, 2015, 43(5): 663-668
15 ZHANG Chi, SONG Ying, PAN Jia-Rong, JIAO Bi-Ning, SUI Ke, LIANG Shi-Zheng, FENG Tao, FU Li-Li. Chinese J. Anal. Chem., 2015, 43(8): 1154-1161
张 弛, 宋 莹, 潘家荣, 焦必宁, 睢 珂, 梁世正, 冯 涛, 付丽丽. 分析化学, 2015, 43(8): 1154-1161
16 LUO Yan-Bo, ZHENG Hao-Bo, JIANG Xing-Yi, LI Xue, ZHANG Hong-Fei, ZHU Feng-Peng, PANG Yong-Qiang, FENG Yu-Qi. Chinese J. Anal. Chem., 2015, 43(10): 1538-1544
罗彦波, 郑浩博, 姜兴益, 李 雪, 张洪非, 朱风鹏, 庞永强, 冯钰锜. 分析化学, 2015, 43(10): 1538-1544
17 Usui K, Hayashizaki Y, Hashiyada M, Funayama M. Legal Med., 2012, 14(6): 286-296
18 Lopes R P, Reyes R C, Romero-González R, Vidal J L, Frenich A G. J. Chromatogr. B, 2012, s895-s896(3): 39-47
19 WANG Peng, JIANG Xue-Hua, WANG Ling. Chinese Journal of New Drugs, 2011, (20): 1953-1956
王 鹏, 蒋学华, 王 凌. 中国新药杂志, 2011, (20): 1953-1956
20 Lee S W, Choi J H, Cho S K, Yu H A, Abd EI-Aty A M, Shimb J H. J. Chromatogr. A, 2011, 1218(28): 4366-77
21 Cajka T, Sandy C, Bachanova V, Drabova L, Kalachova K, Pulkrabova J, Hajslova J. Anal. Chim. Acta, 2012, 743(18): 51-60
22 Ewa C, Anna S R, Ruiz J M M, Magdalena S Z. Food Chem., 2011, 125(2): 773-778
23 YAO Meng-Kan, MA Bing-Liang, MA Yue-Ming. Chin. J. Pharm. Anal., 2010, 30(12): 2436-2439
姚梦侃, 马秉亮, 马越鸣. 药物分析杂志, 2010, 30( 2): 2436-2439
24 Dmitrovic J, Chan S C, Chan S H Y. Toxicol. Lette., 2002, 134(s 1–3): 253-258
25 GUO Zhen, CHANG Jing, YANG Rui-Qin, LUAN Yu-Jing, WANG Fang-Lin, YU Zhong-Shan. Journal of Instrumental Analysis, 2015, 34(9): 986-992
郭 震, 常 靖, 杨瑞琴, 栾玉静, 王芳琳, 于忠山. 分析测试学报, 2015, 34(9): 986-992
26 Matuszewski B K, Constanzer M L, Chavez-Eng C M. Anal. Chem., 2003, 75(13): 3019-3030
Abstract A fast testing method was established for the determination of zaleplon and its two metabolites, 5-oxozaleplon and desethylzaleplon, in blood by ultra performance liquid chromatography tandem electrospray ionization triple quadrapole-mass spectrometry (UPLC-TQ/MS). The optimized QuEChERS (Quick, Easy, Cheap, Effective, Rugged and Safe) method was used for sample preparation. The blood samples were extracted with 0.1% acetic acid and dehydrated by adding anhydrous magnesium sulfate. The targets were separated on a Waters BEH C18 column by gradient elution with 0.1% formic acid-0.1% formic acid/acetonitrile as mobile phase, ionized with positive electrospray (ESI+), and detected under multiple reaction monitoring (MRM) mode. As a result, zaleplon and its two metabolites displayed excellent linearity in the concentration of 0.5-100 ng/mL (R2>0.997). The average recoveries ranged from 92.0% to 100.1%. The RSD were in the range of 1.9%-5.3%. Besides, the limit of detection(LOD)of this method for target drugs was 0.05 ng/mL (S/N=3), while limits of quantification (LOQ) were in the range of 0.1-0.5 ng/mL (S/N=10) . This method can meet the demand of rapidity and accuracy in the analysis of actual cases.
Keywords Zaleplon; 5-Oxozaleplon; Desethylzaleplon; QuEChERS; Ultra performance liquid chromatography-mass spectrometry

