HPLC同时测定痛经灵颗粒中3种有效成分含量
李中娥


摘要:目的 建立高效液相色谱法同时测定痛经灵颗粒中丹酚酸B、芍药苷和羟基红花黄色素A含量的方法,为有效控制其质量提供可靠的方法。方法 采用Welchrom C18色谱柱,以乙腈(A)-0.1%磷酸(B)为流动相梯度洗脱,流速1.0 mL/min,检测波长为230 nm。结果 丹酚酸B在0.197~1.316 μg范围内呈良好的线性关系(r=0.999 6),平均回收率为98.72%,RSD=1.49%;芍药苷在0.158~1.051 μg范围内呈良好的线性关系(r=0.999 8),平均回收率为99.01%,RSD=0.92%;羟基红花黄色素A在0.053~0.353 μg范围内呈良好的线性关系(r=0.999 4),平均回收率为98.34%,RSD=1.60%。结论 该方法简便、灵敏、准确、重复性好,可用于痛经灵颗粒的质量控制。
关键词:痛经灵颗粒;丹酚酸B;芍药苷;羟基红花黄色素A;高效液相色谱法
DOI:10.3969/j.issn.1005-5304.2016.01.025
中图分类号:R284.1 文献标识码:A 文章编号:1005-5304(2016)01-0103-03
Simultaneous Determination of Three Active Ingredients in Tongjingling Granules by HPLC LI Zhong-e (Nanyang Institute for Food and Drug Control, Nanyang 473061, China)
Abstract: Objective To establish a simultaneous determination method for Salvianolic acid B, Paeoniflorin and Hydroxysafflor yellow A in Tongjingling Granules; To provide a reliable method for effective quality control. Methods The determination was performed on a Welchrom C18 column with acetonitrile (A) - 0.1% phosphoric acid (B) as the mobile phase in gradient elution mode at the flow rate of 1.0 mL/min. The detection wavelength was 230 nm. Results Salvianolic acid B presented in a good linear relation in the range of 0.197–1.316 μg, and the average recovery rate was 98.72% with RSD 1.49%; Paeoniflorin presented in a good linear relation in the range of 0.158–1.051 μg, and the average recovery rate was 99.01% with RSD 0.92%; Hydroxysafflor yellow A presented in a good linear relation in the concentration range of 0.053–0.353 μg, and the average recovery rate was 98.34% with RSD of 1.60%. Conclusion This method is simple, sensitive, accurate and with good reproducibility, which can be used for quality control of Tongjingling Granules.
Key words: Tongjingling Granules; Salvianolic acid B; Paeoniflorin; Hydroxysafflor yellow A; HPLC
痛经灵颗粒收载于《中华人民共和国卫生部药品标准·中药成方制剂》第十五册,由丹参、赤芍、香附(醋制)、蒲黄、红花、延胡索、乌药等组成,具有活血化瘀、理气止痛功效,临床用于治疗气滞血瘀所致痛经。该产品现行标准中没有含量测定项[1],无法有效控制其质量。以往报道多以原儿茶醛或芍药苷等单一成分作为质控指标[2-3],本研究参考有关文献[4-8],对样品处理方法和色谱分离系统进行优化,采用高效液相色谱法(HPLC)同时对方中3味主药的特征性活性成分丹酚酸B、芍药苷、羟基红花黄色素A含量进行测定,从而在简化检测步骤、节约检测资源的情况下,更好地控制该药品的质量。
1 仪器与试药
Agilent 1260高效液相色谱仪,配四元梯度泵、G1314F紫外检测器;赛多利斯BP-211D电子天平;KQ-300DE型数控超声波仪(昆山市超声仪器有限公司)。
对照品丹酚酸B(批号111562-201110,含量98.0%)、芍药苷(批号110736-201035,含量96.5%)、羟基红花黄色素A(批号111637-200905,含量91.8%)均购自中国食品药品检定研究院,乙腈(HPLC,Welch Materials Inc.),磷酸(分析纯,天津市福晨化学试剂厂),水为重蒸馏水。痛经灵颗粒(市售)。
2 方法与结果
2.1 色谱条件
色谱柱:Welchrom C18(250 mm×4.6 mm,5 μm);流动相:乙腈(A)-0.1%磷酸(B),梯度洗脱(0~12 min,12%A;12~20 min,12%A→34%A;20~30 min,34%A;30~35 min,34%A→12%A);检测波长:230 nm;流速:1.0 mL/min;柱温:35 ℃;进样量:10 μL。理论板数按羟基红花黄色素A峰计算应不低于4000,各峰之间分离度符合要求。
2.2 溶液的制备
2.2.1 对照品溶液制备 精密称取羟基红花黄色素A对照品9.62 mg,置50 mL量瓶中,加75%甲醇适量使溶解并稀释至刻度,摇匀。精密称取丹酚酸B对照品16.78 mg、芍药苷对照品13.61 mg,置25 mL量瓶中,加上述羟基红花黄色素A对照品溶液使溶解并稀释至刻度,摇匀,即得含丹酚酸B 0.657 8 mg/mL、芍药苷0.525 3 mg/mL、羟基红花黄色素A 0.176 6 mg/mL的溶液(对照品溶液①),精密量取2 mL,置20 mL量瓶中,加75%甲醇至刻度,摇匀,即得对照品溶液。
2.2.2 供试品溶液制备 取本品适量,研细,精密称取0.5 g,置具塞锥形瓶中,精密加75%甲醇25 mL,密塞,称定质量,超声提取(250 W,40 kHz)30 min,放冷,再称定质量,用75%甲醇补足减失的质量,摇匀,过滤,取续滤液,用微孔滤膜过滤,即得。
2.2.3 阴性对照溶液制备 按处方制法分别制备不含丹参、赤芍和红花的阴性对照样品,按供试品溶液制备方法分别制成阴性对照溶液。
2.3 专属性试验
吸取对照品溶液、供试品溶液和阴性对照溶液各10 μL,按“2.1”项下色谱条件分别进样,结果供试品色谱中,在与丹酚酸B、芍药苷和羟基红花黄色素A对照品色谱相同的保留时间处有色谱峰,与其他组分能达到良好分离,分离度均>1.5,理论塔板数分别为8326、10 967、13 980。阴性对照色谱中,在与丹酚酸B、芍药苷和羟基红花黄色素A对照品色谱峰相应的位置上无干扰峰,说明供试品溶液中的其他成分对测定结果无影响,见图1。
2.4 线性关系的考察
精密量取“2.2.1”项下对照品溶液① 0.3、0.6、0.9、1.2、1.6、2.0 mL,分别置10 mL量瓶中,加75%甲醇至刻度,摇匀,按“2.1”项下色谱条件测定,以浓度(μg/mL)为横坐标,峰面积为纵坐标,分别绘制标准曲线,得回归方程。丹酚酸B:Y=10.866X-1.100 9,r=0.999 6(n=6)。芍药苷:Y=7.621X+0.292 1,r=0.999 8(n=6)。羟基红花黄色素A:Y=11.834X-0.352 8,r=0.999 4(n=6)。结果表明,丹酚酸B在0.197~1.316 μg、芍药苷在0.158~1.051 μg、羟基红花黄色素A在0.053~0.353 μg范围内呈良好的线性关系。
2.5 精密度试验
取“2.2.1”项下对照品溶液,进样量10 μL,连续进样6次,测定峰面积,结果丹酚酸B、芍药苷和羟基红花黄色素A的峰面积RSD分别为0.97%、1.56%、1.22%,表明精密度良好。
2.6 重复性试验
取同一批号样品6份,按“2.2.2”项下方法制备供试品溶液,在“2.1”项色谱条件下测定每份样品中3种成分含量,结果丹酚酸B、芍药苷、羟基红花黄色素A的含量RSD分别为1.33%、0.91%、1.52%,说明重复性良好。
2.7 稳定性试验
取同一份供品溶液,分别在0、3、6、9、12 h进样测定峰面积,结果丹酚酸B、芍药苷、羟基红花黄色素A的峰面积RSD分别为1.59%、1.13%、1.27%。表明供试品溶液在12 h内稳定。
2.8 加样回收率试验
精密称取已测得含量(丹酚酸B 2.628 mg/g,芍药苷2.083 mg/g,羟基红花黄色素A 0.706 mg/g)的痛经灵颗粒6份,每份0.25 g,分别精密加入“2.2.1”项下对照品溶液①各1.0 mL,按“2.2.2”项下方法制备供试品溶液,进样测定,计算回收率,结果见表1。
2.9 样品测定
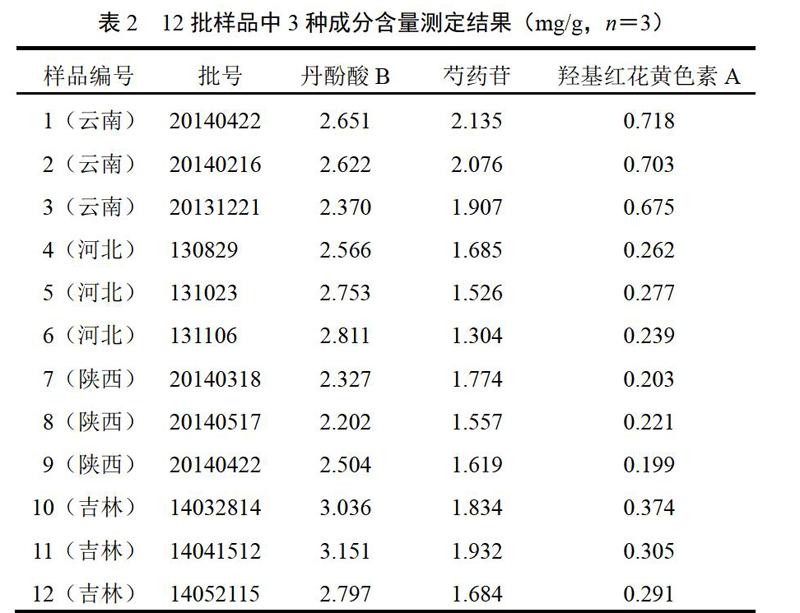
按“2.2.2”项下方法制备供试品溶液,按“2.1”项色谱条件,测定来自云南、河北、陕西、吉林不同厂家共12批样品中3种成分的含量,结果见表2。
根据12批样品所测得的结果,可看出不同厂家不同批次所含3种成分的含量有所差异,质量参差不齐,其中尤以羟基红花黄色素A的含量差别为大,可能与红花药材较贵且在成药质量标准中较少被检测有关,因此很有必要对这3种成分合理定量,从而更好地监管该药品的质量。
3 讨论
本试验比较了30%乙醇、甲醇、50%甲醇及75%甲醇几种溶剂的提取效果,结果以75%甲醇提取所得可更好兼顾3种成分的含量,故以75%甲醇为提取溶剂。因丹酚酸B对热不太稳定,故未采用回流而采用超声方式提取,试验发现超声提取25 min后,3种成分的含量无明显增加,所以将提取时间定在30 min。
在多成分同时检测中,很多需要采用转换波长的方式以取得好的效果[5-6]。本试验发现,以芍药苷的最大吸收波长230 nm作为单一检测波长,其他2种成分亦吸收稳定,响应信号良好,线性范围满足需要,故采用单波长检测,便于该方法更广泛地应用。
参考文献:
[1] 中华人民共和国卫生部药典委员会.中华人民共和国卫生部药品标准:中药成方制剂 第十五册[M].1997:209.
[2] 任红兵.痛经灵颗粒质量标准研究[J].现代中药研究与产践,2011, 25(2):76-79.
[3] 章常华,曾宗浪,施宏斌,等.痛经灵颗粒质量标准研究[J].亚太传统医药,2008,4(4):34-37.
[4] 严红.HPLC法同时测定中药多种有效成分含量的应用[J].天津药学, 2010,22(1):67-70.
[5] 厉瑶,郭正泰,龚行楚,等.丹参红花混煎液中丹参素、羟基红花黄色素A、迷迭香酸、紫草酸和丹酚酸B的HPLC测定方法[J].中国中药杂志,2013,38(11):1653-1656.
[6] 刘敏彦,赵韶华,王玉峰.超高效液相色谱法同时测定参松养心胶囊中8种活性成分的含量[J].中国医院药学杂志,2014,34(6):435-438.
[7] 贾歆.HPLC同时测定尿塞通片中的芍药苷、丹酚酸B及隐丹参酮[J].华西药学杂志,2014,29(1):77-79.
[8] 王亚洲.HPLC法同时测定蝎龙酒中芍药苷、羟基红花黄色素A和阿魏酸[J].中成药,2012,34(10):1925-1928.
(收稿日期:2014-12-02;编辑:陈静)



摘要:目的 建立高效液相色谱法同时测定痛经灵颗粒中丹酚酸B、芍药苷和羟基红花黄色素A含量的方法,为有效控制其质量提供可靠的方法。方法 采用Welchrom C18色谱柱,以乙腈(A)-0.1%磷酸(B)为流动相梯度洗脱,流速1.0 mL/min,检测波长为230 nm。结果 丹酚酸B在0.197~1.316 μg范围内呈良好的线性关系(r=0.999 6),平均回收率为98.72%,RSD=1.49%;芍药苷在0.158~1.051 μg范围内呈良好的线性关系(r=0.999 8),平均回收率为99.01%,RSD=0.92%;羟基红花黄色素A在0.053~0.353 μg范围内呈良好的线性关系(r=0.999 4),平均回收率为98.34%,RSD=1.60%。结论 该方法简便、灵敏、准确、重复性好,可用于痛经灵颗粒的质量控制。
关键词:痛经灵颗粒;丹酚酸B;芍药苷;羟基红花黄色素A;高效液相色谱法
DOI:10.3969/j.issn.1005-5304.2016.01.025
中图分类号:R284.1 文献标识码:A 文章编号:1005-5304(2016)01-0103-03
Simultaneous Determination of Three Active Ingredients in Tongjingling Granules by HPLC LI Zhong-e (Nanyang Institute for Food and Drug Control, Nanyang 473061, China)
Abstract: Objective To establish a simultaneous determination method for Salvianolic acid B, Paeoniflorin and Hydroxysafflor yellow A in Tongjingling Granules; To provide a reliable method for effective quality control. Methods The determination was performed on a Welchrom C18 column with acetonitrile (A) - 0.1% phosphoric acid (B) as the mobile phase in gradient elution mode at the flow rate of 1.0 mL/min. The detection wavelength was 230 nm. Results Salvianolic acid B presented in a good linear relation in the range of 0.197–1.316 μg, and the average recovery rate was 98.72% with RSD 1.49%; Paeoniflorin presented in a good linear relation in the range of 0.158–1.051 μg, and the average recovery rate was 99.01% with RSD 0.92%; Hydroxysafflor yellow A presented in a good linear relation in the concentration range of 0.053–0.353 μg, and the average recovery rate was 98.34% with RSD of 1.60%. Conclusion This method is simple, sensitive, accurate and with good reproducibility, which can be used for quality control of Tongjingling Granules.
Key words: Tongjingling Granules; Salvianolic acid B; Paeoniflorin; Hydroxysafflor yellow A; HPLC
痛经灵颗粒收载于《中华人民共和国卫生部药品标准·中药成方制剂》第十五册,由丹参、赤芍、香附(醋制)、蒲黄、红花、延胡索、乌药等组成,具有活血化瘀、理气止痛功效,临床用于治疗气滞血瘀所致痛经。该产品现行标准中没有含量测定项[1],无法有效控制其质量。以往报道多以原儿茶醛或芍药苷等单一成分作为质控指标[2-3],本研究参考有关文献[4-8],对样品处理方法和色谱分离系统进行优化,采用高效液相色谱法(HPLC)同时对方中3味主药的特征性活性成分丹酚酸B、芍药苷、羟基红花黄色素A含量进行测定,从而在简化检测步骤、节约检测资源的情况下,更好地控制该药品的质量。
1 仪器与试药
Agilent 1260高效液相色谱仪,配四元梯度泵、G1314F紫外检测器;赛多利斯BP-211D电子天平;KQ-300DE型数控超声波仪(昆山市超声仪器有限公司)。
对照品丹酚酸B(批号111562-201110,含量98.0%)、芍药苷(批号110736-201035,含量96.5%)、羟基红花黄色素A(批号111637-200905,含量91.8%)均购自中国食品药品检定研究院,乙腈(HPLC,Welch Materials Inc.),磷酸(分析纯,天津市福晨化学试剂厂),水为重蒸馏水。痛经灵颗粒(市售)。
2 方法与结果
2.1 色谱条件
色谱柱:Welchrom C18(250 mm×4.6 mm,5 μm);流动相:乙腈(A)-0.1%磷酸(B),梯度洗脱(0~12 min,12%A;12~20 min,12%A→34%A;20~30 min,34%A;30~35 min,34%A→12%A);检测波长:230 nm;流速:1.0 mL/min;柱温:35 ℃;进样量:10 μL。理论板数按羟基红花黄色素A峰计算应不低于4000,各峰之间分离度符合要求。
2.2 溶液的制备
2.2.1 对照品溶液制备 精密称取羟基红花黄色素A对照品9.62 mg,置50 mL量瓶中,加75%甲醇适量使溶解并稀释至刻度,摇匀。精密称取丹酚酸B对照品16.78 mg、芍药苷对照品13.61 mg,置25 mL量瓶中,加上述羟基红花黄色素A对照品溶液使溶解并稀释至刻度,摇匀,即得含丹酚酸B 0.657 8 mg/mL、芍药苷0.525 3 mg/mL、羟基红花黄色素A 0.176 6 mg/mL的溶液(对照品溶液①),精密量取2 mL,置20 mL量瓶中,加75%甲醇至刻度,摇匀,即得对照品溶液。
2.2.2 供试品溶液制备 取本品适量,研细,精密称取0.5 g,置具塞锥形瓶中,精密加75%甲醇25 mL,密塞,称定质量,超声提取(250 W,40 kHz)30 min,放冷,再称定质量,用75%甲醇补足减失的质量,摇匀,过滤,取续滤液,用微孔滤膜过滤,即得。
2.2.3 阴性对照溶液制备 按处方制法分别制备不含丹参、赤芍和红花的阴性对照样品,按供试品溶液制备方法分别制成阴性对照溶液。
2.3 专属性试验
吸取对照品溶液、供试品溶液和阴性对照溶液各10 μL,按“2.1”项下色谱条件分别进样,结果供试品色谱中,在与丹酚酸B、芍药苷和羟基红花黄色素A对照品色谱相同的保留时间处有色谱峰,与其他组分能达到良好分离,分离度均>1.5,理论塔板数分别为8326、10 967、13 980。阴性对照色谱中,在与丹酚酸B、芍药苷和羟基红花黄色素A对照品色谱峰相应的位置上无干扰峰,说明供试品溶液中的其他成分对测定结果无影响,见图1。
2.4 线性关系的考察
精密量取“2.2.1”项下对照品溶液① 0.3、0.6、0.9、1.2、1.6、2.0 mL,分别置10 mL量瓶中,加75%甲醇至刻度,摇匀,按“2.1”项下色谱条件测定,以浓度(μg/mL)为横坐标,峰面积为纵坐标,分别绘制标准曲线,得回归方程。丹酚酸B:Y=10.866X-1.100 9,r=0.999 6(n=6)。芍药苷:Y=7.621X+0.292 1,r=0.999 8(n=6)。羟基红花黄色素A:Y=11.834X-0.352 8,r=0.999 4(n=6)。结果表明,丹酚酸B在0.197~1.316 μg、芍药苷在0.158~1.051 μg、羟基红花黄色素A在0.053~0.353 μg范围内呈良好的线性关系。
2.5 精密度试验
取“2.2.1”项下对照品溶液,进样量10 μL,连续进样6次,测定峰面积,结果丹酚酸B、芍药苷和羟基红花黄色素A的峰面积RSD分别为0.97%、1.56%、1.22%,表明精密度良好。
2.6 重复性试验
取同一批号样品6份,按“2.2.2”项下方法制备供试品溶液,在“2.1”项色谱条件下测定每份样品中3种成分含量,结果丹酚酸B、芍药苷、羟基红花黄色素A的含量RSD分别为1.33%、0.91%、1.52%,说明重复性良好。
2.7 稳定性试验
取同一份供品溶液,分别在0、3、6、9、12 h进样测定峰面积,结果丹酚酸B、芍药苷、羟基红花黄色素A的峰面积RSD分别为1.59%、1.13%、1.27%。表明供试品溶液在12 h内稳定。
2.8 加样回收率试验
精密称取已测得含量(丹酚酸B 2.628 mg/g,芍药苷2.083 mg/g,羟基红花黄色素A 0.706 mg/g)的痛经灵颗粒6份,每份0.25 g,分别精密加入“2.2.1”项下对照品溶液①各1.0 mL,按“2.2.2”项下方法制备供试品溶液,进样测定,计算回收率,结果见表1。
2.9 样品测定
按“2.2.2”项下方法制备供试品溶液,按“2.1”项色谱条件,测定来自云南、河北、陕西、吉林不同厂家共12批样品中3种成分的含量,结果见表2。
根据12批样品所测得的结果,可看出不同厂家不同批次所含3种成分的含量有所差异,质量参差不齐,其中尤以羟基红花黄色素A的含量差别为大,可能与红花药材较贵且在成药质量标准中较少被检测有关,因此很有必要对这3种成分合理定量,从而更好地监管该药品的质量。
3 讨论
本试验比较了30%乙醇、甲醇、50%甲醇及75%甲醇几种溶剂的提取效果,结果以75%甲醇提取所得可更好兼顾3种成分的含量,故以75%甲醇为提取溶剂。因丹酚酸B对热不太稳定,故未采用回流而采用超声方式提取,试验发现超声提取25 min后,3种成分的含量无明显增加,所以将提取时间定在30 min。
在多成分同时检测中,很多需要采用转换波长的方式以取得好的效果[5-6]。本试验发现,以芍药苷的最大吸收波长230 nm作为单一检测波长,其他2种成分亦吸收稳定,响应信号良好,线性范围满足需要,故采用单波长检测,便于该方法更广泛地应用。
参考文献:
[1] 中华人民共和国卫生部药典委员会.中华人民共和国卫生部药品标准:中药成方制剂 第十五册[M].1997:209.
[2] 任红兵.痛经灵颗粒质量标准研究[J].现代中药研究与产践,2011, 25(2):76-79.
[3] 章常华,曾宗浪,施宏斌,等.痛经灵颗粒质量标准研究[J].亚太传统医药,2008,4(4):34-37.
[4] 严红.HPLC法同时测定中药多种有效成分含量的应用[J].天津药学, 2010,22(1):67-70.
[5] 厉瑶,郭正泰,龚行楚,等.丹参红花混煎液中丹参素、羟基红花黄色素A、迷迭香酸、紫草酸和丹酚酸B的HPLC测定方法[J].中国中药杂志,2013,38(11):1653-1656.
[6] 刘敏彦,赵韶华,王玉峰.超高效液相色谱法同时测定参松养心胶囊中8种活性成分的含量[J].中国医院药学杂志,2014,34(6):435-438.
[7] 贾歆.HPLC同时测定尿塞通片中的芍药苷、丹酚酸B及隐丹参酮[J].华西药学杂志,2014,29(1):77-79.
[8] 王亚洲.HPLC法同时测定蝎龙酒中芍药苷、羟基红花黄色素A和阿魏酸[J].中成药,2012,34(10):1925-1928.
(收稿日期:2014-12-02;编辑:陈静)

