新型石墨烯—壳聚糖/二茂铁衍生物/细胞色素c修饰电极的制备及其用于亚硝酸钠的检测研究
黄娜等

摘 要 具有共轭结构的分子导线是构筑分子电子器件的重要组成单元,而含有二茂铁单元的该类化合物具有良好的电化学性质,被广泛研究。基于此,本实验通过Sonogashira交叉偶联等反应合成了一种新型二茂铁乙炔衍生物(FcNH2),并经红外(IR)、核磁共振(1H NMR和13C NMR)、质谱(MS)和循环伏安(CV)等方法表征。利用FcNH2与石墨烯壳聚糖(GHCS)之间的相互作用制备了GHCS/FcNH2复合物,并成功用于细胞色素c(Cytc)的固定,得到GHCS/FcNH2/Cytc修饰电极。研究表明,GHCS/FcNH2/Cytc/GCE在0.2 V附近出现一对峰,对应于Cytc的可逆氧化还原峰。此电极对NaNO2有良好的电催化作用,在1×107~1.5×104 mol/L范围内,NaNO2浓度与氧化峰电流呈良好的线性关系,检测限低至4×108 mol/L。此修饰电极不但可以实现细胞色素c的直接电化学,也可以用于定量检测NaNO2。
关键词 二茂铁乙炔衍生物; 细胞色素c; 石墨烯; 亚硝酸盐; 电催化
1 引 言
亚硝酸盐是一种工业用盐,同时也是食品添加剂[1],起着色、防腐作用,广泛用于熟肉类、灌肠类和罐头等动物性食品中,但用量受到严格限制。亚硝酸盐可以与胺类物质形成致癌物亚硝胺[2]。摄入过量的亚硝酸盐可使血液中的低铁血红蛋白氧化成高铁血红蛋白,失去运输氧的能力而引起组织缺氧性损害。由于亚硝酸盐潜在的危害,定量分析亚硝酸盐尤为重要。目前,定量检测亚硝酸盐的方法主要有电化学传感法[3]、质谱法[4]、光谱法[2,5]、色谱法[6]、比色法[7]等。电化学方法简单、廉价、分析迅速、检测灵敏度和选择性高,是相对简单有效的方法之一。最近,许多研究者成功构建了不同的化学修饰电极,用于亚硝酸盐的高灵敏传感检测[8,9],但是发展更可靠、更灵敏的分析检测亚硝酸盐的电化学传感器,仍然是近期亚硝酸盐研究的热点之一。
由于NO2在裸电极表面直接发生还原或氧化的电位很高,干扰物多[10],因此,电化学检测亚硝酸盐的关键是降低亚硝酸盐氧化还原的过电位,通常认为采用某些无机、有机或者有机金属化合物(如铁卟啉和酞花菁[11]等)修饰电极可以实现。二茂铁及其衍生物是常用的小分子电子媒介体,热稳定性好,电化学活性高,常用于构建高灵敏的化学/生物传感器。但该类传感器中的电子媒介体会发生部分溶解或扩散而离开电极表面导致媒介体流失,从而影响传感器的稳定性和使用寿命。因此,如何将二茂铁改性以获得结构特殊的衍生物并固定于电极表面,且保持其活性和稳定性,是研究者极其关注的问题。
石墨烯(GH)是由单层碳原子通过共价键结合而成的具有规则六方对称的理想二维晶体, 是继富勒烯(C60)和碳纳米管(CNT)之后的又一种碳质新材料,是构建其它维数碳质材料的基本结构单元[12]。由于石墨烯具有很大的共轭结构,可与共轭分子发生ππ堆积作用。如果将二茂铁与一个共轭结构相连,制备一种新型二茂铁衍生物,就可以实现二茂铁在石墨烯材料表面的有效固定。
在修饰电极上固定细胞色素c(Cytc)或血红素等,不但可实现它们与电极表面的电荷传输,同时也可用于电催化检测过氧化氢、超氧自由基阴离子[13]、抗坏血酸和L半胱氨酸[14]等。研究表明,采用电子媒介体有助于促进Cytc与电极表面的电子转移[15]。因此,使用一种新的电子媒介体,并采用有效的方法构建Cytc化学修饰电极,可以实现Cytc的直接电化学,同时可用于双重放大检测某些小分子。
基于此,本实验合成了一种氨基封端的二茂铁乙炔衍生物,结合石墨烯和二茂铁的优良性质,一锅法合成石墨烯二茂铁乙炔胺(GHCS/FcNH2)复合物,并构建一种新型亚硝酸盐传感器。此二茂铁衍生物含有苯乙炔单元、氨基和二茂铁等基团,其中的苯乙炔基和氨基可以与石墨烯非共价或共价键合形成稳定的复合物,从而将二茂铁电子媒介体固定在电极表面,不仅可以有效克服电子媒介体的泄漏,还可大大改善传感界面上的电子传递。Cytc可有效固定在该复合物表面,实现其直接氧化还原,同时,制备的传感器对NO 2具有良好的催化氧化效果,据此可建立定量检测亚硝酸盐的有效方法。
2 实验部分
2.1 仪器与试剂
UV2450型紫外分光光度计(UV,日本岛津公司)、Nicolet 670 红外光谱仪(IR,美国Nicolet公司)、F4500型荧光光谱仪(FL,日本日立公司)、Bruker500型高分辨核磁共振谱仪(CDCl3为溶剂,TMS为内标)、Nicolet 670傅立叶变换红外光谱仪(KBr压片,美国尼高力公司)、扫描电子显微镜(Quanta200,美国FEI公司)、Hitachi600透射电子显微镜(TEM,日本Hitachi公司)。CHI 660C电化学工作站(上海CHI公司),采用三电极系统:修饰的玻碳电极、碳棒电极和饱和甘汞电极分别作为工作电极、对电极和参比电极。玻碳电极使用前先用金相砂纸抛光,再依次用1.0, 0.3和0.05 μm的A12O3悬浊液在麂皮上抛光,最后分别用HNO3 (1∶1, V/V)、无水乙醇和二次蒸馏水超声清洗,然后置于室温下干燥备用。
壳聚糖(美国Sigma公司),用醋酸溶解,配制成0.5%(w/w)水溶液; Cytc (分析纯,美国Sigma公司);亚硝酸钠(分析纯,北京化学试剂有限公司); 四氢呋喃、二异丙胺使用前均用钠回流重蒸,进行无水处理。其它试剂均为分析纯,未经任何处理直接使用。二茂铁衍生物(FcNH2)和石墨烯均自行合成,具体合成步骤见文献[16]。0.1 mol/L pH 7.0的 PBS(0.1 mol/L NaH2PO4 + 0.1 mol/L Na2HPO4)用超纯水(经美国Milli Q 纯水仪处理)配制。
2.2 实验步骤
2.2.1 石墨烯及FcNH2的合成与表征 石墨烯氧化物由天然石墨片合成,具体步骤参见文献[17]。主要合成步骤如下: 取500 mg天然石墨片与20 mL浓H2SO4混合, 不断搅拌下,在15 min内加入1.75 g KMnO4。将混合物加热至35 ℃,继续搅拌2 h。冰浴冷却反应液至3~4 ℃,缓慢加入23 mL去离子水,在冰水浴中搅拌反应。由温度计监控冰水浴的温度,确保温度低于7 ℃。待温度稳定后, 继续加入270 mL水稀释反应液。反应液以300 r/min搅拌,逐滴加入H2O2溶液除去多余的KMnO4。将反应液过滤,用10% HCl溶液洗涤,在空气中干燥后,再真空室温干燥24 h。水洗,并用0.2 μm的微孔尼龙网过滤后,部分还原的石墨烯氧化物再分散于75 g水中,超声。将2 g水合肼溶于5 g水中,再加入到石墨烯氧化物的水溶液中,反应混合液保持100 ℃,并不断搅拌,持续反应24 h。过滤,充分水洗,得石墨烯(GH)。其结构和组成经红外、紫外、透射电子显微镜等表征[16]。
FcNH2的合成如图1所示:氮气保护下,在100 mL的单口烧瓶中依次加入126 mg (6×104 mol/L)二茂铁乙炔(实验室合成)[16]、131 mg (6×104 mol/L) 对碘苯胺(参考文献[18]合成)、21 mg Pd (PPh3)2Cl2、 6 mg CuI,再加入24 mL THF和8 mL二异丙胺,搅拌溶解,于55 ℃加热回流反应20 h,薄层色谱跟踪反应进程,旋转蒸发除去溶剂,残余物用30 mL二氯甲烷溶解,水洗,无水硫酸钠干燥,硅胶柱层析分离纯化(石油醚为洗脱剂)得153.5 mg 褐色固体,产率85%;1H NMR (CDCl3, 500 MHz) δ: 4.23 (s, 2H), 4.25 (s, 5H), 4.50 (s, 2H), 6.55(s, 2H), 7.39 (d, 2H, J=8.5 Hz), 7.60 (d, 2H, J=8.5 Hz); 13C NMR (CDCl3, 126 MHz) δ: 68.53, 69.91, 70.17, 71.22, 85.93, 86.44, 112.65, 114.96, 132.75, 146.77; IR (cm 1): 3440, 3358, 2924, 2853, 2197, 1701, 1622, 1604, 1519, 1408, 1289, 1102,1027, 823;MS m/z: 301(M+, 100%)。 将产物溶于乙腈,加入高氯酸锂作为电解质,将玻碳电极置于其中,在0.4 V附近有一对可逆的氧化还原峰,对应于二茂铁的氧化还原[16]。
2.2.2 修饰电极的制备、表征与应用研究
将片状壳聚糖用醋酸溶液搅拌溶解,调至pH 5.0,配成0.5%(w/w)的CS溶液,备用。将1 mg GH溶于1 mL上述CS溶液中,配成1 mg/mL的石墨烯溶液。用乙醇溶解FcNH2,配成1×10 3 mol/L溶液。取适量FcNH2溶液与石墨烯溶液,超声混合10 min,振荡过夜,以使石墨烯和FcNH2充分混匀,形成稳定的复合物。取适量复合物,加入Cytc的PBS溶液,振荡混合,搅拌过夜。取适量的混合液滴于干净的玻碳电极表面,自然风干,得GHCS/FcNH2/Cytc/GCE(具体见图1A),备用。为对比研究,同法制备了GHCS/Cytc/GCE和GHCS/FcNH2/GCE修饰电极。
TEM, UV和IR等用于考察石墨烯及其复合物的形貌。探讨不同的修饰电极在PBS中的循环伏安(CV)曲线以表征其电化学性质,并考察扫速的影响。在2×10 3 mol/L K3Fe(CN)6/K4Fe(CN)6中进行电化学阻抗测试,考察修饰电极的电子传递性能。CV法考察不同修饰电极对NaNO2的电化学响应;对NaNO2检测条件进行优化,并探讨最优条件下修饰电极对NaNO2检测的线性范围。计时安培实验在搅拌下进行,施加电压为700 mV。实际样品检测操作如下:将超市购买的葡萄汁饮料经直接过滤后,稀释10倍再采用标准加入法进行检测。所有测试电解质溶液实验前均通入高纯氮气除氧15 min。实验温度20 ℃。
3 结果与讨论
3.1 修饰电极的表征
图1A是修饰电极的制备过程。将GH先溶于CS溶液,再加入FcNH2,其与GH通过ππ堆积或者氢键作用等形成复合物。由TEM图(图1B)可知,石墨烯/FcNH2呈现清晰的片状结构,表明石墨烯可分散在二茂铁衍生物溶液中。
通过UV和FTIR光谱进一步确认GH与FcNH2复合物的形成,且排除壳聚糖的影响。由GH,FcNH2和GH/FcNH2的紫外光谱图(图2A)可知,石墨烯的紫外峰位于278 nm处,而FcNH2有两个紫外吸收峰,分别位于260和305 nm附近。对于GH/FcNH2纳米复合物,在270 nm附近出现一个紫外吸收峰。相对于石墨烯的特征吸收峰,复合物中石墨烯的峰强度有所增强,且发生一定的蓝移。这些现象可能是由于石墨烯与FcNH2发生ππ堆积作用形成了复合物所致。这也可以由红外光谱进一步证实。比较GH/FcNH2的红外光谱图与FcNH2和GH的红外光谱(图2B),复合物在2926, 1406,1082和810 cm 1处出现了二茂铁的特征峰,同时氨基和炔键的峰清晰可见,分别位于3430和2218 cm 1处。另外,复合物中FcNH2的炔键由2210 cm 1移至2218 cm 1,氨基的位置也发生移动,表明石墨烯和FcNH2发生了作用[16]。在1635及1117 cm 1处的GH峰分别移至1620和1082 cm 1处,也证明FcNH2与GH间的ππ堆积作用。
图3A是修饰电极在0.1 mol/L PBS(pH 7.0)中扫描的CV曲线。在0.7~0.3 V范围内,裸玻碳电极和GHCS/FcNH2/GCE上都没有任何氧化峰(若将电位范围扩大,在0.4 V附近会出现二茂铁的氧化峰),而GHCS/FcNH2/Cytc/GCE在0.2 V 附近有一对氧化还原峰,对应于细胞色素c的氧化还原。这说明GHCS/FcNH2可以作为Cytc的固定基底,同时有助于实现Cytc与电极之间的电子传递。值得注意的是,这里的GHCS不但可以增大电极的表面积,同时能为FcNH2的固定提供结合位点。另一方面,文献报道表明氨基可以与Cytc (pI 10)的赖氨酸残基进一步作用,稳定地固定在电极表面[10]。因此,GH/CS/FcNH2修饰电极可为Cytc提供更多的结合位点,从而固定更多Cytc分子,同时又可以实现Cytc的直接氧化还原。
图3B是在不同扫速下,GHCS/FcNH2/Cytc/GCE在0.1 mol/L PBS(pH 7.0)中扫描的CV曲线。随着扫速增加,氧化还原峰电流增大,同时峰电位也发生移动。在0.05~0.5 V/s内,峰电流与扫速成正比,表明固定在电极表面的 Cyt c 的氧化还原过程主要是表面控制过程。
由各种修饰电极在K3Fe(CN)6/K4Fe(CN)6中的Nyquist图(图4A)可知,裸玻碳电极的阻抗Ret约为90 Ω;而固定GHCS后,修饰电极的Ret迅速减小至15 Ω,这是由于GHCS良好的导电性使得电荷传输电阻减小,促进了电子传递。当修饰电极继续固定上FcNH2或者Cytc后,Ret都较GHCS修饰电极大,这是由于FcNH2是一种带有苯环的有机分子,其导电性不佳,从而在一定程度上影响电荷传输,而加入Cytc对电荷传输电阻影响很小。对于GHCS/FcNH2/Cytc/GCE,其Ret几乎为一条直线,也表明GHCS,FcNH2和Cytc都已成功固定于电极表面,且三者协同下有利于电荷传输。
3.2 修饰电极对NaNO2的催化氧化
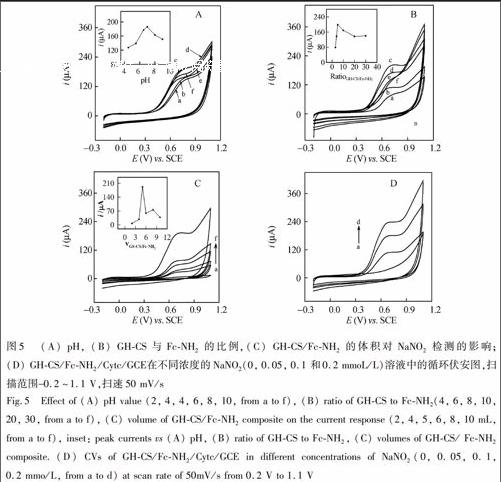
由图5可知,当pH=7(图5A),GH与FcNH2的质量比为5∶1(图5B),GHCS/FcNH2复合物的体积为5 μL(图5C)时,NaNO2的氧化峰电流最高。图5D是在最优化条件下,GHCS/FcNH2/Cytc修饰电极在不同浓度的NaNO2存在下的CV曲线。随着NaNO2浓度增加,氧化峰电流逐渐增大,表明此修饰电极可用于NaNO2的检测。计时安培法是常用于获得分析物检测线性范围的方法,因此对检测电位也进行了优化,发现当检测电位为0.7 V时,响应电流最大,因此计时安培法中采用电位为0.7 V。
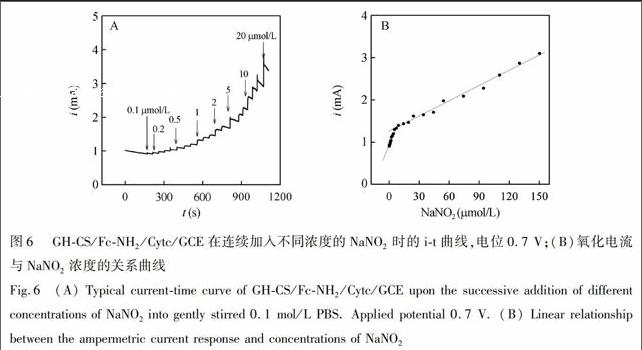
在最优条件下,在搅拌的PBS中不断加入如图6A所示浓度的NaNO2溶液时,修饰电极对NaNO2的响应非常快,且响应电流随浓度明显增大,在5s内基本达到稳态电流。在此条件下,得到的浓度校正曲线如图6B所示,由此可知,在检测条件下,可得到两条直线:当NaNO2浓度在0.1×10 6~5.2×10 6 mol/L和5.2×10 6~150 ×10 6 mol/L时,峰电流和浓度呈良好的线性关系,线性相关系数分别为0.992和0.996。传感器的检测范围达1×10 7~1.5×10 4 mol/L,根据3倍信噪比计算出检测限为4×10 8 mol/L, 比文献报道基于酶传感检测亚硝酸的传感器的检测限50 nmol/L[19]或100 nmol/L [20]更优。因此,该传感器有望用于实际样品中NaNO2的灵敏检测。
将制备的修饰电极用于实际样品中NaNO2的检测。实验中葡萄汁样品经过滤稀释与PBS溶液混合后采用标准加入法检测其中的NaNO2,结果见表1。回收率在99.1%~103.4%之间,3次测量的相对标准偏差小于3.8%,表明制备的修饰电极可以用于实际样品中NaNO2的检测。
综上所述,本实验利用设计合成的新型的二茂铁乙炔衍生物与石墨烯结合,制备稳定的纳米复合物(GHCS/FcNH2),该化合物成功作为Cytc的固定基底,不但固定了大量Cytc,同时可实现其与电极表面的直接电子传递。实验表明,GHCS/FcNH2/Cytc修饰电极对NaNO2有良好的电催化作用,检测线性范围宽,检测限低。制备的修饰电极简单,利用了二茂铁和Cytc对NaNO2的催化作用,二者的协同作用使电化学催化检测NaNO2的效果最优。因此,结合碳纳米材料与电子媒介体用于固定蛋白质或其它生物分子,有望用于其它电化学/生物传感领域的放大检测。
References
1 Cammack R, Joannou C L, Cui X, Martinez C, Maraj S R, Hughes M N. Biochim. Bioph. Acta, 1999, 1411: 475-488
2 Ximenes M I N, Rath S, Reyes F G R. Talanta, 2000, 51: 49-58
3 Cui L, Zhu J, Meng X, Yin H, Pan X, Ai S. Sensors and Actuators B, 2012, 161(1): 641-647
4 Pagliano E, Meija J, Mester Z. Anal. Chim. Acta, 2014, 824: 36-41
5 Dunham A J, Barkley R M, Sievers R E. Anal. Chem., 1995, 67(1): 220-224
6 Nilsson K F., Lundgren M, Agvald P, Adding L C, Linnarsson D, Gustafsson L E. Biochem. Pharmacol., 2011, 82(3): 248-259
7 Xiao N, Yu C. Anal. Chem., 2011, 82(9): 3659-3663
8 Qin C, Wang W, Chen C, Bu L, Wang T, Su X, Xie Q, Yao S. Sensors and Actuators B, 2013, 181: 375-381
9 Li X R, Kong F Y, Liu J, Liang T M, Xu J J, Chen H Y. Advanced Functional Material, 2012, 22: 1981-1986
10 Welch C M, Hyde M E, Banks C E, Compton R G. Anal. Sci., 2005, 21: 1421-1430
11 Cui L, Pu T, Liu Y, He X. Electrochim. Acta, 2013, 88: 559-564
12 Geim A K, Novoselov K S. Nature Material, 2007, 6: 183-191
13 Ding S, Wei W, Zhao G. Electrochem. Commun., 2007, 9: 2202-2206
14 Shie J, Yogeswaran U, Chen S. Talanta, 2008, 74: 1659-1669
15 Koh W C A, Rahman M A, Choe E S, Lee D K, Shim Y B. Biosens. Bioelectron., 2008, 23: 1374-1381
16 Liu M, Wang L, Deng J, Chen Q, Li Y, Zhang Y, Li H, Yao S. Analyst, 2012, 137(19): 4577-4583
17 Hummers W S, Offeman R E. J. Am. Chem. Soc., 1958, 80: 1339-1339
18 Dreyse P, Isaacs M, Calfumn K, Cceres C, Aliaga A, Aguirre M J, Villagra D. Electrochim. Acta, 2011, 56(14): 5230-5237
19 Serraa A S, Jorgea S R, Silveira C M, Mouraa J J G, Jubeteb E, Ochotecob E, Cabnerob G, Grandeb H, Almeidaa M G. Anal. Chim. Acta, 2011, 693: 41-46
20 Madasamy T, Pandiaraj M, Balamurugan M, Bhargava K, KumarSethy N, Karunakaran C. Biosens. Bioelectron., 2014, 52: 209-215
Abstract Highly conjugated linear molecular wires are one of the basic elements for constructing molecular electronic devices. Among these conjugated compounds, ferroceneterminated compounds as well as their derivatives have been widely studied because of their ideal electrochemical activity. Based on these, a new ferroceneterminated phenylethynyaniline (FcNH2) was synthesized by Sonogashira cross coupling reaction. The structure of the target compound was identified by infrared (IR), nuclear magnetic resonance (NMR), mass spectra (MS) and cyclic voltammetry (CV). Combined the graphenechitosan (GHCS) and FcNH2, a new composite of GHCS/FcNH2 was prepared and then used for immobilization of Cytc to prepare the GHCS/FcNH2/Cytc/GCE. It was found from the CV result that a pair of peaks near
0.2 V appeared which can be attributed to Cytc. The GHCS/FcNH2/Cytc modified GCE showed good catalysis towards NaNO2, and good linear relationship was found in the range of 1×10 7-1.5×10 4 mol/L,and the determination limit was bellow 4×10 8 mol/L. Therefore, cytochrome c (Cytc) can be immobilized on the GHCS/FcNH2 and the direct electron transfer can be realized between the electrode and solution and shows good prospect for detection of NaNO2.
Keywords Ferroceneterminated phenylethynyamine; Cytochrome C; Graphene, Sodium nitrite; Electrocatalysis
(Received 26 August 2014; accepted 25 December 2014)
This work was supported by the National Natural Science Foundation of China (Nos. 21305042, 21275051, 21375037), the Science and Technology Department of Hunan Province (Nos. 14JJ4030, 13JJ2020), and the Aid Program for Science and Technology Innovative Research Team in Higher Educational Institutions of Hunan Province. State Key Laboratory of Chemo/Biosensing and Chemometrics (2013013) and the Aid Program for Science and Technology Innovative Research Team in Higher Educational Institutions of Hunan Province.



摘 要 具有共轭结构的分子导线是构筑分子电子器件的重要组成单元,而含有二茂铁单元的该类化合物具有良好的电化学性质,被广泛研究。基于此,本实验通过Sonogashira交叉偶联等反应合成了一种新型二茂铁乙炔衍生物(FcNH2),并经红外(IR)、核磁共振(1H NMR和13C NMR)、质谱(MS)和循环伏安(CV)等方法表征。利用FcNH2与石墨烯壳聚糖(GHCS)之间的相互作用制备了GHCS/FcNH2复合物,并成功用于细胞色素c(Cytc)的固定,得到GHCS/FcNH2/Cytc修饰电极。研究表明,GHCS/FcNH2/Cytc/GCE在0.2 V附近出现一对峰,对应于Cytc的可逆氧化还原峰。此电极对NaNO2有良好的电催化作用,在1×107~1.5×104 mol/L范围内,NaNO2浓度与氧化峰电流呈良好的线性关系,检测限低至4×108 mol/L。此修饰电极不但可以实现细胞色素c的直接电化学,也可以用于定量检测NaNO2。
关键词 二茂铁乙炔衍生物; 细胞色素c; 石墨烯; 亚硝酸盐; 电催化
1 引 言
亚硝酸盐是一种工业用盐,同时也是食品添加剂[1],起着色、防腐作用,广泛用于熟肉类、灌肠类和罐头等动物性食品中,但用量受到严格限制。亚硝酸盐可以与胺类物质形成致癌物亚硝胺[2]。摄入过量的亚硝酸盐可使血液中的低铁血红蛋白氧化成高铁血红蛋白,失去运输氧的能力而引起组织缺氧性损害。由于亚硝酸盐潜在的危害,定量分析亚硝酸盐尤为重要。目前,定量检测亚硝酸盐的方法主要有电化学传感法[3]、质谱法[4]、光谱法[2,5]、色谱法[6]、比色法[7]等。电化学方法简单、廉价、分析迅速、检测灵敏度和选择性高,是相对简单有效的方法之一。最近,许多研究者成功构建了不同的化学修饰电极,用于亚硝酸盐的高灵敏传感检测[8,9],但是发展更可靠、更灵敏的分析检测亚硝酸盐的电化学传感器,仍然是近期亚硝酸盐研究的热点之一。
由于NO2在裸电极表面直接发生还原或氧化的电位很高,干扰物多[10],因此,电化学检测亚硝酸盐的关键是降低亚硝酸盐氧化还原的过电位,通常认为采用某些无机、有机或者有机金属化合物(如铁卟啉和酞花菁[11]等)修饰电极可以实现。二茂铁及其衍生物是常用的小分子电子媒介体,热稳定性好,电化学活性高,常用于构建高灵敏的化学/生物传感器。但该类传感器中的电子媒介体会发生部分溶解或扩散而离开电极表面导致媒介体流失,从而影响传感器的稳定性和使用寿命。因此,如何将二茂铁改性以获得结构特殊的衍生物并固定于电极表面,且保持其活性和稳定性,是研究者极其关注的问题。
石墨烯(GH)是由单层碳原子通过共价键结合而成的具有规则六方对称的理想二维晶体, 是继富勒烯(C60)和碳纳米管(CNT)之后的又一种碳质新材料,是构建其它维数碳质材料的基本结构单元[12]。由于石墨烯具有很大的共轭结构,可与共轭分子发生ππ堆积作用。如果将二茂铁与一个共轭结构相连,制备一种新型二茂铁衍生物,就可以实现二茂铁在石墨烯材料表面的有效固定。
在修饰电极上固定细胞色素c(Cytc)或血红素等,不但可实现它们与电极表面的电荷传输,同时也可用于电催化检测过氧化氢、超氧自由基阴离子[13]、抗坏血酸和L半胱氨酸[14]等。研究表明,采用电子媒介体有助于促进Cytc与电极表面的电子转移[15]。因此,使用一种新的电子媒介体,并采用有效的方法构建Cytc化学修饰电极,可以实现Cytc的直接电化学,同时可用于双重放大检测某些小分子。
基于此,本实验合成了一种氨基封端的二茂铁乙炔衍生物,结合石墨烯和二茂铁的优良性质,一锅法合成石墨烯二茂铁乙炔胺(GHCS/FcNH2)复合物,并构建一种新型亚硝酸盐传感器。此二茂铁衍生物含有苯乙炔单元、氨基和二茂铁等基团,其中的苯乙炔基和氨基可以与石墨烯非共价或共价键合形成稳定的复合物,从而将二茂铁电子媒介体固定在电极表面,不仅可以有效克服电子媒介体的泄漏,还可大大改善传感界面上的电子传递。Cytc可有效固定在该复合物表面,实现其直接氧化还原,同时,制备的传感器对NO 2具有良好的催化氧化效果,据此可建立定量检测亚硝酸盐的有效方法。
2 实验部分
2.1 仪器与试剂
UV2450型紫外分光光度计(UV,日本岛津公司)、Nicolet 670 红外光谱仪(IR,美国Nicolet公司)、F4500型荧光光谱仪(FL,日本日立公司)、Bruker500型高分辨核磁共振谱仪(CDCl3为溶剂,TMS为内标)、Nicolet 670傅立叶变换红外光谱仪(KBr压片,美国尼高力公司)、扫描电子显微镜(Quanta200,美国FEI公司)、Hitachi600透射电子显微镜(TEM,日本Hitachi公司)。CHI 660C电化学工作站(上海CHI公司),采用三电极系统:修饰的玻碳电极、碳棒电极和饱和甘汞电极分别作为工作电极、对电极和参比电极。玻碳电极使用前先用金相砂纸抛光,再依次用1.0, 0.3和0.05 μm的A12O3悬浊液在麂皮上抛光,最后分别用HNO3 (1∶1, V/V)、无水乙醇和二次蒸馏水超声清洗,然后置于室温下干燥备用。
壳聚糖(美国Sigma公司),用醋酸溶解,配制成0.5%(w/w)水溶液; Cytc (分析纯,美国Sigma公司);亚硝酸钠(分析纯,北京化学试剂有限公司); 四氢呋喃、二异丙胺使用前均用钠回流重蒸,进行无水处理。其它试剂均为分析纯,未经任何处理直接使用。二茂铁衍生物(FcNH2)和石墨烯均自行合成,具体合成步骤见文献[16]。0.1 mol/L pH 7.0的 PBS(0.1 mol/L NaH2PO4 + 0.1 mol/L Na2HPO4)用超纯水(经美国Milli Q 纯水仪处理)配制。
2.2 实验步骤
2.2.1 石墨烯及FcNH2的合成与表征 石墨烯氧化物由天然石墨片合成,具体步骤参见文献[17]。主要合成步骤如下: 取500 mg天然石墨片与20 mL浓H2SO4混合, 不断搅拌下,在15 min内加入1.75 g KMnO4。将混合物加热至35 ℃,继续搅拌2 h。冰浴冷却反应液至3~4 ℃,缓慢加入23 mL去离子水,在冰水浴中搅拌反应。由温度计监控冰水浴的温度,确保温度低于7 ℃。待温度稳定后, 继续加入270 mL水稀释反应液。反应液以300 r/min搅拌,逐滴加入H2O2溶液除去多余的KMnO4。将反应液过滤,用10% HCl溶液洗涤,在空气中干燥后,再真空室温干燥24 h。水洗,并用0.2 μm的微孔尼龙网过滤后,部分还原的石墨烯氧化物再分散于75 g水中,超声。将2 g水合肼溶于5 g水中,再加入到石墨烯氧化物的水溶液中,反应混合液保持100 ℃,并不断搅拌,持续反应24 h。过滤,充分水洗,得石墨烯(GH)。其结构和组成经红外、紫外、透射电子显微镜等表征[16]。
FcNH2的合成如图1所示:氮气保护下,在100 mL的单口烧瓶中依次加入126 mg (6×104 mol/L)二茂铁乙炔(实验室合成)[16]、131 mg (6×104 mol/L) 对碘苯胺(参考文献[18]合成)、21 mg Pd (PPh3)2Cl2、 6 mg CuI,再加入24 mL THF和8 mL二异丙胺,搅拌溶解,于55 ℃加热回流反应20 h,薄层色谱跟踪反应进程,旋转蒸发除去溶剂,残余物用30 mL二氯甲烷溶解,水洗,无水硫酸钠干燥,硅胶柱层析分离纯化(石油醚为洗脱剂)得153.5 mg 褐色固体,产率85%;1H NMR (CDCl3, 500 MHz) δ: 4.23 (s, 2H), 4.25 (s, 5H), 4.50 (s, 2H), 6.55(s, 2H), 7.39 (d, 2H, J=8.5 Hz), 7.60 (d, 2H, J=8.5 Hz); 13C NMR (CDCl3, 126 MHz) δ: 68.53, 69.91, 70.17, 71.22, 85.93, 86.44, 112.65, 114.96, 132.75, 146.77; IR (cm 1): 3440, 3358, 2924, 2853, 2197, 1701, 1622, 1604, 1519, 1408, 1289, 1102,1027, 823;MS m/z: 301(M+, 100%)。 将产物溶于乙腈,加入高氯酸锂作为电解质,将玻碳电极置于其中,在0.4 V附近有一对可逆的氧化还原峰,对应于二茂铁的氧化还原[16]。
2.2.2 修饰电极的制备、表征与应用研究
将片状壳聚糖用醋酸溶液搅拌溶解,调至pH 5.0,配成0.5%(w/w)的CS溶液,备用。将1 mg GH溶于1 mL上述CS溶液中,配成1 mg/mL的石墨烯溶液。用乙醇溶解FcNH2,配成1×10 3 mol/L溶液。取适量FcNH2溶液与石墨烯溶液,超声混合10 min,振荡过夜,以使石墨烯和FcNH2充分混匀,形成稳定的复合物。取适量复合物,加入Cytc的PBS溶液,振荡混合,搅拌过夜。取适量的混合液滴于干净的玻碳电极表面,自然风干,得GHCS/FcNH2/Cytc/GCE(具体见图1A),备用。为对比研究,同法制备了GHCS/Cytc/GCE和GHCS/FcNH2/GCE修饰电极。
TEM, UV和IR等用于考察石墨烯及其复合物的形貌。探讨不同的修饰电极在PBS中的循环伏安(CV)曲线以表征其电化学性质,并考察扫速的影响。在2×10 3 mol/L K3Fe(CN)6/K4Fe(CN)6中进行电化学阻抗测试,考察修饰电极的电子传递性能。CV法考察不同修饰电极对NaNO2的电化学响应;对NaNO2检测条件进行优化,并探讨最优条件下修饰电极对NaNO2检测的线性范围。计时安培实验在搅拌下进行,施加电压为700 mV。实际样品检测操作如下:将超市购买的葡萄汁饮料经直接过滤后,稀释10倍再采用标准加入法进行检测。所有测试电解质溶液实验前均通入高纯氮气除氧15 min。实验温度20 ℃。
3 结果与讨论
3.1 修饰电极的表征
图1A是修饰电极的制备过程。将GH先溶于CS溶液,再加入FcNH2,其与GH通过ππ堆积或者氢键作用等形成复合物。由TEM图(图1B)可知,石墨烯/FcNH2呈现清晰的片状结构,表明石墨烯可分散在二茂铁衍生物溶液中。
通过UV和FTIR光谱进一步确认GH与FcNH2复合物的形成,且排除壳聚糖的影响。由GH,FcNH2和GH/FcNH2的紫外光谱图(图2A)可知,石墨烯的紫外峰位于278 nm处,而FcNH2有两个紫外吸收峰,分别位于260和305 nm附近。对于GH/FcNH2纳米复合物,在270 nm附近出现一个紫外吸收峰。相对于石墨烯的特征吸收峰,复合物中石墨烯的峰强度有所增强,且发生一定的蓝移。这些现象可能是由于石墨烯与FcNH2发生ππ堆积作用形成了复合物所致。这也可以由红外光谱进一步证实。比较GH/FcNH2的红外光谱图与FcNH2和GH的红外光谱(图2B),复合物在2926, 1406,1082和810 cm 1处出现了二茂铁的特征峰,同时氨基和炔键的峰清晰可见,分别位于3430和2218 cm 1处。另外,复合物中FcNH2的炔键由2210 cm 1移至2218 cm 1,氨基的位置也发生移动,表明石墨烯和FcNH2发生了作用[16]。在1635及1117 cm 1处的GH峰分别移至1620和1082 cm 1处,也证明FcNH2与GH间的ππ堆积作用。
图3A是修饰电极在0.1 mol/L PBS(pH 7.0)中扫描的CV曲线。在0.7~0.3 V范围内,裸玻碳电极和GHCS/FcNH2/GCE上都没有任何氧化峰(若将电位范围扩大,在0.4 V附近会出现二茂铁的氧化峰),而GHCS/FcNH2/Cytc/GCE在0.2 V 附近有一对氧化还原峰,对应于细胞色素c的氧化还原。这说明GHCS/FcNH2可以作为Cytc的固定基底,同时有助于实现Cytc与电极之间的电子传递。值得注意的是,这里的GHCS不但可以增大电极的表面积,同时能为FcNH2的固定提供结合位点。另一方面,文献报道表明氨基可以与Cytc (pI 10)的赖氨酸残基进一步作用,稳定地固定在电极表面[10]。因此,GH/CS/FcNH2修饰电极可为Cytc提供更多的结合位点,从而固定更多Cytc分子,同时又可以实现Cytc的直接氧化还原。
图3B是在不同扫速下,GHCS/FcNH2/Cytc/GCE在0.1 mol/L PBS(pH 7.0)中扫描的CV曲线。随着扫速增加,氧化还原峰电流增大,同时峰电位也发生移动。在0.05~0.5 V/s内,峰电流与扫速成正比,表明固定在电极表面的 Cyt c 的氧化还原过程主要是表面控制过程。
由各种修饰电极在K3Fe(CN)6/K4Fe(CN)6中的Nyquist图(图4A)可知,裸玻碳电极的阻抗Ret约为90 Ω;而固定GHCS后,修饰电极的Ret迅速减小至15 Ω,这是由于GHCS良好的导电性使得电荷传输电阻减小,促进了电子传递。当修饰电极继续固定上FcNH2或者Cytc后,Ret都较GHCS修饰电极大,这是由于FcNH2是一种带有苯环的有机分子,其导电性不佳,从而在一定程度上影响电荷传输,而加入Cytc对电荷传输电阻影响很小。对于GHCS/FcNH2/Cytc/GCE,其Ret几乎为一条直线,也表明GHCS,FcNH2和Cytc都已成功固定于电极表面,且三者协同下有利于电荷传输。
3.2 修饰电极对NaNO2的催化氧化
由图5可知,当pH=7(图5A),GH与FcNH2的质量比为5∶1(图5B),GHCS/FcNH2复合物的体积为5 μL(图5C)时,NaNO2的氧化峰电流最高。图5D是在最优化条件下,GHCS/FcNH2/Cytc修饰电极在不同浓度的NaNO2存在下的CV曲线。随着NaNO2浓度增加,氧化峰电流逐渐增大,表明此修饰电极可用于NaNO2的检测。计时安培法是常用于获得分析物检测线性范围的方法,因此对检测电位也进行了优化,发现当检测电位为0.7 V时,响应电流最大,因此计时安培法中采用电位为0.7 V。
在最优条件下,在搅拌的PBS中不断加入如图6A所示浓度的NaNO2溶液时,修饰电极对NaNO2的响应非常快,且响应电流随浓度明显增大,在5s内基本达到稳态电流。在此条件下,得到的浓度校正曲线如图6B所示,由此可知,在检测条件下,可得到两条直线:当NaNO2浓度在0.1×10 6~5.2×10 6 mol/L和5.2×10 6~150 ×10 6 mol/L时,峰电流和浓度呈良好的线性关系,线性相关系数分别为0.992和0.996。传感器的检测范围达1×10 7~1.5×10 4 mol/L,根据3倍信噪比计算出检测限为4×10 8 mol/L, 比文献报道基于酶传感检测亚硝酸的传感器的检测限50 nmol/L[19]或100 nmol/L [20]更优。因此,该传感器有望用于实际样品中NaNO2的灵敏检测。
将制备的修饰电极用于实际样品中NaNO2的检测。实验中葡萄汁样品经过滤稀释与PBS溶液混合后采用标准加入法检测其中的NaNO2,结果见表1。回收率在99.1%~103.4%之间,3次测量的相对标准偏差小于3.8%,表明制备的修饰电极可以用于实际样品中NaNO2的检测。
综上所述,本实验利用设计合成的新型的二茂铁乙炔衍生物与石墨烯结合,制备稳定的纳米复合物(GHCS/FcNH2),该化合物成功作为Cytc的固定基底,不但固定了大量Cytc,同时可实现其与电极表面的直接电子传递。实验表明,GHCS/FcNH2/Cytc修饰电极对NaNO2有良好的电催化作用,检测线性范围宽,检测限低。制备的修饰电极简单,利用了二茂铁和Cytc对NaNO2的催化作用,二者的协同作用使电化学催化检测NaNO2的效果最优。因此,结合碳纳米材料与电子媒介体用于固定蛋白质或其它生物分子,有望用于其它电化学/生物传感领域的放大检测。
References
1 Cammack R, Joannou C L, Cui X, Martinez C, Maraj S R, Hughes M N. Biochim. Bioph. Acta, 1999, 1411: 475-488
2 Ximenes M I N, Rath S, Reyes F G R. Talanta, 2000, 51: 49-58
3 Cui L, Zhu J, Meng X, Yin H, Pan X, Ai S. Sensors and Actuators B, 2012, 161(1): 641-647
4 Pagliano E, Meija J, Mester Z. Anal. Chim. Acta, 2014, 824: 36-41
5 Dunham A J, Barkley R M, Sievers R E. Anal. Chem., 1995, 67(1): 220-224
6 Nilsson K F., Lundgren M, Agvald P, Adding L C, Linnarsson D, Gustafsson L E. Biochem. Pharmacol., 2011, 82(3): 248-259
7 Xiao N, Yu C. Anal. Chem., 2011, 82(9): 3659-3663
8 Qin C, Wang W, Chen C, Bu L, Wang T, Su X, Xie Q, Yao S. Sensors and Actuators B, 2013, 181: 375-381
9 Li X R, Kong F Y, Liu J, Liang T M, Xu J J, Chen H Y. Advanced Functional Material, 2012, 22: 1981-1986
10 Welch C M, Hyde M E, Banks C E, Compton R G. Anal. Sci., 2005, 21: 1421-1430
11 Cui L, Pu T, Liu Y, He X. Electrochim. Acta, 2013, 88: 559-564
12 Geim A K, Novoselov K S. Nature Material, 2007, 6: 183-191
13 Ding S, Wei W, Zhao G. Electrochem. Commun., 2007, 9: 2202-2206
14 Shie J, Yogeswaran U, Chen S. Talanta, 2008, 74: 1659-1669
15 Koh W C A, Rahman M A, Choe E S, Lee D K, Shim Y B. Biosens. Bioelectron., 2008, 23: 1374-1381
16 Liu M, Wang L, Deng J, Chen Q, Li Y, Zhang Y, Li H, Yao S. Analyst, 2012, 137(19): 4577-4583
17 Hummers W S, Offeman R E. J. Am. Chem. Soc., 1958, 80: 1339-1339
18 Dreyse P, Isaacs M, Calfumn K, Cceres C, Aliaga A, Aguirre M J, Villagra D. Electrochim. Acta, 2011, 56(14): 5230-5237
19 Serraa A S, Jorgea S R, Silveira C M, Mouraa J J G, Jubeteb E, Ochotecob E, Cabnerob G, Grandeb H, Almeidaa M G. Anal. Chim. Acta, 2011, 693: 41-46
20 Madasamy T, Pandiaraj M, Balamurugan M, Bhargava K, KumarSethy N, Karunakaran C. Biosens. Bioelectron., 2014, 52: 209-215
Abstract Highly conjugated linear molecular wires are one of the basic elements for constructing molecular electronic devices. Among these conjugated compounds, ferroceneterminated compounds as well as their derivatives have been widely studied because of their ideal electrochemical activity. Based on these, a new ferroceneterminated phenylethynyaniline (FcNH2) was synthesized by Sonogashira cross coupling reaction. The structure of the target compound was identified by infrared (IR), nuclear magnetic resonance (NMR), mass spectra (MS) and cyclic voltammetry (CV). Combined the graphenechitosan (GHCS) and FcNH2, a new composite of GHCS/FcNH2 was prepared and then used for immobilization of Cytc to prepare the GHCS/FcNH2/Cytc/GCE. It was found from the CV result that a pair of peaks near
0.2 V appeared which can be attributed to Cytc. The GHCS/FcNH2/Cytc modified GCE showed good catalysis towards NaNO2, and good linear relationship was found in the range of 1×10 7-1.5×10 4 mol/L,and the determination limit was bellow 4×10 8 mol/L. Therefore, cytochrome c (Cytc) can be immobilized on the GHCS/FcNH2 and the direct electron transfer can be realized between the electrode and solution and shows good prospect for detection of NaNO2.
Keywords Ferroceneterminated phenylethynyamine; Cytochrome C; Graphene, Sodium nitrite; Electrocatalysis
(Received 26 August 2014; accepted 25 December 2014)
This work was supported by the National Natural Science Foundation of China (Nos. 21305042, 21275051, 21375037), the Science and Technology Department of Hunan Province (Nos. 14JJ4030, 13JJ2020), and the Aid Program for Science and Technology Innovative Research Team in Higher Educational Institutions of Hunan Province. State Key Laboratory of Chemo/Biosensing and Chemometrics (2013013) and the Aid Program for Science and Technology Innovative Research Team in Higher Educational Institutions of Hunan Province.

