反向微乳毛细管电泳法在线富集技术灵敏检测化妆品中的多环芳烃
陈新+倪鑫炯+张佳瑜+刘瑛+曹玉华
摘 要 要建立了反向微乳毛细管电泳(MEEKC)在线富集技术灵敏检测多环芳烃的方法。采用大体积进样-pH动态连接-扫集微乳毛细管电泳法(LVSS-DypH-MEEKC)对于常规条件下很难分离的6种强亲脂性的多环芳烃中性分子进行富集分离。结果表明,在反相电压下,当微乳液的组成为: ?2.4% (w/w) SDS、0.6% (w/w)正辛烷、6.6% (w/w)正丁醇、20 mmol/L NaH2PO4 缓冲液(pH 2.2); 进HCB时间为20 s(16 kPa),进样时间为80 s(16 kPa)时,富集效果良好,富集倍数在25~80倍之间,在27 min内实现了对多环芳烃化合物的灵敏检测。将本方法用于化妆品中多环芳烃的检测,回收率在90.6%~95.9%之间,相对标准偏差均小于5.1%(n=5)。
关键词 微乳毛细管电泳; ?大体积进样; ?pH动态连接; ?扫集; ?多环芳烃(PAHs)
1 引 言
多环芳烃(PAHs)多为脂溶性高、疏水性强的中性分子,可诱发皮肤癌、阴囊癌和肺癌,是重要的环境和食品污染物。《化妆品卫生规范》[1]规定,苯并[g,h,i]芘、二苯并[a,h]蒽、苯并[a]芘、 苯并[b]荧蒽、苯并[a]蒽、荧蒽等多环芳烃化合物为化妆品中禁用物质。目前,PAHs的主要分析技术有高效液相色谱法(HPLC)[2~4]和气相色谱法(GC)[5~7]。有些PAHs不能用GC直接分析。而对于结构相似的PAHs,利用HPLC分析,灵敏度和分离度均较低。毛细管电泳方法具有仪器简单、操作方便、分离效率高、分析速度快、操作模式多等特点,越来越广泛地应用于各类样品的分析。目前已有一些利用胶束毛细管电泳(MEKC)[8,9]和填充毛细管色谱(CEC)[10]成功分离PAHs的报道。但是传统毛细管电泳方法的检测灵敏度较低,不能满足质量监控要求。在线富集技术仅通过对缓冲液组成和进样程序进行调控就可显著提高检测灵敏度,近年来成为毛细管电泳分析领域的研究热点[11,12]。在线富集技术大致可分为样品堆积技术[13]、扫集术[14]、等速电泳[15]等,其中堆积技术往往在进样时实现,可与后几种技术联用,进一步改善灵敏度。
大体积进样电堆积是常规电堆积模式的一种特殊形式,能有效克服常规堆积技术进样体积的限制,使检测灵敏度提高两个数量级以上[16]。在MEEKC方法中,样品与含有更高容量因子的微乳粒子的作用增强,浓缩程度增加,使检测灵敏度显著提高。本研究采用大体积进样、pH动态连接及扫集相联用的方式对PAHs进行富集分离,通过改变携带分析物前进的微乳粒子的迁移速度,在pH连接区带上产生堆积,不需要转变极性就可以实现大体积进样堆积,进而实现对PAHs的灵敏检测。本方法不仅可以用于多环芳烃的检测,而且为结构及性质较为相近的其它中性化合物的分离富集提供了参考。
2 实验部分
2.1 仪器与试剂
JA2003电子分析天平(上海分析天平仪器厂); CAPEL105高效毛细管电泳系统,配有Lumex紫外检测器(俄罗斯),反向电压0~30 kV,可调; HS3120D超声波振荡器(天津恒奥科技发展公司); 未涂层石英毛细管(65 cm×75 SymbolmA@ m ,有效长度50 cm); 未涂层石英毛细管(65 cm ×50 μm.i.d.,有效长度为55 cm, 河北永年光纤); 0.45 μm微孔滤膜(吉安市青原区庆丰过滤器材有限公司); 台式高速离心机(无锡市瑞江分析仪器有限公司)。
PAHs: 荧蒽,苯并[a]蒽,苯并[b]荧蒽,苯并[a]芘,二苯并[a,h]蒽,苯并[g,h,i]芘(德国DR公司); 其余试剂均为分析纯; 超纯水(华晶微电子公司)。
2.2 标准和样品的制备
标准溶液配制: 准确称取6个标准品,用二氯甲烷及乙醇溶解并定容至5 mL,配成2 g/L的贮备液,在 Symbolm@@ 18 ℃下避光保存。
样品溶液的制备: 准确称取2.00 g待测化妆品,加入10 mL正己烷-丙酮(1∶1, V/V)溶液,超声20 min后,利用高速离心机离心5 min,取上清液,在下层残渣中再加入10 mL正己烷-丙酮(1∶1, V/V)溶液,操作方法同上,重复提取3次,合并上清液; 膏霜类化妆品在上述步骤基础上再重复提取两次上层清液,合并上清液。将上清液放入冰箱内冷冻5 min; 冷冻后的提取液用0.45 SymbolmA@ m过滤膜过滤,并定容于50 mL容量瓶中。将滤液再用二氨甲烷液液萃取4次,每次10 mL,合并上层二氯甲烷相,浓缩至约2 mL。
2.3 微乳毛细管电动色谱条件
微乳液的组成为: 2.4% (w/w)SDS、0.6% (w/w)正辛烷、6.6% (w/w)正丁醇、20 mmol/L NaH2PO4 缓冲液(pH 2.2)。
高导缓冲液(HCB)组成为: 20 mmol/L NaH2PO4(pH 2.2)-乙腈(80∶20, V/V)。
样品基质为: 2.4% (w/w)SDS、0.6% (w/w)正辛烷、6.6% (w/w)正丁醇、0.2 mmol/L 硼砂缓冲液(pH 7.8)、20%乙腈。
紫外检测波长为280 nm,运行电压为 Symbolm@@ 20 kV,温度为20 ℃。
2.4 LVSS-DypH-sweep MEEKC运行模式
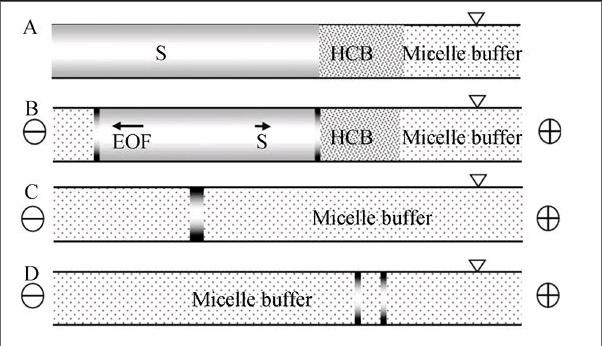
图1是LVSS-DypH-sweep的原理图。毛细管先用含有胶束的缓冲液冲洗,然后在毛细管中注入低pH值的高导缓冲液(HCB),用于收集大体积进样的样品(图1A); 样品溶在高pH值的样品基质中,分析物带负电荷并且向检测器方向迁移,在毛细管两端加了合适的电压后,电渗流(EOF)应指向进口端(如图1B),样品区和HCB区的接触界面附近产生一个pH动态连接区带,在电渗和电泳的合力下,低pH值HCB区带中的H+向负极方向(进口端)移动,与样品区带中的OH-发生中和作用,样品区带转变成低导区域,分析物速度增加; 快速移动的分析物从碱性样品区带分离,并且被酸性HCB区带质子化变成中性,迁移速度接近于零,在pH连接区带发生堆积产生富集效应。在毛细管两端换上胶束运行缓冲液,当胶束穿过样品区带时,样品在胶束相中分配富集,并被胶束带着向前运动。随着分离的进行,样品区带不断缩短,样品浓度不断浓缩,从而实现了二次富集(如图1C)。富集完成后,按照MEEKC方法分离(如图1D)。
3 结果与讨论
3.1 SDS浓度的影响
表面活性剂SDS浓度对形成微乳液的稳定性有重要影响。较低的表面活性剂浓度会减少分析时间,但同时也会降低界面张力,使得到的微乳体系不稳定。当SDS浓度低于2.4%时,在反向富集的过程中会出现破乳现象,堵塞毛细管; 当SDS浓度在2.4%~6.6%之间变化时,由图2可知,随着SDS浓度的增加,分析物的保留时间延长,分离度减弱。因此SDS的最佳浓度选择2.4%。
3.2 缓冲液pH值和浓度对分离的影响
当缓冲液的pH<3.0时,能够有效抑制电渗流。当缓冲液的在pH 1.8~3.0范围内变化时,pH值对各组分的分离度影响较小,但随着pH值增大,迁移时间延长。因此确定缓冲液的pH=2.2。固定缓冲液的pH=2.2,考察了NaH2PO4 的浓度对于分析结果的影响。当NaH2PO4的浓度在10~50 mmol/L 范围内时,缓冲液浓度的增加对PAHs分离度的影响较小,但分析时间延长。故本实验选用20 mmol/L NaH2PO4 缓冲液(pH 2.2)为运行液。
3.3 样品液基质组成及浓度
多环芳烃是强疏水性物质,基质需要采用脂溶性较强的溶液,为了让大体积进样的基质能排出毛细管,需要将基质调节成弱碱性,使电渗流方向指向入口端与样品适度分开。经过考察,采用2.4% (w/w)SDS-0.6% (w/w)正辛烷-6.6% (w/w)正丁醇-0.2 mmol/L 硼砂缓冲液(pH 7.8)-乙腈(80∶20, V/V)作为样品液基质。
3.4 进样时间和进HCB时间优化
动力学进样的灵敏度受到毛细管管长的制约,在动态pH连接扫集方法中,动力学进样的体积一般为管长的20%或22%[17]。实验考察了样品进样体积的限值(40~90 s/16 kPa),发现进样时间过长,会导致堆积效率降低、峰展宽。
实验表明,加入HCB区带能够克服峰展宽,堆积效率提高,当分析物进入到HCB区带中时,由于它的高导低场使分析物迁移速度降低,产生堆积效应。如图3所示,未加入HCB,峰形有所展宽,峰顶部出现平台峰; 而加入HCB后,峰形尖锐、灵敏度增加。
对HCB区带的长度和进样时间进行了优化。当进HCB区带的时间为20 s(16 kPa)时,进样的体积(80 s,16 kPa)可以达到管长的50%左右,并且获得了较高的检测灵敏度。
3.5 方法学考察
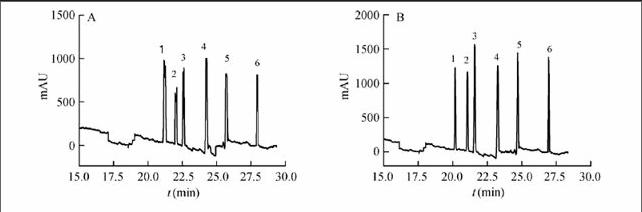
图4为6种PAHs的标准品的正向MEEKC电泳谱图,图3B为标准品的LVSS-DypH-sweep电泳谱图。
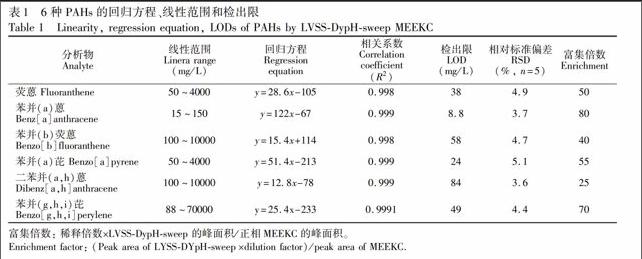
表明利用反向MEEKC法分离6种物质,分析时间变短、分离度增加,采用联用方式富集后的灵敏度明显提高。配制6种PAHs系列标准溶液,在最优化条件下进行分离分析,以峰面积(y)对样品浓度(x, mg/L)进行线性回归,以3倍信噪比(S/N=3)计算出6种分析物的检出限(LOD),见表1。
3.6 样品测定和回收率实验
选择了洗面奶、爽肤水、乳液、润肤霜、沐浴露、粉底液、洗发水、护发素等9种不同形态的市售及美容院专用化妆品,每种选择4个品牌,在优化条件下同时检测上述6种PAHs,均未检出分析物。考虑到样品基质对富集效果的影响,将样品溶液用二氯甲烷和微乳缓冲液稀释20倍后进行分析。将提取后的样品平行取2份,其中1份测定其本底值,另1份添加一定质量浓度的混合标准溶液,做回收实验,图5是某品牌化妆品乳液加标后的毛细管电泳富集谱图。重复5次的测定结果如表2所示。由结果可知,6种物质的回收率均在 90.6%~95.9%之间,其RSD均小于5.1%。
References
1 Hygienic Standard for Losmetics. Ministry of Health, People′s Republic of China. Beijing, 2007: 16
化妆品卫生规范. 北京: 中华人民共和国卫生部, 2007: 16
2 Demirci A. Polycyclic Aromatic Compounds, ?2014, 34(2): 115-134
3 MO Li-Gui, MA Sheng-Tao, LI Hui-Ru, YU Zhi-Qiang, SHENG Guo-Ying, FU Jia-Mo. Chinese J. Anal.Chem., 2013, ?41(12): 1825-1830
莫李桂, 马盛韬, 李会茹, 于志强, 盛国英, 傅家谟. 分析化学, 2013, ?41(12): 1825-183
4 Oluseyi T O, Olayinka K O, Adedapo E A. J. Chem. Soc. Nigeria., ?2013, 38(2): 43-47
5 YIN Yi, ZHENG Guang-Ming, ZHU Xin-Ping,MA Li-Sha, WU Shi-Hui, PAN De-Bo, Dai Xiao-Xin, XIE Wen-Ping. Journal of Instrumental Analysis, 2011, 30(10): 1107-1112
尹 怡, 郑光明, 朱新平, 马丽莎, 吴仕辉, 潘德博, 戴晓欣, 谢文平. 分析测试学报, 2011, 30(10): 1107-1112
6 WANG Li, JIN Fen, LI Min-Jie, LIU Yue. Chinese J. Anal. Chem., ?2013, 41(6): 869-875
王 丽, 金 芬, 李敏洁, 刘 玥. ?分析化学, 2013, 41(6): 869-875
7 Sun J, Qiao B, Sun D. Advanced Materials Research (Durnten-Zurich Switzerland), ?2014: 838-841
8 Rosario P M A, Nogueira J M F. Electrophoresis, ?2006, 27(23): 4694-4702
9 Alzola R, Pons B, Bravo D. Environ. Technol., ?2008, 29(11): 1219-1228
10 Qu Q S, Wang S, Mangelings D. Electrophoresis, ?2009, 30(6): 1071-1076
11 Chen J, Sun J Z, Liu S H. Anal. Lett., ?2013, 46(6): 887-899
12 Kukusamude C, Srijaranai S, Quirin J P. Electrophoresis, ?2014, 35(10):1478-1483
13 Quirino J P, Terabe S. Science, ?1998, 282 (5388): 465-468
14 Palmer J, Burgi D S, Munro N J, Landers J P. Anal. Chem., ?2001, 73 (4): 725-731
15 Britz-mckbbin P, Wong J, Chen D D Y. J. Chromatogr. A, ?1999, 853 (1-2): 535-540
16 Morales S, Cela, R. J. Chromatogr. A , ?1999, 846 (1-2) : 401-411
17 Yu L, Li S F. Electrophoresis, ?2005, 26(22): 4360-4367
On-line Preconcentration for Sensitive Analysis of PAHs in
Cosmetics by Reversed Microemulsion Electrokinetic Chromatography
CHEN Xin, NI Xing-Jiong, ZHANG Jia-Yu, LIU Ying, CAO Yu-Hua*
(School of Chemical and Material Engineering, the Ministry of Education Key Laboratory of Food Colloid and Technology,
Jiangnan University, Wuxi 214122, China)
Abstract A sensitive analytical method based on reversed microemulsion electrokinetic chromatography (MEEKC) combined with on-line preconcentration technique was developed for the determination of polycyclic aromatic hydrocarbons (PAHs) in cosmetics. For six lipophilic PAHs analytes which are difficult to be separated under conventional conditions, three stacking techniques including large volume sample stacking (LVSS), dynamic pH junction and sweeping (LVSS-DypH-sweep) were combined to realize the efficient preconcentration and separation. Under the optimum conditions, including the microemulsion buffer with the composition of 2.4%(w/w)SDS-0.6% (w/w) octane-6.6% (w/w)n-butyl alcohol-20 mmol/L NaH2PO4 (pH 2.2), HCB injection time of 20 s (16 kPa) and sample injection time of 80 s (16 kPa), good enrichment effect was reached with the enrichment factors ranged from 25 to 80, and the PAHs were analyzed successfully within 27 min. The developed method was used to analyze the PAHs in cosmetics. The recoveries ranged from 90.6% to 95.9%. The RSD values (n=5) were less than 5.1%.
Keywords Microemulsion electrokinetic chromatography; Large volume sample stacking; Dynamic pH junction; Sweeping; Polycyclic aromatic hydrocarbons
(Received 17 September 2014; accepted 16 October 2014)
This work was supported by the General Administration of Quality Supervision, Inspection and Quarantine of the People′s Republic of China(No.2010IK183)



摘 要 要建立了反向微乳毛细管电泳(MEEKC)在线富集技术灵敏检测多环芳烃的方法。采用大体积进样-pH动态连接-扫集微乳毛细管电泳法(LVSS-DypH-MEEKC)对于常规条件下很难分离的6种强亲脂性的多环芳烃中性分子进行富集分离。结果表明,在反相电压下,当微乳液的组成为: ?2.4% (w/w) SDS、0.6% (w/w)正辛烷、6.6% (w/w)正丁醇、20 mmol/L NaH2PO4 缓冲液(pH 2.2); 进HCB时间为20 s(16 kPa),进样时间为80 s(16 kPa)时,富集效果良好,富集倍数在25~80倍之间,在27 min内实现了对多环芳烃化合物的灵敏检测。将本方法用于化妆品中多环芳烃的检测,回收率在90.6%~95.9%之间,相对标准偏差均小于5.1%(n=5)。
关键词 微乳毛细管电泳; ?大体积进样; ?pH动态连接; ?扫集; ?多环芳烃(PAHs)
1 引 言
多环芳烃(PAHs)多为脂溶性高、疏水性强的中性分子,可诱发皮肤癌、阴囊癌和肺癌,是重要的环境和食品污染物。《化妆品卫生规范》[1]规定,苯并[g,h,i]芘、二苯并[a,h]蒽、苯并[a]芘、 苯并[b]荧蒽、苯并[a]蒽、荧蒽等多环芳烃化合物为化妆品中禁用物质。目前,PAHs的主要分析技术有高效液相色谱法(HPLC)[2~4]和气相色谱法(GC)[5~7]。有些PAHs不能用GC直接分析。而对于结构相似的PAHs,利用HPLC分析,灵敏度和分离度均较低。毛细管电泳方法具有仪器简单、操作方便、分离效率高、分析速度快、操作模式多等特点,越来越广泛地应用于各类样品的分析。目前已有一些利用胶束毛细管电泳(MEKC)[8,9]和填充毛细管色谱(CEC)[10]成功分离PAHs的报道。但是传统毛细管电泳方法的检测灵敏度较低,不能满足质量监控要求。在线富集技术仅通过对缓冲液组成和进样程序进行调控就可显著提高检测灵敏度,近年来成为毛细管电泳分析领域的研究热点[11,12]。在线富集技术大致可分为样品堆积技术[13]、扫集术[14]、等速电泳[15]等,其中堆积技术往往在进样时实现,可与后几种技术联用,进一步改善灵敏度。
大体积进样电堆积是常规电堆积模式的一种特殊形式,能有效克服常规堆积技术进样体积的限制,使检测灵敏度提高两个数量级以上[16]。在MEEKC方法中,样品与含有更高容量因子的微乳粒子的作用增强,浓缩程度增加,使检测灵敏度显著提高。本研究采用大体积进样、pH动态连接及扫集相联用的方式对PAHs进行富集分离,通过改变携带分析物前进的微乳粒子的迁移速度,在pH连接区带上产生堆积,不需要转变极性就可以实现大体积进样堆积,进而实现对PAHs的灵敏检测。本方法不仅可以用于多环芳烃的检测,而且为结构及性质较为相近的其它中性化合物的分离富集提供了参考。
2 实验部分
2.1 仪器与试剂
JA2003电子分析天平(上海分析天平仪器厂); CAPEL105高效毛细管电泳系统,配有Lumex紫外检测器(俄罗斯),反向电压0~30 kV,可调; HS3120D超声波振荡器(天津恒奥科技发展公司); 未涂层石英毛细管(65 cm×75 SymbolmA@ m ,有效长度50 cm); 未涂层石英毛细管(65 cm ×50 μm.i.d.,有效长度为55 cm, 河北永年光纤); 0.45 μm微孔滤膜(吉安市青原区庆丰过滤器材有限公司); 台式高速离心机(无锡市瑞江分析仪器有限公司)。
PAHs: 荧蒽,苯并[a]蒽,苯并[b]荧蒽,苯并[a]芘,二苯并[a,h]蒽,苯并[g,h,i]芘(德国DR公司); 其余试剂均为分析纯; 超纯水(华晶微电子公司)。
2.2 标准和样品的制备
标准溶液配制: 准确称取6个标准品,用二氯甲烷及乙醇溶解并定容至5 mL,配成2 g/L的贮备液,在 Symbolm@@ 18 ℃下避光保存。
样品溶液的制备: 准确称取2.00 g待测化妆品,加入10 mL正己烷-丙酮(1∶1, V/V)溶液,超声20 min后,利用高速离心机离心5 min,取上清液,在下层残渣中再加入10 mL正己烷-丙酮(1∶1, V/V)溶液,操作方法同上,重复提取3次,合并上清液; 膏霜类化妆品在上述步骤基础上再重复提取两次上层清液,合并上清液。将上清液放入冰箱内冷冻5 min; 冷冻后的提取液用0.45 SymbolmA@ m过滤膜过滤,并定容于50 mL容量瓶中。将滤液再用二氨甲烷液液萃取4次,每次10 mL,合并上层二氯甲烷相,浓缩至约2 mL。
2.3 微乳毛细管电动色谱条件
微乳液的组成为: 2.4% (w/w)SDS、0.6% (w/w)正辛烷、6.6% (w/w)正丁醇、20 mmol/L NaH2PO4 缓冲液(pH 2.2)。
高导缓冲液(HCB)组成为: 20 mmol/L NaH2PO4(pH 2.2)-乙腈(80∶20, V/V)。
样品基质为: 2.4% (w/w)SDS、0.6% (w/w)正辛烷、6.6% (w/w)正丁醇、0.2 mmol/L 硼砂缓冲液(pH 7.8)、20%乙腈。
紫外检测波长为280 nm,运行电压为 Symbolm@@ 20 kV,温度为20 ℃。
2.4 LVSS-DypH-sweep MEEKC运行模式
图1是LVSS-DypH-sweep的原理图。毛细管先用含有胶束的缓冲液冲洗,然后在毛细管中注入低pH值的高导缓冲液(HCB),用于收集大体积进样的样品(图1A); 样品溶在高pH值的样品基质中,分析物带负电荷并且向检测器方向迁移,在毛细管两端加了合适的电压后,电渗流(EOF)应指向进口端(如图1B),样品区和HCB区的接触界面附近产生一个pH动态连接区带,在电渗和电泳的合力下,低pH值HCB区带中的H+向负极方向(进口端)移动,与样品区带中的OH-发生中和作用,样品区带转变成低导区域,分析物速度增加; 快速移动的分析物从碱性样品区带分离,并且被酸性HCB区带质子化变成中性,迁移速度接近于零,在pH连接区带发生堆积产生富集效应。在毛细管两端换上胶束运行缓冲液,当胶束穿过样品区带时,样品在胶束相中分配富集,并被胶束带着向前运动。随着分离的进行,样品区带不断缩短,样品浓度不断浓缩,从而实现了二次富集(如图1C)。富集完成后,按照MEEKC方法分离(如图1D)。
3 结果与讨论
3.1 SDS浓度的影响
表面活性剂SDS浓度对形成微乳液的稳定性有重要影响。较低的表面活性剂浓度会减少分析时间,但同时也会降低界面张力,使得到的微乳体系不稳定。当SDS浓度低于2.4%时,在反向富集的过程中会出现破乳现象,堵塞毛细管; 当SDS浓度在2.4%~6.6%之间变化时,由图2可知,随着SDS浓度的增加,分析物的保留时间延长,分离度减弱。因此SDS的最佳浓度选择2.4%。
3.2 缓冲液pH值和浓度对分离的影响
当缓冲液的pH<3.0时,能够有效抑制电渗流。当缓冲液的在pH 1.8~3.0范围内变化时,pH值对各组分的分离度影响较小,但随着pH值增大,迁移时间延长。因此确定缓冲液的pH=2.2。固定缓冲液的pH=2.2,考察了NaH2PO4 的浓度对于分析结果的影响。当NaH2PO4的浓度在10~50 mmol/L 范围内时,缓冲液浓度的增加对PAHs分离度的影响较小,但分析时间延长。故本实验选用20 mmol/L NaH2PO4 缓冲液(pH 2.2)为运行液。
3.3 样品液基质组成及浓度
多环芳烃是强疏水性物质,基质需要采用脂溶性较强的溶液,为了让大体积进样的基质能排出毛细管,需要将基质调节成弱碱性,使电渗流方向指向入口端与样品适度分开。经过考察,采用2.4% (w/w)SDS-0.6% (w/w)正辛烷-6.6% (w/w)正丁醇-0.2 mmol/L 硼砂缓冲液(pH 7.8)-乙腈(80∶20, V/V)作为样品液基质。
3.4 进样时间和进HCB时间优化
动力学进样的灵敏度受到毛细管管长的制约,在动态pH连接扫集方法中,动力学进样的体积一般为管长的20%或22%[17]。实验考察了样品进样体积的限值(40~90 s/16 kPa),发现进样时间过长,会导致堆积效率降低、峰展宽。
实验表明,加入HCB区带能够克服峰展宽,堆积效率提高,当分析物进入到HCB区带中时,由于它的高导低场使分析物迁移速度降低,产生堆积效应。如图3所示,未加入HCB,峰形有所展宽,峰顶部出现平台峰; 而加入HCB后,峰形尖锐、灵敏度增加。
对HCB区带的长度和进样时间进行了优化。当进HCB区带的时间为20 s(16 kPa)时,进样的体积(80 s,16 kPa)可以达到管长的50%左右,并且获得了较高的检测灵敏度。
3.5 方法学考察
图4为6种PAHs的标准品的正向MEEKC电泳谱图,图3B为标准品的LVSS-DypH-sweep电泳谱图。
表明利用反向MEEKC法分离6种物质,分析时间变短、分离度增加,采用联用方式富集后的灵敏度明显提高。配制6种PAHs系列标准溶液,在最优化条件下进行分离分析,以峰面积(y)对样品浓度(x, mg/L)进行线性回归,以3倍信噪比(S/N=3)计算出6种分析物的检出限(LOD),见表1。
3.6 样品测定和回收率实验
选择了洗面奶、爽肤水、乳液、润肤霜、沐浴露、粉底液、洗发水、护发素等9种不同形态的市售及美容院专用化妆品,每种选择4个品牌,在优化条件下同时检测上述6种PAHs,均未检出分析物。考虑到样品基质对富集效果的影响,将样品溶液用二氯甲烷和微乳缓冲液稀释20倍后进行分析。将提取后的样品平行取2份,其中1份测定其本底值,另1份添加一定质量浓度的混合标准溶液,做回收实验,图5是某品牌化妆品乳液加标后的毛细管电泳富集谱图。重复5次的测定结果如表2所示。由结果可知,6种物质的回收率均在 90.6%~95.9%之间,其RSD均小于5.1%。
References
1 Hygienic Standard for Losmetics. Ministry of Health, People′s Republic of China. Beijing, 2007: 16
化妆品卫生规范. 北京: 中华人民共和国卫生部, 2007: 16
2 Demirci A. Polycyclic Aromatic Compounds, ?2014, 34(2): 115-134
3 MO Li-Gui, MA Sheng-Tao, LI Hui-Ru, YU Zhi-Qiang, SHENG Guo-Ying, FU Jia-Mo. Chinese J. Anal.Chem., 2013, ?41(12): 1825-1830
莫李桂, 马盛韬, 李会茹, 于志强, 盛国英, 傅家谟. 分析化学, 2013, ?41(12): 1825-183
4 Oluseyi T O, Olayinka K O, Adedapo E A. J. Chem. Soc. Nigeria., ?2013, 38(2): 43-47
5 YIN Yi, ZHENG Guang-Ming, ZHU Xin-Ping,MA Li-Sha, WU Shi-Hui, PAN De-Bo, Dai Xiao-Xin, XIE Wen-Ping. Journal of Instrumental Analysis, 2011, 30(10): 1107-1112
尹 怡, 郑光明, 朱新平, 马丽莎, 吴仕辉, 潘德博, 戴晓欣, 谢文平. 分析测试学报, 2011, 30(10): 1107-1112
6 WANG Li, JIN Fen, LI Min-Jie, LIU Yue. Chinese J. Anal. Chem., ?2013, 41(6): 869-875
王 丽, 金 芬, 李敏洁, 刘 玥. ?分析化学, 2013, 41(6): 869-875
7 Sun J, Qiao B, Sun D. Advanced Materials Research (Durnten-Zurich Switzerland), ?2014: 838-841
8 Rosario P M A, Nogueira J M F. Electrophoresis, ?2006, 27(23): 4694-4702
9 Alzola R, Pons B, Bravo D. Environ. Technol., ?2008, 29(11): 1219-1228
10 Qu Q S, Wang S, Mangelings D. Electrophoresis, ?2009, 30(6): 1071-1076
11 Chen J, Sun J Z, Liu S H. Anal. Lett., ?2013, 46(6): 887-899
12 Kukusamude C, Srijaranai S, Quirin J P. Electrophoresis, ?2014, 35(10):1478-1483
13 Quirino J P, Terabe S. Science, ?1998, 282 (5388): 465-468
14 Palmer J, Burgi D S, Munro N J, Landers J P. Anal. Chem., ?2001, 73 (4): 725-731
15 Britz-mckbbin P, Wong J, Chen D D Y. J. Chromatogr. A, ?1999, 853 (1-2): 535-540
16 Morales S, Cela, R. J. Chromatogr. A , ?1999, 846 (1-2) : 401-411
17 Yu L, Li S F. Electrophoresis, ?2005, 26(22): 4360-4367
On-line Preconcentration for Sensitive Analysis of PAHs in
Cosmetics by Reversed Microemulsion Electrokinetic Chromatography
CHEN Xin, NI Xing-Jiong, ZHANG Jia-Yu, LIU Ying, CAO Yu-Hua*
(School of Chemical and Material Engineering, the Ministry of Education Key Laboratory of Food Colloid and Technology,
Jiangnan University, Wuxi 214122, China)
Abstract A sensitive analytical method based on reversed microemulsion electrokinetic chromatography (MEEKC) combined with on-line preconcentration technique was developed for the determination of polycyclic aromatic hydrocarbons (PAHs) in cosmetics. For six lipophilic PAHs analytes which are difficult to be separated under conventional conditions, three stacking techniques including large volume sample stacking (LVSS), dynamic pH junction and sweeping (LVSS-DypH-sweep) were combined to realize the efficient preconcentration and separation. Under the optimum conditions, including the microemulsion buffer with the composition of 2.4%(w/w)SDS-0.6% (w/w) octane-6.6% (w/w)n-butyl alcohol-20 mmol/L NaH2PO4 (pH 2.2), HCB injection time of 20 s (16 kPa) and sample injection time of 80 s (16 kPa), good enrichment effect was reached with the enrichment factors ranged from 25 to 80, and the PAHs were analyzed successfully within 27 min. The developed method was used to analyze the PAHs in cosmetics. The recoveries ranged from 90.6% to 95.9%. The RSD values (n=5) were less than 5.1%.
Keywords Microemulsion electrokinetic chromatography; Large volume sample stacking; Dynamic pH junction; Sweeping; Polycyclic aromatic hydrocarbons
(Received 17 September 2014; accepted 16 October 2014)
This work was supported by the General Administration of Quality Supervision, Inspection and Quarantine of the People′s Republic of China(No.2010IK183)

