筆者于2015年10月30日~11月2日,参加了在福建省福州举行的第三届全国中小学实验教学说课活动,并荣获一等奖。
说课的课题是《补铁剂中铁的检测》。现对该探究实验课简要评析如下。
一、教学目标
知识与技能:了解检测补铁剂中铁的定性检验和定量测定的方法;培养学生滴定实验操作能力,并将定性实验和定量实验进行综合应用。
过程与方法:通过定性实验和定量实验的一般思路探究补铁剂中的铁,加深对科学探究一般过程的认识;通过检测补铁剂中的铁,提升学生实验方案设计、分析和评价的能力。
情感态度与价值观:使学生体会化学来源于生活,又服务于社会的思想;通过体验科学探究成功的喜悦,同时培养与他人交流合作的良好品质。
二、教学设计思路
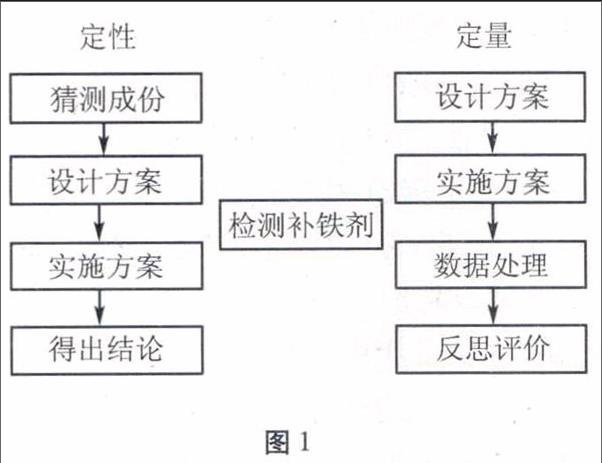
引导学生依据科学探究的八要素(提出问题、猜想假设、设计方案、进行实验、收集证据、解释与结论、反思评价、表达与交流)进行实验探究,检验方法——定性检验和定量检验相结合。实验设计如图1所示。
三、教学过程
环节l:情境引入
[教师](1)PPT出示我国目前患有缺铁性贫血人员众多的资料和数据(2)PPT展示图片:为了防治缺铁性贫血市售有多种补铁剂,如某品牌的乳酸亚铁口服液。
[学生]观看和体会。
[教师]“你能否运用所学知识来检测这盒补铁剂,你应该从哪些方面来检测呢?”
[学生]思考和讨论后,互相补充归纳得出——需要检测是否存在有效成分,以及有效成分含量是否达标。
[教师]检测是否存在有效成分需要采取定性检验,而检测有效成分含量是否达标需要采取定量测定,本节课就请同学们运用物质检测的方法——即定性研究和定量研究相结法合的方法检测该品牌的乳酸亚铁口服液是否合格。
设计意图:本环节联系生活实际创设情境,提出了具有探究价值的化学问题,激发了学生运用化学实验解决生活问题的热情,最重要的是引导学生得出物质检测的方法,也就是定性研究和定量研究相结合的学科方法,为下面的实验做好了方法的铺垫。
环节2:定性检验
(1)猜测成份
[教师]首先让学生阅读药品说明书。
[学生]知道了药品说明书中标识的有效成分是乳酸亚铁,观察口服液,却发现溶液为黄色。
[学生]对口服液中铁元素的价态进行了思考,并预测为以下三种情况:①补铁剂中铁元素可能是Fe2+;②补铁剂中铁元素可能是Fe3+;③补铁剂中铁元素可能Fe2+、Fe3+均有。
(2)设计方案
[教师]引导学生根据提供的仪器和药品,自主设计实验进行定性检验。
仪器和药品:试管(若干)、胶头滴管、补铁口服液、KSCN溶液、NaOH溶液、稀硝酸、酸性KMnO4溶液
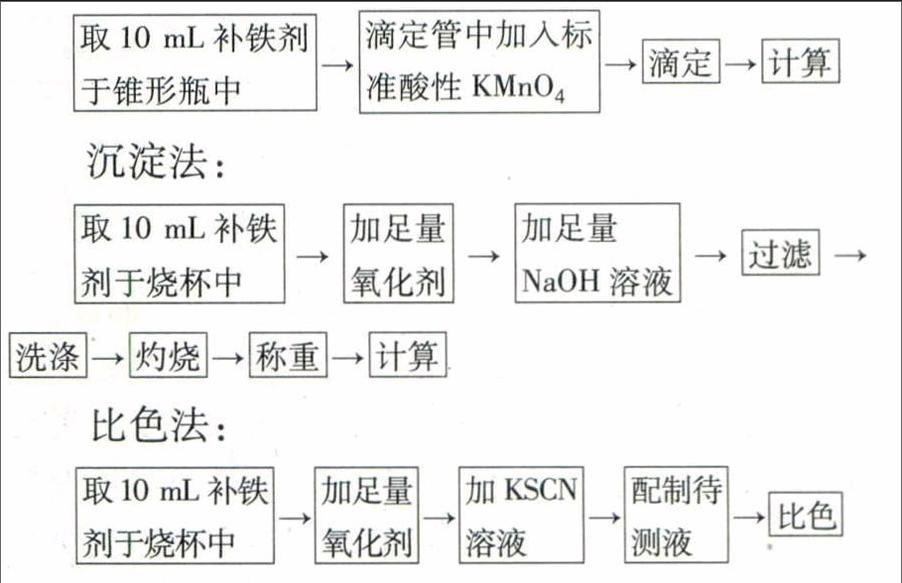
[学生]思考讨论后,主要设计了三种实验方案①酸性KMnO4氧化法(口服液+KMn4溶液);②KSCN特征反应法(口服液+KSCN溶液+稀硝酸);③NaOH沉淀法(口服液+NaOH溶液)。
(3)实施方案
[学生]分组实验,合作探究
(4)得出结论
[学生]甲同学汇报方案①中酸性KMn4溶液褪色,说明口服液中有Fe2+;乙同学汇报方案②中滴加KSCN溶液,口服液中没有变红,而继续滴加稀硝酸时口服液变为红色,说明口服液中只含有Fe2+。但丙同学在汇报方案③实验时,说有意外的发现:向补铁剂中滴加NaOH溶液,产生灰绿色沉淀,震荡后沉淀消失,最后溶液变为澄清。
[教师]针对方案③给予学生知识支持——Fe(OH)2在溶液中乳酸和氧气的作用下生成了Fe3+,Fe3+极易与乳酸根络合,因此看不到红褐色Fe(OH),沉淀。
[教师]“经过定性检验同学们得出补铁剂中含有的是乳酸亚铁,那么乳酸亚铁的含量是否和药品说明书中标识的一致呢?请同学们进入定量测定环节。”
设计意图:教师大胆地将实验放手给学生,学生调动《化学1(必修)》中所学Fe2+、Fe3+的知识,自主设计实验,进行定性检验,并如实地记录了实验现象,将观察和思维紧密结合,培养了学生分析问题、解决问题和动手实践的能力。
环节3:定量测定
(1)设计方案
[教师]出示资料卡片:
材料1.定量检测中常将待测量转变为某个可以测定的物理量如溶液的体积(滴定法)、沉淀的质量(沉淀法)、气体的质量或体积(气化法):
材料2.在一定条件下,有色溶液的颜色愈深,浓度愈大,故可以通过眼睛观察比较待测溶液与标准溶液颜色深浅来确定物质含量,此方法叫做目视比色法。如Fe3+中加入SCN生成较稳定的血红色物质,通过观察待测溶液与标准比色液的颜色深浅可确定待测液中的Fe3+浓度。
设计意图:由于学生缺乏定量测定的经验,对于如何检测一支补铁剂中铁元素的含量,学生遇到了思维瓶颈,此时教师出示资料卡片,帮助学生搭建思维平台。
[学生]阅读资料卡片,并提取有用信息。
[学生]独立思考,小组合作交流讨论。
[师生]共同归纳得出三种实验方案:
[师生]进行方案可行性评价,针对沉淀法,有同学指出从上面定性检验中知道了在乳酸存在下,会影响Fe(OH),沉淀产生,接着又有同学发言认为沉淀法步骤也太复杂了。而针对目视比色法,有同学指出目视比色法用眼睛观察误差比较大,而且还需要配置标准溶液操作起来也比较麻烦。最后,教师引导学生选择了简便易行的氧化还原滴定法。
设计意图:在定量测定方案设计环节,培养了学生利用资料获取有效信息的能力,提升了学生自主设计实验,分析、评价、选择实验方案的能力。
(2)实施方案
[师生]梳理滴定操作的实验步骤,分析决定实验成败的关键是滴定终点的判断。
[学生]实施方案——用已知浓度的酸性KMnO4溶液测定一支补铁剂中铁的含量。
(3)数据处理
[学生]按照方程式关系进行数据处理
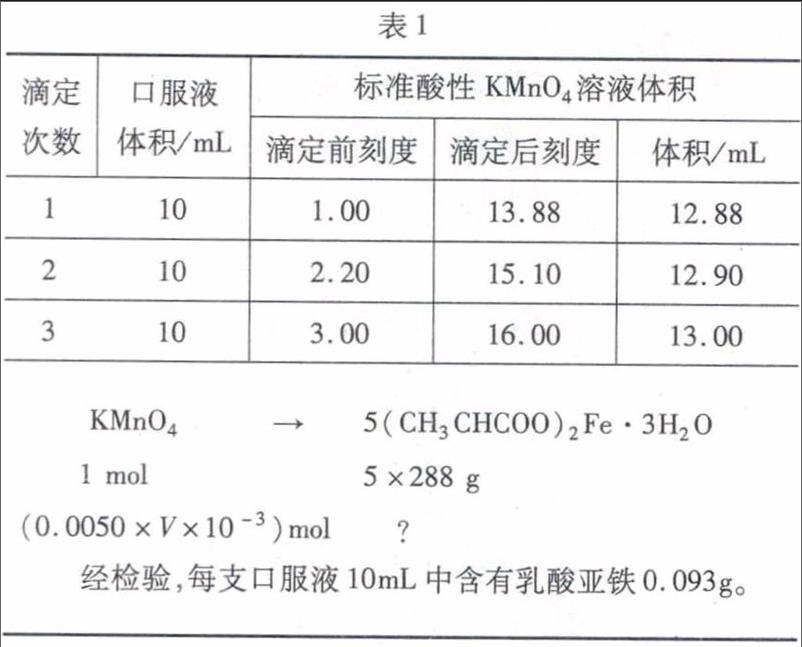
[教师]展示某小组实验报告(见表1)
[学生]将结果与药品说明书中的规格(10mL:0.1g)相对照,发现结果略于规格要求。
(4)反思评价
[教师]引导学生以全面观点看问题,并进行实验后反思。
[学生]进行误差分析,找出导致误差的可能原因:①少量口服液漏出;②滴定终点不宜观察;③口服液试剂瓶没进行洗涤;④俯视读数……。
设计意图:经过定量测定,实现了滴定法的迁移使用,丰富了学生对滴定法的认识。学生对物质的研究由定性上升到定量,发展了学生在物质检测领域的学科方法,提升了实验操作技能,培养了创新精神和实践能力。实验后进行反思,培养了学生严谨认真的科学态度。
[学生]有学生问:“老师,有没有新技术可以测口服液中铁元素含量?”
[教师]联系目视比色法,引出还可以用手持技术色度计测铁离子浓度,同时要求学生课下到探究实验室继续用手持技术测口服液中铁元素含量。
设计意图:向学生介绍现代化学的进展,以及所用到的先进手段,激发学生进行拓展探究的热情,进而拓宽了学生探究实验的视野。
环节4:总结提升
[教师]本节课你经历了怎样的科学探究过程?你建构了什么样的学科方法?你体验了什么样的学科价值?
[学生]归纳整理,感悟学科思想、方法,形成能力。
设计意图:通过总结,达到对本课的理论提升。
四、教学反思
1.设计该课题的意义和教学价值
设计本节课的目的,是为了落实《普通高中化学课程标准》提出的:“重视探究学习活动,发展学生的科学探究能力”的精神。其教学价值主要体现在以下几个方面。
(1)学科知识的建构价值
本课题建立在高中化学基本实验操作的基础上,通过本课题的研究,一方面可以让学生对Fe2+、Fe3+的检验方法进行巩固和应用;另一方面发展了高中阶段所学最重要的定量实验的潜在价值,即由酸碱中和滴定迁移到氧化还原滴定。
(2)学科方法的发展价值
通过本课题的研究,可以丰富学生对物质检测方法的认识,建构起定性研究和定量研究相结合的学科方法;可以引导学生親身经历和体验科学探究的过程,初步学会运用化学实验解决生产和生活中的问题,发展学生的化学实验观。
(3)学科认知的情感价值
本课题从生活中的补铁剂到化学上的常见反应,再到如何检测补铁剂,让学生充分体会化学来源于生活,又服务于社会的化学价值观。
(4)丰富教材内容的实用价值
本课题通过对“补铁剂”的定性实验,把已学的氧化还原反应有关概念如物质的氧化性、还原性、Fe2+与Fe3+的转化关系等,有机地联系起来;通过定量实验的测定,把酸碱中和滴定实验迁移到氧化还原滴定。这样的教学设计,丰富了教材联系实际的内容,拉近了理论与实际的距离,使学生感到化学就在我身边,学习化学更加亲切,体会到学习化学大有用途,对新知识的认识更加深刻。与此同时,还提高了学生的实验设计、科学探究、实验操作的能力和学以致用的能力。
2.教学效果
从教学效果看,不仅仅激发了学生的学习兴趣、锻炼了学生的实验操作技能、巩固提升了旧知,而且更重要的是引导学生体验了科学探究的过程,学习了如何运用化学知识分析和解决社会问题,体会了化学科学的社会发展价值,建构了化学的思想方法,发展和提高了学生的化学实验素养。
此外,为了防止将实验探究课上成表演课,教师还特别重视对课堂进行适当地引领,在整个探究过程中,都注重了让学生自主思考,小组之间的交流、讨论、总结,及时地发现和纠正学生实验中存在的问题,适时地引导学生展示思维的“火花”,收到了非常理想的教学效果。
- 农村生态旅游发展对策研究
- 建设嵊州越剧小镇所带来的启示
- 城镇主干路景观规划设计探析
- 棕榈科植物在华北地区的运用
- 红松母树林经营技术研究
- 浅析现代住宅小区绿化设计存在的问题及改进举措
- 论园林景观规划的主题与文化
- 促进人与自然和谐发展的节约型园林
- 金叶榆的嫁接技术和后期管理
- 滨河绿道景观设计探析
- 园林花卉苗木繁殖培育及栽培管理技术
- 提高桉树单产造林技术与管理措施
- 如何提高地表水水质监测质量
- 园林园艺施工技术要点与养护管理途径
- 对林业生态环境保护与林业经济建设的几点感悟
- 非市场失灵原因分析及对策研究
- 我国地方政府债务问题的现状及对策研究
- 互联网时代信息产品“免费”模式的应用分析
- 实施乡村振兴战略的重大意义及着力点
- 丝绸之路与“一带一路”的历史文化发展进程
- 科研机构主导型农业推广模式研究
- 实用菌栽培技术研究
- 探讨如何实现水稻优质高产高效生产技术
- 如何推广绿色农业种植技术的探讨
- 谷子提质增效综合措施
- physiognosy
- physiological
- physiologically
- physiologies
- physiologist
- physiologists
- physiologize
- physiology
- physiophilosophy
- physioplastic
- physio-psychologic
- physio-psychological
- physio-psychology
- physiotherapies
- physiotherapist
- physiotherapists
- physiotherapy
- physique
- physiqued
- physiques
- pi
- pianist
- pianiste
- pianists
- piano
- 顽尊
- 顽廉懦立
- 顽强
- 顽强勇敢
- 顽强地拼死战斗
- 顽强持久的精神,坚忍不拔的意志
- 顽强挣扎
- 顽强的意志、劲头
- 顽很
- 顽徒
- 顽心
- 顽念
- 顽忽
- 顽怠
- 顽恶
- 顽悍
- 顽悖
- 顽惫
- 顽惰暗情
- 顽愁
- 顽愎
- 顽意
- 顽愚
- 顽懦
- 顽戏