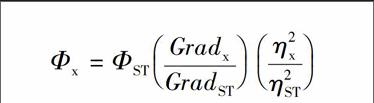
摘要 以绿色、简单、成本低的球磨方法制备的石墨烯为碳源,采用一步水热法成功制备了分散性好、尺寸分布均一、平均直径为(480 ± 020) nm、厚度为1~3层石墨烯烯量子点。分别采用高分辨透射电镜、原子力显微镜、傅里叶变换红外光谱、X射线光电子能谱、紫外可见吸收光谱、荧光光谱等对石墨烯量子点进行形貌、结构以及荧光性能的表征。 合成的石墨烯量子点可用于Fe3+的非标记、特异性检测,检测线性范围为20×10
ymbolm@@ 6~70×10
ymbolm@@ 4 mol/L,检出限为18×10
ymbolm@@ 6 mol/L(/N=3),同时对检测机理进行了推断,证明此石墨烯量子点用于自来水中Fe3+的检测的可行性;基于其低毒性和优良的生物相容性,所制备的石墨烯量子点可应用于细胞成像研究。本研究为碳纳米材料的制备提供了一种新途径,也为石墨烯量子点在生化分析、成像等方面的研究奠定了基础。
关键词 球磨法制备石墨烯; 一步水热法; 石墨烯量子点; 铁离子检测; 细胞成像
1引 言
石墨烯是由单层碳原子经sp2杂化紧密堆积而成的二维蜂窝状的碳质新材料,具有大比表面积、高载流子迁移率、优异的机械性能、良好的散热和化学稳定性及对环境友好等特征\[1~6\]。 石墨烯量子点作为石墨烯家族的新成员,尺寸一般在10 nm以下,除了具有石墨烯的优异性能外,还因其较小的尺寸而具有量子限制效应和边界效应,展现出一系列新的物理化学特性\[7~9\],包括良好的光学性质、极佳的水中分散性、易于功能化、较好的抗光漂白效果及尺寸和波长依赖的光致发光等,因此引起了研究者的广泛关注\[10~14\]。这些优点使得石墨烯量子点被广泛应用于生化传感、生物成像等各个领域\[11,15~18\]。如石墨烯量子点可与银纳米粒子复合进而应用于过氧化氢和葡萄糖的比色检测\[11\]。Ju等\[15\]将基于水合肼还原的水热法制备的石墨烯量子点应用于Fe3+的灵敏检测。尽管如此,寻找一种绿色环保、简单有效的石墨烯量子点的制备方法仍然是科研工作者追求的目标之一。
目前,石墨烯量子点的制备方法主要是采用超声法\[16\]、水热法\[8\]、离子束溅射法\[16\]、电化学法\[17~19\]等将大尺寸的石墨烯薄片,或者含有石墨烯结构的碳材料切割成10 nm左右的量子点\[20~22\]。这些方法步骤相对简单,但其中离子束溅射仪器设备复杂、成本高昂\[15\];而电化学方法需采用离子液体\[16\]等缓冲介质,这些缓冲介质附着在石墨烯量子点表面不易除去。 其次,采用NO3(65%)和 2O4(98%)处理氧化石墨烯的水相分散液,再以微波加热法将氧化石墨烯变为石墨烯量子点\[23\];在酸性条件下,用超声波方法也可将氧化石墨烯剥离为石墨烯量子点\[24\],但这些方法在制备过程中使用强酸性氧化剂,对实验操作人员和环境都造成潜在的危害。水热法是目前应用较为广泛的石墨烯量子点合成方法,一般借助长时间超声前处理促进石墨烯片的剥离。上述方法采用的前驱体一般是氧化还原法\[8,15,23,24\]或化学气相沉积(CVD)法\[16,17\]制备的石墨烯。氧化还原法由于使用强酸和水合肼等还原剂,会对环境造成污染\[8,15,23,24\];CVD技术需要使用氢气、甲烷等易燃易爆气体,而且程序比较复杂,仪器比较昂贵\[16,17,25\],均不适于大批量石墨烯量子点的制备和推广。因此,探索一种绿色环保、工艺简单、成本低廉、易于纯化的石墨烯量子点的制备方法迫在眉睫。球磨法是一种机械剥离技术,是石墨烯制备技术中低成本、 可大规模生产的技术之一。目前,湿式行星球磨法在石墨烯的制备中应用较为广泛,是将石墨分散在合适的溶剂中,这类溶剂具有足够的表面能,能克服石墨烯薄片之间的范德华力,如二甲基甲酰胺、N甲基吡咯烷酮、表面活性剂的水溶液(如十二烷基硫酸钠)等湿介质,施加于长时间的碾磨(30 h)和低速(300 r/min)旋转完成制备\[26,27\]。通过这些介质能够得到石墨烯,但剝离程度相对较低,而且一般还需要后期超声处理,同时这些溶剂属于有机溶剂和介质,有一定毒性。 同时,球磨介质由于高能量导致的分解,在球磨过程中球磨溶剂和介质的分解无法避免, 导致碎片化和缺陷, 从而引进的缺陷和杂质也不可控。所以选择合适湿介质,如干冰,一方面可被用于功能化石墨烯和提高剥离效率,另一方面可减小石墨烯尺寸,同时引进杂质可控\[28\]。利用基于干冰作为湿介质通过球磨技术制备的石墨烯, 还未见其作为前驱体制备石墨烯量子点的报道。
本研究采用球磨法制备的石墨烯作为前驱体,通过一步水热法制得荧光性质良好、粒径均匀、性能稳定的石墨烯量子点,相对于CVD技术及氧化石墨还原法得到的石墨烯作为前驱体,本方法具有绿色环保、工艺简单、成本低廉等优势。 分别采用高分辨透射电镜、原子力显微镜、傅里叶变换红外光谱、X射线光电子能谱、紫外可见吸收光谱、荧光光谱等对得到的石墨烯量子点进行了形貌、结构以及荧光性能的表征。所得到的石墨烯量子点分散性好, 尺寸分布均一, 平均直径为(480 ± 020) nm, 厚度为1~3层,其量子产率为102%。此外,制备的石墨烯量子点可用于Fe3+的特异性检测,检测线性范围为20×10
ymbolm@@ 6~70×10
ymbolm@@ 4 mol/L,检出限为18× 10
ymbolm@@ 6 mol/L(/N=3); 将制备的石墨烯量子点用于自来水中Fe3+的检测,结果令人满意。由于其低毒性和优良的生物相容性,所制备的石墨烯量子点被成功应用于细胞成像研究。
2实验部分
21仪器与试剂
FEIECNAI G2 高分辨透射电镜和原子力显微镜(德国 Bruker公司); 傅里叶变换红外光谱(美国热电集团); 紫外可见分光光度计(美国 PerkinElmer公司); 荧光分光光度计(澳大利亚Varian公司); X射线光电子能谱(英国VG cientific公司); C sp2荧光共聚焦显微镜(德国徕卡公司); ecan Infinite 200 Pro酶标仪(瑞士ecan公司)。
石墨、FeCl3、FeCl2、ZnCl2、CuCl2、MgO4、MnCl2、gCl2、PbCl2、AgNO3、AlCl3、Ni(NO3)2、Co(NO3)2及Cd(Ac)2(分析纯,山东莱阳经济和技术开发区化工厂);硫酸奎宁、二甲亚砜(DMO)及3(4,5二甲基噻唑2)2,5二苯基四氮唑溴盐(M)(分析纯,上海阿拉丁试剂有限公司)。实验用水为二次去离子水(18 MΩ·cm)。
22实验方法
221石墨烯量子点的制备参照文献\[28\]报道的球磨法制备的石墨烯方法并稍作改进。步骤如下:在球磨罐中放入400 g干冰和200 g碳粉,控制罐体内的气压,设置球磨时间48 h。实验得到的石墨烯颜色为深黑色。开罐取出石墨烯,加入Cl清洗除去产物中多余的铁杂质,水清洗3次,冷冻干燥得到固体产品,备用;对纯化后的石墨烯进行比表面积和透射电镜(EM)表征测试。
取0500 g球磨法制得的石墨烯分散于700 mL去离子水中,在冰浴中超声波(400 W)处理3 h, 将分散液倒入100 mL聚四氟乙烯反应釜中,在180℃下水热反应12 h;通过超声作用,可以将多层石墨烯变为少层石墨烯,有助于水热条件下石墨烯被切割成更小尺寸石墨烯量子点,提高量子产率。最后,将得到的黑色悬浮液10000 r/min离心5 min,取上清液,即得到无色的石墨烯量子点的分散液。
222Fe3+对石墨烯量子点荧光的影响石墨烯量子点用于Fe3+的检测, 荧光激发波长为300 nm,狭缝宽度为5 nm × 5 nm。
向200 mL石墨烯量子点分散液中分别加入500 μL不同浓度的Fe3+溶液,使溶液中Fe3+的終浓度分别为0、0002、001、004、006、008、010、014、018、022、026、032、040、050、060和070 mmol/L, 反应10 min,分别测定荧光强度。
223自来水中Fe3+的测定将不同浓度的Fe3+(0、100、200、300 和 400 μmol/L)分别加入到含有相同含量石墨烯量子点的自来水中,记录相应样品的荧光强度,绘制荧光强度减小值相对于加入Fe3+浓度的标准曲线,得到的上述标准曲线中X轴截距的绝对值即为自来水中Fe3+的浓度。每个实验重复测量3次。
224原子吸收光谱法测定自来水中Fe3+采用带有空心阴极灯(Cl)的原子吸收分光光度计测定Fe3+浓度。原子吸收光谱法的条件为:波长为2483 nm; Cl电流100 mA; 乙炔的流量为0500 L/min; 裂缝宽度为0200 nm
用Cl处理后,分别在自来水中加入不同浓度的Fe3+ (0、100、200、300 和 400 μmol/L)。在上述的分析条件下,通过原子吸收光谱法测定Fe3+标准品溶液, 绘制标准曲线法, 根据测定结果计算出自来水中Fe3+的浓度\[29\]。
225细胞成像和细胞毒性测试eLa细胞来源于上海细胞库,DMEM培养基加10%胎牛血清培养。将ela细胞用250%(w/w)胰酶消化后,将105个细胞分到玻璃底培养皿中培养。过夜后加入含100 μg/mL 石墨烯量子点的培养液,用上述培养基在37 ℃、5% CO2环境中孵育4 h。 弃去细胞培养液,加入100 μL 磷酸盐缓冲液清洗细胞, 重复3次。选择488 nm Ar离子激光器对孵育细胞进行激发, 激光扫描共聚焦显微镜采集获得图像。
石墨烯量子点的体外细胞毒性测试:将石墨烯量子点溶于新鲜的DMEM培养基,最终浓度分别为200、500、100、150、200和250 μg/mL,孵育; 另设对照组(用DMEM培养基孵育eLa细胞)和调零组(仅DMEM培养基),在37 ℃、5% CO2环境中孵育24 h。向各孔中加入100 μL M溶液,在上述条件中继续孵育4 h,再向各孔中加入100 μL二甲基亚砜溶液,在继续孵育10 min,用振荡器晃动10 min。用酶标仪测定各个孔在570 nm下的吸光度,未经过石墨烯量子点孵育的细胞活性设定为100%,计算各组细胞的相对活力。
226荧光量子产率(QY)的测定以硫酸奎宁为参照物测量石墨烯量子点的荧光量子产率\[30\],计算公式如下\[31\]:
其中,和X分别代表硫酸奎宁和量子点,Φ代表荧光量子产率,η代表溶剂的相对指数。
3结果与讨论
31石墨烯量子点的表征
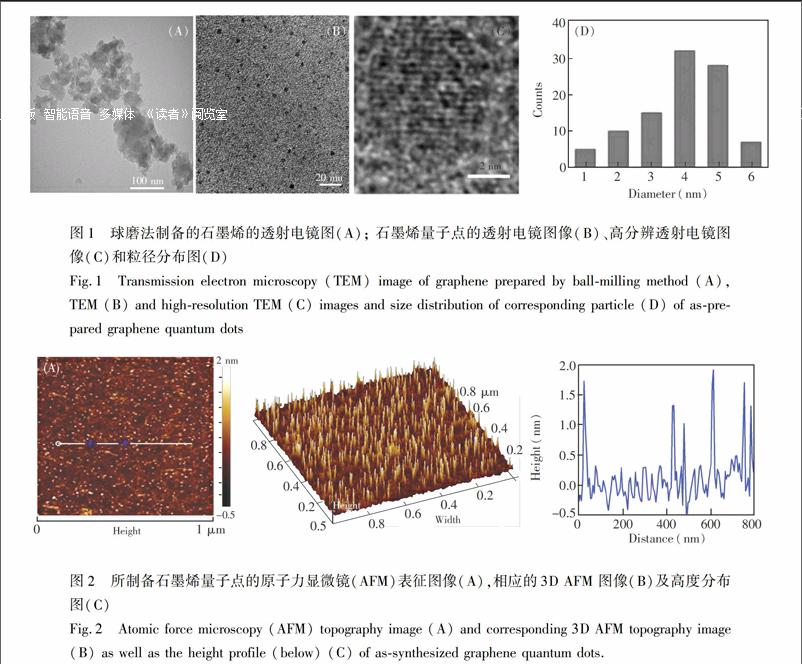
图1A为球磨法制备的石墨烯的透射电镜图,同时测得比表面积为568 m2/g\[32\]。 通过球磨方法对石墨粉进行充分剥离,所制备的石墨烯为层数较少的石墨烯纳米片,可以为石墨烯量子点的制备提供良好的石墨烯前驱体。图1B为石墨烯量子点的透射电镜图像,石墨烯量子点尺寸均一、分散性良好。图1C为石墨烯量子点的高分辨透射电镜图,可见石墨烯量子点的晶格结构,晶格间距为0210 nm,与文献\[33,34\]报道一致。图1D是石墨烯量子点的粒径分布图,其粒径范围为100~600 nm,平均尺寸为(480 ± 020) nm。
为进一步确认石墨烯量子点的层数、厚度及形貌特征,利用原子力显微镜测定的石墨烯量子点的形貌(图2)。从图2A可见,石墨烯量子点尺寸均一,均匀分散排布,这与透射电镜图的结果一致。图2B和2C分别是图2A的石墨烯量子点的高度分布图和分布曲线,可见大部分石墨烯量子点的高度为0300~200 nm,说明所合成的石墨烯量子点为1~3层石墨烯的厚度\[34\]。
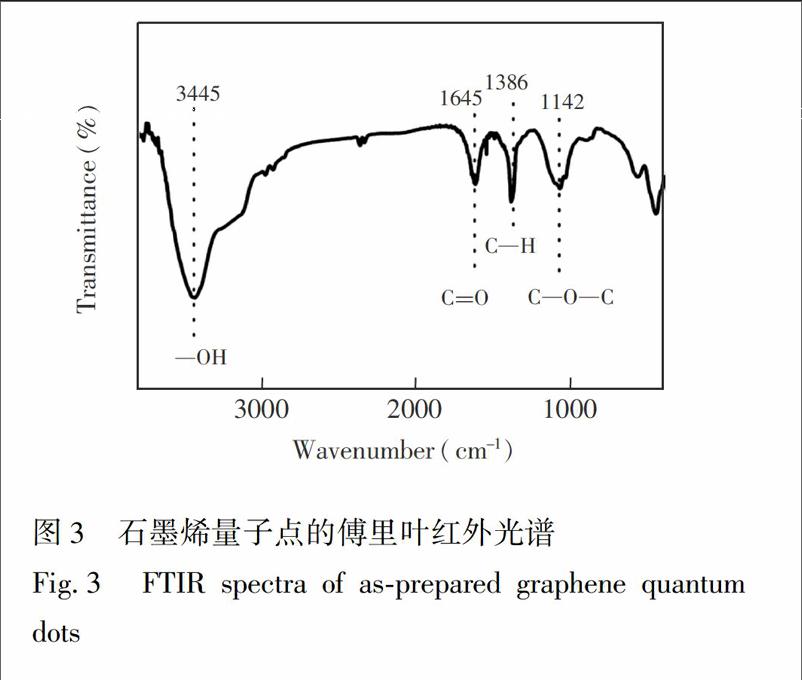
由石墨烯量子点的傅里叶红外光谱(图3)可见,石墨烯量子点表面含有丰富的含氧功能基团,其中3445 cm
ymbolm@@ 1处为O的伸缩振动峰,1645 cm
ymbolm@@ 1处为CO的伸缩振动峰,1386 cm
ymbolm@@ 1处为C键的弯曲振动峰,1142 cm
ymbolm@@ 1处为COC的伸缩振动峰\[35\]。
通过X射线光电子能谱(XP)对制备得到的石墨烯量子点的组成进行了分析。图4A是得到的石墨烯量子点的XP全谱图。结果表明,石墨烯量子点主要由C和O两种元素组成。图4B为石墨烯量子点的C1s XP谱图,石墨烯量子点在2845、2869和2893 eV处出现了3个明显的特征峰,分别对应的是sp2 CC、CO、CO\[3,36\]。XP的结果与FIR的结果相互验证,进一步证明了石墨烯量子点表面富氧功基能团的存在。正是由于含氧功能基团的存在,使得所制备的石墨烯量子点在水溶液介质中具有较好的分散性。
图5A为石墨烯量子点溶液的紫外吸收光谱和不同光源照射下的照片。日光照射下溶液呈无色,但在365 nm的紫外灯照射下,发出强烈的蓝色荧光。紫外可见吸收光谱表明,石墨烯量子点在285 nm处具有显著的吸收峰,此吸收峰与石墨烯量子点中含有的芳香烃结构引起的π→π跃迁有关,这种多环芳香烃结构表明石墨烯量子点保留了石墨烯原有的共轭结构\[37\]。图5B为石墨烯量子点的最大激发和最大发射光谱及其在不同激发波长下的荧光光谱。当激发波长从250 nm变到390 nm时,荧光发射峰强度随激发波长的增加呈先增加后减小的趋势。此外,石墨烯量子点的荧光发射峰发生红移,从310 nm增加至490 nm,表现出激发波长依赖的荧光特性,推测可能是与其粒径分布不均匀或表面存在不同的发射位点有关\[38,39\]。结合石墨烯量子点的激发谱和发射谱,可以确定其最大激发波长在300 nm处,在此激发波长下荧光发射最强,最大荧光发射峰波长为368 nm。因此,后续实验均在300 nm的激发光下测试相关石墨烯量子点的荧光光谱。
石墨烯量子点发光机理是由于量子效应和边缘效应。量子效应是由于其粒径小于激子波尔半径时,发生了能级分裂,导带和价带间的能级差进入可见光区,在受激发后发生电子跃迁,当激发态电子通过发射光子的方式返回基态时就会发光;边缘效应是由于石墨烯结构通常具有缺陷,这种缺陷赋予石墨烯量子点在激发波长的作用下发光\[40\]。以硫酸奎宁为参照物,测量石墨烯量子点的荧光量子产率为102%;文献\[41\]已报道的炭黑和硝酸的混合物得到的石墨烯量子点的荧光产率为404%,微波法等技术得到的石墨烯量子点的荧光产率为70%~100%\[42\],进一步证明了本方法合成石墨烯量子点具有优良的发光性能。
32石墨烯量子点的实际应用
321Fe3+的特异性检测石墨烯量子点作为荧光探针被广泛应用于金属离子的检测中。本研究首先考察了相同浓度(20×10
ymbolm@@ 4 mol/L)的不同金属离子(如Fe2+、Fe3+、g2+、Mg2+、Mn2+、Co2+、Ni2+、Ag+、Al3+、Cd2+、Cu2+、Pb2+、Zn2+)等对相同浓度的石墨烯量子点荧光强度的影响。对金属离子的测定需在中性或偏酸性的条件下进行,因为碱性条件下金属离子会发生水解。如图6A所示,Fe3+对石墨烯量子点的荧光强度有明显的淬灭作用,而其它金属离子对其荧光强度几乎没有影响,所以,制得的石墨烯量子点可用于对Fe3+的特异性检测。此外,在实验过程中,所选择金属盐的阴离子均为Cl
ymbolm@@ ,阴离子的影响可以作为背景扣除。另外,Fe3+与Cl
ymbolm@@ 之间不会产生配位络合作用,故Cl
ymbolm@@ 的影响可以忽略不计。 在石墨烯量子点分散液中逐次加入不同浓度的Fe3+溶液,反应10 min后测其荧光强度。如图6B所示,随着Fe3+浓度增加,石墨烯量子点的荧光强度逐渐下降。当Fe3+浓度达到70×10
ymbolm@@ 4mol/L时,石墨烯量子点的荧光基本淬灭。当Fe3+浓度范围分别为20×10
ymbolm@@ 6~60×10
ymbolm@@ 5 mol/L和80×10
ymbolm@@ 5~10×10
ymbolm@@ 4 mol/L时,体系的荧光强度变化值(ΔI=I0-Ii)与Fe3+浓度呈良好的线性关系(图6C),线性回归方程分别为ΔI=256C+2201 (R2=09358)及ΔI=102C+15991 (R2=09823), 检出限(LOD)为18×10
ymbolm@@ 6 mol/L (/N=3)。 因此,根据Fe3+对石墨烯量子点荧光强度的影响可以测定溶液中Fe3+的浓度。
金属离子淬灭石墨烯量子点荧光的机理,目前仍不明确。根据本研究结果, 推测是由于石墨烯量子点表面含有丰富的含氧功能基团,因而带有负电性,可以充当电子供体;当加入带正电的Fe3+后,Fe3+会充当电子受体,通过电荷转移作用改变了石墨烯量子点的电子态,从而引起荧光淬灭; 并且石墨烯量子点表面的-O与Fe3+之间有很强的结合力,会形成石墨烯量子点Fe络合物,引起石墨烯量子点聚集长大, 导致石墨烯量子点的荧光淬灭\[43,44\]。 此外,石墨烯量子点对Fe3+的特异性与Fe3+特有的顺磁性有关,但仍需实验和理论数据进一步验证。
通过标准加入法可将石墨烯量子点用于实际样品(如自来水)中Fe3+的检测(图6D),线性回归方程为ΔI=130C+240,相关系数R2=0987,通过计算可知自来水样品中Fe3+的浓度约为185 μmol/L,与用原子吸收光谱得到的结果接近(192×10
ymbolm@@ 6 mol/L)。结果表明,此方法用于检测自來水中Fe3+的浓度具有很好的准确性及灵敏度。为进一步地证明所建立方法的可靠性,在待测水样品中
分别加入20、50和100 μmol/L Fe3+标准溶液,研究结果如表1所示,相对标准偏差为25%~56%,回收率为954%~1073%。按照GB 57492006生活饮用水卫生标准,Fe3+限量水平为03 mg/L
322细胞成像量子点作为荧光探针,已被广泛用于生物成像研究中,石墨烯量子点由于其独特的荧光特性、低细胞毒性和高生物标记潜力等优点,在细胞、组织及活体等的生物成像研究中具有很大的优势。
本研究采用荧光共聚焦显微镜观察了石墨烯量子点对eLa细胞的成像效果。图7为石墨烯量子点在eLa细胞中培养4 h后的成像图,在488 nm玻长激发下, 细胞呈均匀明亮的绿色荧光,说明本研究制备的石墨烯量子点可以成功地被细胞吸收;由于其具有良好的光谱特性,可以作为荧光探针用于细胞成像。不同樣品浓度石墨烯量子点的体外细胞毒性测试见图7D,随着用于孵育细胞的石墨烯量子点浓度增加,细胞的活性逐渐降低(即死细胞数量增加),石墨烯量子点浓度在250 μg/mL时,细胞活性最低,但细胞存活率仍维持在85%以上,说明石墨烯量子点对细胞的毒性较低。上述结果表明, 石墨烯量子点具有良好的生物相容性和低毒性,可用于荧光生物成像。
4结 论
采用球磨法制备的石墨烯作为前驱体,通过一步水热法成功制备出了分散性良好、平均尺寸为(480 ± 020)nm的石墨烯量子点。本方法具有绿色环保、简单、成本低等优势。此外,石墨烯量子点的表面含有丰富的含氧功能基团,在紫外区有很强的吸收,并且表现出激发波长依赖的荧光性能。所制备的石墨烯量子点可用于Fe3+的特异性检测。基于其低毒性和优良的生物相容性,所制备的石墨烯量子点被成功应用于细胞成像研究。本研究为碳纳米材料的制备提供了一种新途径。
References
1Allen M J, ung V C, Kaner R B Chem Rev, 2009, 110(1): 132-145
2ang L A L, Lee W C, hi , Wong E Y L, adovoy A, Gorelik , obley J, Lim C , Loh K P mall, 2012, 8(3): 423-431
3ZANG Qian, ZANG Ling, LI Jingong Chinese J Anal Chem, 2013, 41(5): 641-649
张 谦, 张 玲, 李景虹 分析化学, 2013, 41(5): 641-649
4Choi W, Lahiri I, eelaboyina R, Kang Y Crit Rev olid tate, 2010, 35(1): 52-71
5MENG XianWen, ONG Xiao, LIU uQin, LIANG Ying Chinese Appl Chem, 2016, 33(12): 1441-144
孟献文, 宋 肖, 刘素芹, 梁 英 应用化学, 2016, 33(12): 1441-1447
6UANG aiPing, ZU JunJie Chinese J Anal Chem, 2011, 39(7): 963-971
黄海平, 朱俊杰 分析化学, 2011, 39(7): 963971
7Chua C K, ofer Z, imek P, Jankovsk O, Klímov K, Bakardjieva , Kucˇkov , Pumera M AC Nano, 2015, 9(3): 2548-2555
8Pan D, Zhang J, Li Z, Wu M Adv Mater, 2010, 22(6): 734-738
9Zhou X, Zhang Y, Wang C, Wu X, Yang Y, Zheng B, Wu , Guo , Zhang J AC Nano, 2012, 6(8): 6592-6599
10Li L, Wu G, Yang G, Peng J, Zhao J, Zhu J J Nanoscale, 2013, 5(10): 4015-4039
11XIA Chang, AI Xin, CEN huai, CEN XuWei, WANG Jianua Chinese J Anal Chem, 2016, 44(1): 41-48
夏 畅, 海 欣, 陈 帅, 陈旭伟, 王建华 分析化学, 2016, 44(1): 41-48
12ang L, Ji R, Cao X, Lin J, Jiang , Li X, eng K , Luk C M, Zeng , ao, J, Lau, P AC Nano, 2012, 6(6): 5102-5110
13Zhuo , hao M, Lee AC Nano, 2012, 6(2): 1059-1064
14Zhu , Zhang J, ang , Qiao C, Wang L, Wang , Liu X, Li B, Li Y, Yu W, Wang X, un , Yang B Adv Funct Mater, 2012, 22(22): 4732-4740
15Ju J, Chen W Biosens Bioelectron, 2014, 58: 219-225
16Zhu , Liu A, Xu Y, han F, Li A, Wang J, Yang W, Barrow C, Liu J Carbon, 2015, 88: 225-232
17Ananthanarayanan A, Wang X, Routh P, ana B, Lim , Kim D, Lim K, Li J, Chen P Adv Funct Mater, 2014, 24(20): 3021-3026
18Bao L, Zhang Z L, ian Z Q, Zhang L, Liu C, Lin Y, Qi B, Pang D Adv Mater, 2011, 23(48): 5801-5806
19Li Y, u Y, Zhao Y, hi G, Deng L, ou Y, Qu L Adv Mater, 2011, 23(6): 776-780
20Zhu , Zhang J, Qiao C, ang , Li Y, Yuan W, Li B, ian L, Liu F, u R, Gao , Wei , Zhang , un , Yang B Chem Commun, 2011, 47(24): 6858-6860
21Qu D, Zheng M, Du P, Zhou Y, Zhang L, Li D, an , Zhao Z, Xie Z, un Z Nanoscale, 2013, 5(24): 12272-12277
22Bacon M, Bradley J, Nann Part Part yst Char, 2014, 31(4): 415-428
23Chen , Liu J W, Chen M L, Chen X W, Wang J Chem Commun, 2012, 48: 7637-7639
24Li L L, Ji J, Fei R, Wang C Z, Lu Q, Zhang J R, Liang L P, Zhu J J Adv Funct Mater, 2012, 22(14): 2971-2979
25Xu Y, Liu J mall, 2016, 12(11): 1400-1419
26Zhao W, Fang M, Wu F, Wu , Wang L, Chen G J Mater Chem, 2010, 20(28): 5817-5819
27Jeon I Y, Choi J, Jung M, eo J M, Kim M J, Dai L, Baek J B J Am Chem oc, 2012, 135(4): 1386-1393
28Jeon I Y, hin Y R, ohn G J, Choi J, Bae Y, Mahmood J, eoa J M, Kim M J, Chang D W, Dai L, Baek J B P Natl Acad ci UA, 2012, 109(15): 5588-5593
29Yaman M, Kaya G Anal Chim Acta, 2005, 540(1): 77-81
30Liu , Ye , Mao C Angew Chem Int Edit, 2007, 46(34): 6473-6475
31Melhuish W J Phys Chem B, 1961, 65(2): 229-235
32Cui L, Xu Y, Niu L, Yang W, Liu J Nano Res, 2017, 10(2): 595-604
33Liu J, hao M, Chen X, Yu W, Liu X, Qian Y J Am Chem oc, 2003, 125(27): 8088-8089
34Kang Z, Wang E, Gao L, Lian , Jiang M, u C, Xu L J Am Chem oc, 2003, 125(45): 13652-13653
35Bao L, Zhang Z L, ian Z Q, Zhang L, Liu C, Lin Y, Qi B, Pang D Adv Mater, 2011, 23(48): 5801-5806
36Zhou C, Jiang W, Via B K Colloid urface B, 2014, 118(118): 72-76
37Xu Y, Wu M, Liu Y, Feng X Z, Yin X B, e X W, Zhang Y K Chem Eur J, 2013, 19(7): 2276-2283
38Ray C, aha A, Jana N R, arkar R J Phys Chem C, 2009, 113 (43): 18546-18551
39Wang Q, Zheng , Long Y, Zhang L, Gao M, Bai W Carbon, 2011, 49(9): 3134-3140
40Zhu , ong Y, Zhao X, hao J, Zhang J, Yang B Nano Res, 2015, 8(2): 355-381
41Dong Y, Chen C, Zheng X, Gao L, Cui Z, Yang , Guo C, Chi Y, Li C M J Mater Chem, 2012, 22(18): 8764-8766
42ang L, Ji R, Cao X, Lin J, Jiang , Lin J, Jiang , Li X, eng K , Chi M L, Zeng , ao J, Lau P AC Nano, 2012, 6(6): 5102-5110
43Zhang , Li J, Zeng M, Xu J, Wang X, u W Nanoscale, 2014, 6(8): 4157-4162
44Li Z X, Zhang L F, Zhao W Y, Li XY, Guo Y K, Yu M M, Liu J X Inorg Chem Commun, 2011, 14(10): 1656-1658
- 让科技照亮未来
- 启光科技
- 大学该为女性就业公平做什么
- 大数据解读真实基层公务员
- 美丽漯河 绘就生态新画卷
- 美丽中国:向污染宣战
- 新媒体时代下的传媒改革
- 中国唐文化对日本的影响
- 纪录片中的情感表达
- 情、智、胆,挥洒教育人生
- 让“师爱”润泽孩子们的生命
- 提升精气神 激发老牌名校的活力
- 优质 均衡 把教育办在百姓的心坎上
- 中原有个“泥人张”
- 晚清对外政策相关思想观念的嬗变
- 古代“中央巡视员”权力很大
- 算清为官的“机会成本”
- 以高水平政务微博微信助推国家治理体系与治理能力现代化
- 法律规范市场,引导低碳经济发展
- 郑州航空港经济综合实验区临空产业发展研究
- 建设郑州现代航空大都市的几点思考
- 河南新型城镇化进程中农村社区建设的问题研究
- 打好实战化练兵组合拳
- 荣誉视点:西方国家军人勋章奖章扫描
- 民权县公路局从细处着手践行群众路线
- workrage
- workrelated
- work-reˌlated
- workroom
- works
- worksampling
- work sampling
- work sb hard
- work sb out
- work sb/yourself up (into sth)
- workscouncil
- works council
- workshadowing
- work shadowing
- worksharing
- worksheet
- worksheets
- workshop
- workshops
- work-shy
- workshy
- worksimplification
- work simplification
- worksite
- works manager
- 招致忧患
- 招致怨恨
- 招致憎恨
- 招致憎恶
- 招致收揽
- 招致杀戮
- 招致某种情感
- 招致毁谤
- 招致生气
- 招致疑怪
- 招致盗匪
- 招致祸乱
- 招致祸害
- 招致祸患
- 招致福
- 招致罪祸
- 招致罪责
- 招致罪过
- 招致羞辱
- 招致讥讽
- 招致讥责
- 招致讪笑、非议
- 招致诉讼
- 招致责难
- 招致败亡