陈秀兰
摘要:Fe3+与SCN-的实际反应情况一直困扰着学生理解Fe(SCN)3在溶液中的存在形式,文章采用数字化传感技术,通过实验对比探究Fe3+与SCN-的络合。
关键词:数字实验;传感技术;Fe(SCN)3
文章编号:1008-0546(2016)10-0092-02 中图分类号:G633.8 文献标识码:B
doi:10.3969/j.issn.1008-0546.2016.10.033
一、 实验背景
苏教版《化学1》在“铁、铜及其化合物的应用”内容中,为三价铁离子的检验给出了信息提示[1]:在含有Fe3+的溶液中加入KSCN溶液,溶液变成血红色,而在含有Fe2+的溶液中加入KSCN溶液,溶液不变色。同时给出了反应的离子方程式。
结合离子反应发生的条件,学生自然而然会得出Fe(SCN)3属于弱电解质的结论,而作为知识补充,部分老师会告诉学生,Fe(SCN)3属于配位化合物。配位化合物和弱电解质就容易出现概念不明或混淆的问题,特别是给化学学习充满热情的学生造成困扰。结合苏教版选修内容“物质结构与性质”对于配位化合物的解释[2],既然由内界和外界构成的配位化合物在水中是完全电离的,那么将Fe(SCN)3理解为弱电解质显然存在问题。如何尽可能贴近学生的知识水平解释Fe(SCN)3在溶液中的存在?《化学1》给出的离子方程式是否能在照顾普通学生理解能力的基础上适当进行改动,以更加贴近科学事实?为探究实验过程中Fe3+与SCN-的实际反应情况,特设计以下实验。
二、 实验准备
0.1mol/L KSCN溶液,0.1mol/L KCl溶液,FeCl3固体,天平,50mL移液管,药匙,蒸馏水,滤纸,不同规格的烧杯若干,电脑,85-2控温式磁力搅拌器(带磁力搅拌转子),GQY数字实验室平台,不带屏数据采集器,电导率传感器
三、 实验装置
四、 实验过程
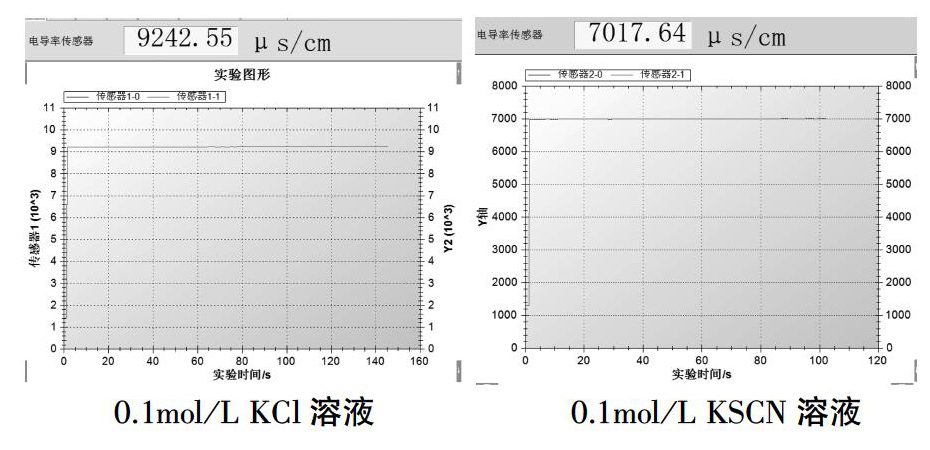
1. 分别取50mL0.1mol/L KSCN溶液和0.1mol/L KCl溶液于200mL烧杯中,用电导率传感器检测两份溶液的导电能力,得到结果如图所示:
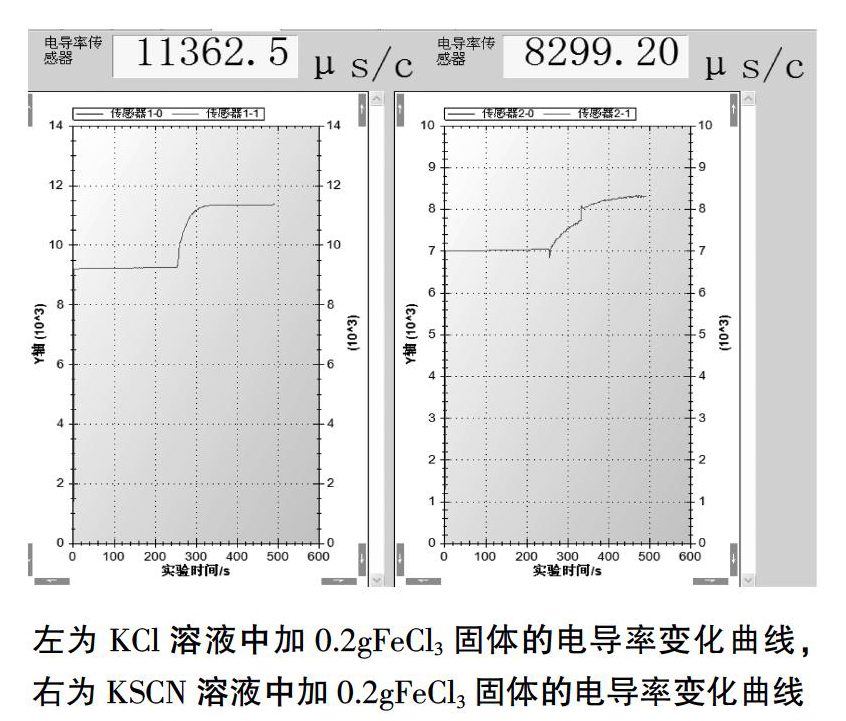
2.在上述溶液中分别加0.2gFeCl3固体(少量),用磁力搅拌器搅拌,观察溶液的导电能力变化,结果如下图所示:
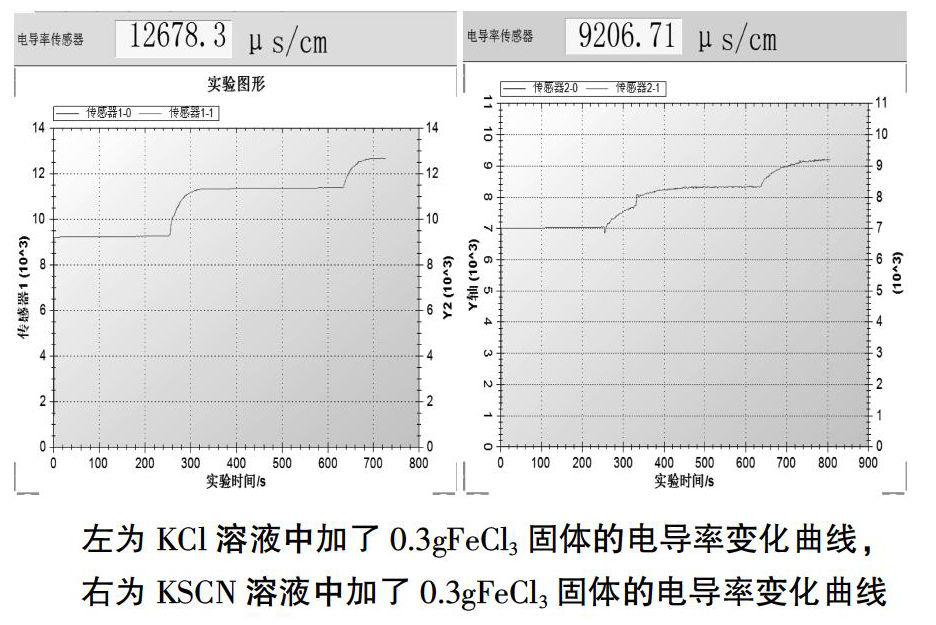
3. 在上述溶液中继续分别加0.1gFeCl3固体,用磁力搅拌器搅拌,观察溶液的导电能力变化,结果如下图所示:
4. 在上述溶液中再次继续加0.1gFeCl3固体(过量),用磁力搅拌器搅拌,观察溶液的导电能力变化,结果如下图所示:
五、 结果分析
1.溶液的导电能力与温度、浓度、电荷数、离子的迁移速率等因素有关,由于离子迁移速率的差异,相同条件下,相同浓度的KCl溶液和KSCN溶液的电导率相差约2225μs/cm。
2.加入0.2gFeCl3固体以后,此时,FeCl3因为量少与KSCN充分反应,若生成的Fe(SCN)3不存在电离,此时溶液的电导率应变化不大,而结果显示电导率仍然上升,上升幅度比同浓度的KCl稍小。说明此时溶液中Fe3+与SCN-开始形成络合物。
3. 再次加入0.1gFeCl3固体,此时原溶液中的KSCN与总的FeCl3物质的量之比为3∶1,恰好完全反应,溶液为Fe(SCN)3与KCl的混合溶液,且KCl的浓度应为0.1mol/L,我们发现此时溶液的电导率与实验开始时0.1mol/L的KCl溶液的电导率几乎相同,证明此时溶液中,Fe3+与SCN-恰好形成了Fe(SCN)3分子,几乎不存在电离。
4.继续加入FeCl3固体0.1g,此时溶液中FeCl3已过量,若此时加进去的Fe3+没有继续反应,溶液的电导率增加幅度应该和KCl溶液相同,结果显示却比KCl要小,证明Fe3+继续再反应形成新的形式的络合物,此时溶液中就不再适合用Fe(SCN)3分子形式来表示络合物了。
六、 实验意义
一直以来,检验三价铁离子的实验都只是停留在对实验现象的粗浅观察,由于配位化合物并不是学业水平考试内容,大部分老师对于Fe(SCN)3也从未提出过质疑。然而从科学的角度讲,弱电解质的说法并不能准确描述配位化合物,而Fe3+与SCN-的配合物也不能简单地由Fe(SCN)3概括。
本实验应用传感器对Fe3+与SCN-的反应进行研究,证明了Fe3+与SCN-的实际络合程度与离子的浓度大小有关,由此建议教材中可用小字部分对于两者的配合物形成过程加以说明,例如:
Fe3++SCN-→Fe(SCN)2+→Fe(SCN)2+→Fe(SCN)3→Fe(SCN)4-→[Fe(SCN)5]2-→[Fe(SCN)6]3-,或者也可将书本中离子方程式的形式改为:Fe3++n SCN-[Fe(SCN)n]3-n。也可以将这个问题设计成一次课外探究活动,一方面解决这个困扰着学生甚至老师的问题,另外一方面也可以帮助对化学学习感兴趣的、有志于发展化学专业的学生掌握实验探究的方法,在追求科学原理的过程中体会解决化学问题的乐趣。
参考文献
[1] 王祖浩.普通高中课程标准实验教科书·化学1[M]. 南京:江苏教育出版社,2014:75
[2] 王祖浩.普通高中课程标准实验教科书·物质结构与性质[M]. 南京:江苏教育出版社,2011:77-78
- 浅谈学生数学核心素养的培养
- 小学音乐体验式教学的技巧
- 新媒体时代小学音乐德育教学的研究
- 童话文本教学要“以趣为先”
- 回归,让体育追寻本真
- 水彩画教学中干湿并用法的实践与探究
- 小学科学创生课堂的实践策略
- 体育强则中国强
- 新时代学生发展离不开劳动教育
- 新理念在初中化学实验教学中的应用
- 在情境教学中构建理趣课堂
- 在学习中蜕变,在蜕变中成长
- 园本教研“三变” 为教师成长开辟幽径
- 赏识,让学困生成长起来
- 小学班主任德育工作探析
- 农村小学班主任工作的有效策略
- 班主任要学会倾听学生的心声
- 如何用“心”做好小学班主任工作
- 新时期班主任工作的根本任务
- 浅谈小学班级管理的艺术
- 浅谈班级规章制度的制订和执行
- 纸短情长话别离
- 教研兴校驱动力研究
- “课程”之我见
- 一位“美术老师”的地理教学启示
- up to sth
- uptotheminute
- up-to-the-minute
- up to the minute
- up to the present day/until the present day
- uptower
- uptown
- uptowner
- uptowners
- uptowns
- uptrained
- uptrend
- upturn
- upturned
- upturner
- upturning
- upturns
- up until/up to
- upvaluation
- upwaft
- upwake
- upward
- upwardly
- upwardly mobile
- upwardlymobile
- 恢诡
- 恢诡谲怪
- 恢谐
- 恢谐戏谑
- 恢豁
- 恢达
- 恢阐
- 恢阔
- 恣
- 恣儿𥩙的
- 恣凶稔恶
- 恣听
- 恣夸
- 恣心
- 恣心所欲
- 恣心纵欲
- 恣志慮
- 恣志虑
- 恣性
- 恣悠悠
- 恣情
- 恣情玩乐
- 恣情纵欲
- 恣意
- 恣意、任意或自由广泛地发表议论、评论