叶小慈 谢永荣


摘要: 要让学生理解和掌握铝与氢氧化钠溶液反应的实质,实验是重要的途径。
设计了两个改进实验:
一是用热的无水乙醇溶解氢氧化钠以加大碱的浓度,加快产生氢气的速率,采用排液的方式收集纯净氢气,通过加水前后反应现象的对比,掌握反应的实质;二是使用注射器实现铝的去膜、与水反应、气体检验一体化,体现反应实质。两个实验都能产生明显的实验教学效果,较好地体现了化学学科核心素养要求。
关键词: 铝; 氢氧化钠溶液; 反应实质; 铝的去膜; 实验改进
文章编号: 10056629(2020)05005904
中图分类号: G633.8
文献标识码: B
人教版教材《化学1(必修)》第三章“金属的化学性质”中的“铝与氢氧化钠溶液反应”实验34“在2支小试管里分别加入5mL盐酸和5mL NaOH溶液,再分别放入一小段铝片,观察实验现象,过一段时间后,将点燃的木条分别放在2支试管口,你看到什么现象?”[1]。教材中描述: 通过实验我们看到,铝既能与盐酸反应,又能与NaOH溶液反应,反应都放出一种可燃性气体氢气。铝与氢氧化钠溶液反应的化学方程式为:
实际上,按照教材的实验设计操作,存在下列三个不足: (1)反应产生的氢气无法燃烧,不能看见火焰;(2)产生的氢气未经验纯步骤就点燃,往往会产生爆鸣声,存在安全隐患;(3)反应现象不能使学生认识到铝与氢氧化钠溶液的反应实质是铝与水的反应。本文通过查阅相关化学文献,比较其中两个有代表性的改进实验。在此基础上又重新设计了两个新的适合课堂演示和学生操作的实验。这两个实验均能顺利地点燃氢气,清晰地看见氢气安静地燃烧,同时还能充分展现铝与水反应的实质。
1 对两个代表性改进实验的对比分析
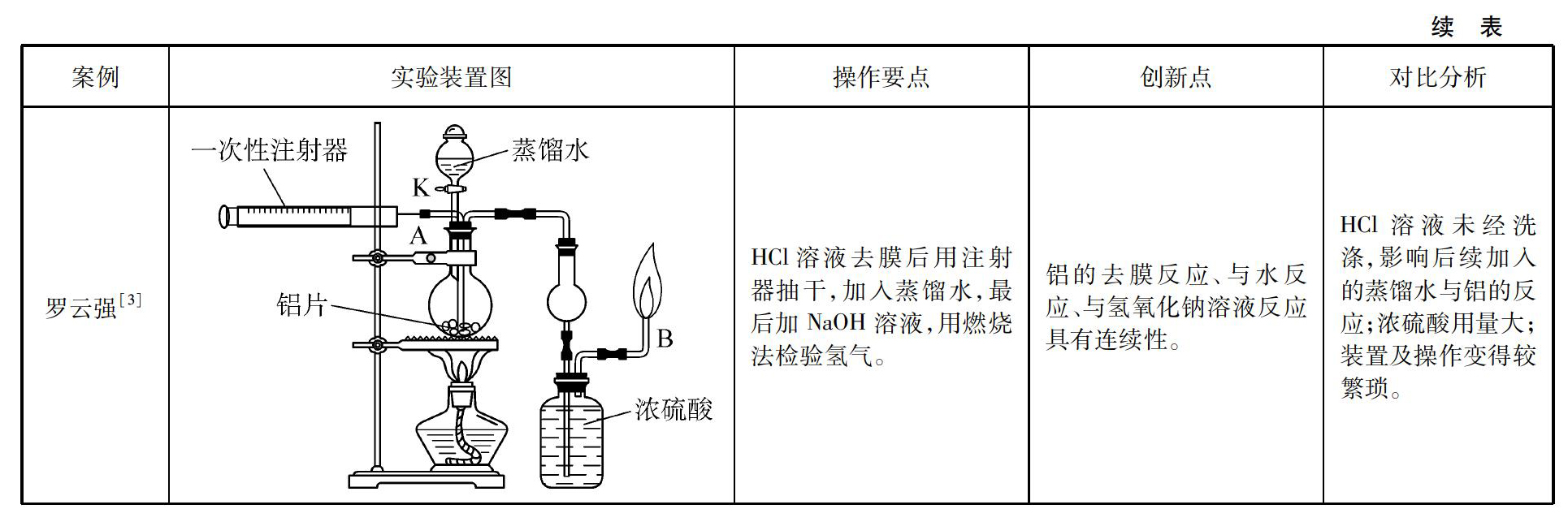
关于铝与氢氧化钠溶液反应的改进实验有很多文献报道,现选取比较有代表性的两个实验进行对比分析,详见表1。
2 铝与氢氧化钠溶液反应实验的再设计
鉴于对以上两种实验的对比分析和对铝的性质的探究,重新设计了两个改进实验,经过多次反复实验验证,均取得较好的实验效果。
2.1 实验一
实验用品与实验装置:
具支试管、橡胶塞、烧杯、玻璃棒、尖嘴玻璃管、橡胶管、火柴、直通活塞、滴管;无水乙醇、NaOH固体、铝丝、蒸馏水。实验装置如图1所示。
实验步骤与现象:
(1) 在100mL的烧杯中加入30mL无水乙醇和1.5g氢氧化钠,用60~70℃水浴加热,使固体氢氧化钠溶解,制成热的饱和氢氧化钠乙醇溶液。
(2) 具支试管的支管接上直通活塞和尖嘴玻璃管,活塞1处于关闭状态,试管中放入适量铝丝,加入上述配置好的30mL热的饱和氢氧化钠乙醇溶液,观察铝丝在氢氧化钠乙醇溶液中不发生反应。
(3) 从具支试管上口通过漏斗加蒸馏水至接近上管口,塞好带长颈分液漏斗的橡胶塞,分液漏斗的活塞2打开着。铝丝表面很快有气泡产生,产生的气体将试管内溶液压至分液漏斗,当试管内液面降至支管口以下时,关闭分液漏斗的活塞2,打开支管直通活塞1(见图1),气体从尖嘴玻璃管排出。
(4) 点燃尖嘴玻璃管口排出的气体,可见明显的蓝色火焰。
注意事项:
(1) 具支试管里的溶液要接近装满,以减少管内的空气,以尽快获得纯净氢气。
(2) 液面降至支管口以下,仍需过一段时间,让试管里少量的空气排净后,尖嘴玻璃管才能点燃。
(3) 无水乙醇吸湿性大,不能选用开封太久的无水乙醇。
设计优点:
(1) 采用排液的方式收集氢气,确保产生纯净的氢气,增加实验的安全性。
(2) 用热的无水乙醇溶解氢氧化钠固体可增大NaOH溶液的浓度,促进反应的进行,提高氢气的产生量使其能够燃烧,增强了实验的直观性。
2.2 实验二
防止铝再次被氧化的方法大致有两种: (1)氯化钠溶液有助于铝片快速和水反应[4];(2)汞盐与铝生成的铝汞齐能阻止铝的氧化膜再生[5]。由于汞盐的毒性大不宜采用,本实验选用1%的氯化钠溶液,并采用注射器作为反应装置。操作步骤如图2所示。
实验用品: 铝条、4mol/L HCl溶液、1% NaCl溶液、2mol/L NaOH溶液、小烧杯、带针头的30mL注射器、肥皂水、酒精燈
实验操作与实验现象:
(1) 将铝条剪成细条状后用笔芯卷成5~6匝的铝圈,拔出注射器活塞芯杆,将铝圈放入。装上活塞芯杆推至贴近铝圈,见图2①。
(2) 从小烧杯中缓缓吸入HCl溶液5mL,见图2②。调整注射器角度,待铝圈有较多气泡冒出时,即可认为去膜完成。此时可用肥皂水检验气体,见图2③。
(3) 缓慢推出HCl溶液,立刻吸入煮沸的NaCl溶液进行洗涤3~4次,见图2④。最后吸入NaCl溶液5mL,调整注射器角度,观察铝表面冒出的气体,见图2⑤。可以看到铝圈表面仍有许多气泡冒出,随溶液温度的降低气泡产生减缓至无明显现象,有明显气泡产生的时间可持续7~8分钟。振荡注射器可以看到少量Al(OH)3白色小颗粒。
(4) 缓慢吸入5mL NaOH溶液,并用胶塞密封针嘴,见图2⑥和⑦。可以看到反应非常激烈,冒出大量的气体,待收集5~10mL气体,拔出胶塞,调整注射器角度靠近火焰点燃,匀速推出气体,可以看到氢气安静燃烧,见图2⑧。
设计优点:
(1) 利用注射器活塞芯杆推、吸的灵活性,使实验洗涤过程变得简单,其密封性保证了不易使去膜后的铝再被氧化。
(2) 实验以注射器作为反应装置具有简单、安全的作用,如果作为课堂演示实验,可以在学生之间传递以观察实验现象。
(3) 用简单的仪器装置可完成铝与氢氧化钠溶液反应实验的去膜、洗涤、铝与水及NaOH溶液反应的一系列操作。
注意事项:
(1) 注射器不能持续加热,实验中所用的必须是煮沸的NaCl溶液。
(2) 盐酸必须经多次洗涤,以排除对铝和水反应现象观察的影响。
(3) 铝圈可以增大铝的反应面积,吸入和推出液体要缓慢匀速,以免吸入空气。
不足之处:
加入NaOH溶液后反应比较激烈,没有经过干燥的氢气中含有少量氯化钠溶液,燃烧时火焰夹带黄色。
3 结语
教材中的实验只是提到铝和氢氧化钠溶液会发生反应,对反应的实质并没有说明。本文参照文献中已有的改进实验的优点和相似性进行新的实验改进设计,通过明显的实验现象推知该反应中水是氧化剂,反应的实质是氢氧化钠溶解了铝和水反应产生的氢氧化铝从而促进了反应的进行。学生通过观察、辨识一定条件下铝与氢氧化钠溶液反应的宏观现象,从微观层面理解物质的性质的联系,体现化学核心素养中的“宏观辨识与微观探析”;根据实验现象推理得出铝与氢氧化钠溶液反应的实质,充分体现了“科学探究与创新意识”素养,培养学生良好的创新思维和解决问题的方式方法。
参考文献:
[1]宋心琦主编. 普通高中课程标准实验教科书·化学1(必修) [M]. 北京: 人民教育出版社, 2007: 51.
[2]唐莹, 黄翠英. 铝和氢氧化钠溶液反应实验改进[J]. 中学化学教学参考, 2017, (16): 65.
[3]罗云强. 铝与氢氧化钠溶液反应的实验探究[J]. 实验教学与仪器, 2011, 28(3): 29~30.
[4]王程杰. 关注氯离子效应在中学化学实验中的应用[J]. 化学教学, 2015, (11): 53~58.
[5]中国人民解放军总参谋部兵种部防化编研室编.刘汉鼎主编. 核化生防护大辞典[Z]. 上海: 上海辞书出版社, 2000.
- 从“帝国”遗产到英国“飞地”:二战结束前后美国视野中香港形象的转变及其意义
- 试论日本的两次“交通战争”
- 北京《商务报》的“知识”面相:清末新政中知识界对“商务”的具体认知
- 行业生存与税制改进:上海华界卷烟特税风潮研究(1923—1926)
- 八旗汉军火器营的创立
- 近代中国城乡划分与市辖区的形成(1909—1936年)
- 试论南宋理学家所撰碑志文中的两浙富民形象
- “国家声音”:民国广播与国语运动
- 略论抗战时期大后方的社会科学研究
- 美国在印度洋的早期经略探析
- 两德统一与欧洲一体化
- 《历史教学》第130卷(2019年1~6期)总目
- 马可·波罗研究在欧洲
- 杨志玖先生与马可·波罗来华的“世纪论战”
- 生长的墓志
- 对反思的沉思
- 秦陵兵马俑艺术源流辨
- 新教节日改革的成效
- 新中国70年中学历史教育价值的演进
- 全面解读明朝灭亡
- 饮茶在近代英国
- 基督教对西欧封建时代的影响
- 初中教材“辛亥革命”研究
- “自由”视阈下的《民国时期民族工业的曲折发展》教学分析与设计
- 历史的昭示 现实的关怀
- unprivatenesses
- unprobational
- unprobationary
- unprobed
- unprocessional
- unproclaimed
- unprocrastinated
- unprocreated
- unprocured
- unprodded
- unprodigious
- unprodigiously
- unprodigiousness
- unprodigiousnesses
- unproduced
- unproducible
- unproductive
- unproductively
- unproductiveness
- unproductivenesses
- unproductivities
- unproductivity
- unprofane
- unprofaned
- unprofanely
- 花色深红
- 花色美
- 花色迷人
- 花艳
- 花艺
- 花花
- 花花世界
- 花花事儿
- 花花公子
- 花花哨
- 花花太岁
- 花花子
- 花花搭搭
- 花花柳柳
- 花花点子
- 花花点点
- 花花田
- 花花簇簇
- 花花糊糊
- 花花绿绿
- 花花绿绿、聚集成堆或成团的样子
- 花花肠子
- 花花草草
- 花花轿子——人抬人
- 花花轿子人抬人