氟代苯硼酸与单糖间结合规律探究
吕辰晨 刘震

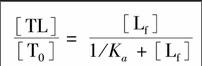
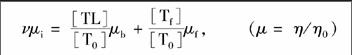
摘 要 取代硼酸与顺式二羟基化合物间的相互作用是设计亲和配基、功能材料和传感元件以分离、富集和识别顺式二羟基化合物的重要基础。氟代苯硼酸在较低pH条件下具有较高的硼亲和力,但其与单糖间的相互作用规律目前尚未得到阐明。本研究以亲和毛细管电泳为相互作用表征手段,研究了9种不同结构的氟代苯硼酸与3种典型单糖(甘露糖、果糖和葡萄糖)在不同pH条件下的结合常数。同时,利用紫外分光光度法测量了这9种氟代苯硼酸的酸度系数。经过结构-性能关联,对氟代苯硼酸与甘露糖、果糖和葡萄糖的结合规律以及对葡萄糖的选择性进行了探讨。
关键词 氟代苯硼酸; 单糖; 相互作用; 亲和毛细管电泳
1 引 言
取代硼酸分子对顺式二羟基结构具有特异性识别作用,被广泛应用于糖、糖蛋白、修饰核苷、RNA等生物分子传感[1~4]和分离富集[5~8]研究中,近年来在亲和分离[9~14]、蛋白质组学[15~19]、代谢组学[20~23]、疾病诊断[24~27]以及固相标记[28]方面得到了越来越多的重要应用。生物样品多为酸性到偏碱性,而且其中含有的顺式二羟基生物分子的丰度低,因硼酸酚基的适用pH范围宽、亲和力高, 在生物学研究中应用广泛。研究取代硼酸与单糖分子间相互作用规律,对于选择合适配基具有重要指导意义。
由于氟原子的特殊结构和电子效应,氟取代被广泛用于药物设计、功能材料等领域中的分子改性,起到增强分子代谢稳定性、改变官能团理化性质和稳定分子构象等作用[29,30]。Yan等[31]考察了卤素取代对硼亲和力的影响,结果表明,氟取代的苯硼酸的亲和力比氯取代和溴取代的高得多。本研究组在前期工作中发现,氟取代能增强苯硼酸在低pH条件下的亲和力[32]。然而,氟取代的位置和数目对苯硼酸的亲和力影响,目前未见文献报道。因此,深入研究氟取代苯硼酸的性质及其与顺式二羟基分子间的相互作用规律具有重要意义。
亲和毛细管电泳(Affinity capillary electrophoresis,ACE)是一种基于被分析物结合前后电泳淌度的变化,表征分子间相互作用的毛细管电泳方法,具有准确度高、重现性好、快速、高通量及操作简便等优点[33]。ACE已被证明是表征取代硼酸与含顺式二羟基生物分子间相互作用的可靠手段[32]。本研究选择3种典型单糖(甘露糖、果糖和葡萄糖)及9种氟代苯硼酸为研究对象,利用ACE考察它们间的相互作用,通过结构-性能关系,分析了氟代苯硼酸与单糖间相互作用与分子结构间的关系规律。硼酸探针分子检测血液中葡萄糖时,果糖为主要干扰物,本研究考察了氟取代苯硼酸对葡萄糖/果糖的选择性。
2 实验部分
2.1 仪器与试剂
2-氟苯硼酸(2-FPBA)、3-氟苯硼酸(3-FPBA)、4-氟苯硼酸(4-FPBA)、2,3-二氟苯硼酸(2,3-DFPBA)、2,4-二氟苯硼酸(2,4-DFPBA)、2,5-二氟苯硼酸(2,5-DFPBA)、2,6-二氟苯硼酸(2,6-DFPBA)、3,5-二氟苯硼酸(3,5-DFPBA)、2-(三氟甲基)苯硼酸(2-TFPBA),均购自百灵威公司,纯度大于97%; 苯硼酸和二甲亚砜(DMSO,分析纯,上海国药集团); D-甘露糖(纯度为99%,Alfa Aesar公司); D-果糖(上海惠兴试剂公司)。以上试剂均未经处理直接使用。实验用水为Milli Q超纯水(Millipore公司),所有溶液使用前用0.45 μm滤膜过滤。
ACE实验在P/ACE MDQ系统(美国Beckman Coulter公司)上进行。实验用毛细管(河北永年锐沣色谱器件有限公司)规格为60 cm×50 μm i.d. (50 cm 至检测器)。若无特殊说明,ACE实验是在25℃下进行,分离电压为 24 kV,二极管阵列检测器检测。每次电泳实验前,依次使用0.1 mol/L NaOH溶液在137.9 kPa条件下冲洗2 min,运行缓冲溶液冲洗2 min。进样采用3.447 kPa,5 s。Nanodrop-2000C微量紫外可见分光光度计(美国Thermo公司)。
2.2 实验方法
2.2.1 亲和毛细管电泳原理 硼酸配基(T)与单糖分子(L)通常以1∶1的化学计量比反应,反应式和结合常数(Ka)如式(1)所示:
当单糖分子对于硼酸分子大大过量时,式(4)中的[Lf]可使用单糖浓度代替。(νμi-μf)是实测的氟代硼酸分子的淌度变化值,而(μb-μf)是硼酸分子与单糖完全结合后与未结合硼酸分子间的淌度差值,对于给定硼酸-糖体系为常数。通过改变运行缓冲溶液中的单糖浓度,可以获得一系列硼酸分子淌度变化值与单糖浓度间关系的数据,根据式(4),用双曲线方程进行数据拟合,获得结合常数Ka的值。
2.2.2 亲和毛细管电泳实验方法 电泳运行缓冲溶液为添加不同浓度单糖分子的50 mmol/L磷酸盐缓冲溶液(PBS,pH 6.0, 7.0 或 8.0),样品使用含有0.1% DMSO的单个或多个硼酸的溶液,浓度为10~10-4 mol/L。对于糖含量大于50 mmol/L的运行缓冲溶液,均对测得的淌度数据进行粘度校正,以排除粘度变化对淌度的影响[34,35]。
2.2.3 数据分析 表观淌度数据由与电泳仪配套的32Karat 软件计算得到。非线性数据分析使用OriginPro8 软件(OriginLab Corporation, USA)。结合常数数据均由3次实验的平均值回归得到。
2.2.4 酸度系数(pKa)的测量
取代硼酸的pKa值利用紫外吸光光度法测量。配制一系列不同pH值的取代硼酸溶液(取代硼酸浓度:3,5-DFPBA为5 mmol/L,其余10 mmol/L,不同pH值溶液硼酸浓度保持一致; 缓冲溶液: 50 mmol/L NaH2PO4-Na2HPO4溶液),测量270 nm处的紫外吸光度,对pH值作图,得到pKa值。
3 结果与讨论
3.1 硼酸酸度的测量
通常认为取代硼酸与糖结合的最佳pH值略高于取代硼酸pKa值,因此pKa值可作为选择结合pH值的参考依据[36]。
通过测量不同pH值下氟代苯硼酸270 nm处的紫外吸光度,得到了不同含氟取代苯硼酸的pKa值(表1)。其中,苯硼酸、4-氟苯硼酸、2,4-二氟苯硼酸和2,5-二氟苯硼酸的结果与文献\[32\]一致。苯环单氟取代可使硼酸pKa值降低0.1~1.2个pH单位,二氟取代可使硼酸pKa值降低1.3~1.9个pH单位。
邻位三氟甲基取代苯硼酸与文献报道的酸性较强的邻位氨基甲基取代苯硼酸[37]和邻位羟基甲基取代苯硼酸[38]结构类似,但却没有测得预期中的低pKa值,pKa值与苯硼酸相比反而升高了一个单位,可能是空间位阻效应阻碍硼酸电离,也可能是三氟甲基能够稳定平面三角形的硼酸结构,具体原因有待进一步实验证实。
3.2 氟代苯硼酸与甘露糖结合常数
甘露糖是糖基化蛋白末端最常见的单糖,研究氟代苯硼酸与甘露糖的结合规律具有重要意义。苯硼酸与甘露糖的结合常数较小[32],实验测得氟取代能使苯硼酸与甘露糖的结合能力最大提高20倍(表2),但结合作用依然较弱,仅勉强达到中等结合强度[36]。结合氟代苯硼酸的pKa值,pH 8.0时,二氟取代苯硼酸的硼酸根主要以四面体结构存在,提高溶液的碱性无法再明显提高硼酸亲和能力。亲和毛细管电泳测量硼酸亲和作用具有高通量、高准确度、适用于不同取代硼酸分子之间亲和能力强弱比较的优势[32],利用该技术对5种二氟取代苯硼酸的结合能力进行了进一步区分。2,3-二氟苯硼酸、2,4-二氟苯硼酸、2,5-二氟苯硼酸与甘露糖的结合强弱与氟取代对其pKa值影响基本一致,而2,6-二氟苯硼酸和3,5-二氟苯硼酸与甘露糖的亲和能力强弱与酸度不一致,说明位阻对硼酸与甘露糖的结合有明显影响。
邻位三氟取代甲基苯硼酸,具有与Wulff型苯硼酸[36]和改进Wulff型苯硼酸[37]相似的结构,如果与硼酸官能团之间存在电子效应,可能会对硼酸的亲和作用有较大影响。从结合常数的数值可知,pH 7.0时,邻位三氟取代甲基苯硼酸与甘露糖的结合常数是苯硼酸的两倍; 而pH 8.0时,邻位三氟取代甲基苯硼酸与甘露糖的结合常数不升反降,说明在pH 7.0 和pH 8.0时邻位三氟取代甲基苯硼酸与甘露糖的结合作用机理可能发生了变化。
3.3 氟代苯硼酸与果糖结合常数
果糖是单糖中与硼酸结合力最强的分子,可用于比较不同取代硼酸亲和能力。测量了氟代苯硼酸与果糖在弱酸性(pH 6.0)\,中性(pH 7.0)和弱碱性(pH 8.0)条件下的结合常数。
对于单氟取代硼酸,在弱酸性和中性条件下,邻、间、对位取代苯硼酸结合能力与其酸度一致; 弱碱性(pH 8.0)条件下,间位氟取代苯硼酸与果糖的结合能力超过了邻位氟取代苯硼酸。对于二氟取代苯硼酸,在中性和弱酸性条件下,2,3-二氟苯硼酸、2,5-二氟苯硼酸、3,5-二氟苯硼酸与果糖的结合能力基本相当,2,4-二氟苯硼酸、2,6-二氟苯硼酸与果糖的结合常数仅为另外3种氟代硼酸结合常数的1/2,与硼酸酸度强弱不完全一致。在弱碱性条件下,邻位氟取代的优势逐渐丧失,3,5-二氟苯硼酸具有最强的亲和能力,说明二氟取代苯硼酸与果糖结合强弱是电子效应和空间位阻共同作用的结果。
邻位三氟取代甲基苯硼酸,在中性和弱酸性条件下,与果糖的结合作用十分弱(中性条件下结合常数不到苯硼酸的1/10)。而在弱碱性条件下,邻位三氟取代甲基苯硼酸与果糖结合能力迅速增强,与苯硼酸接近。关于果糖与苯硼酸的强结合能力,多数文献认为源自其占主导地位的含顺式邻位二羟基结构的呋喃糖形式,使二羟基间角度更适合与硼酸形成硼酸酯五元环[39,40]; 但也有研究认为,果糖的顺式邻二羟基结构与硼酸成酯的同时,环外羟基与硼原子配位增强硼酸酯稳定性,使结合能力强于其它单糖[40],同时受邻位基团的影响更加明显 \[41]。邻位三氟甲基苯硼酸与果糖间相互作用的异常现象佐证了第二种观点,在中性和弱酸性条件下,苯硼酸与果糖的结合受益于果糖环外羟基与硼原子配位,三氟甲基巨大的位阻效应阻止了配位键的形成; 而在弱碱性条件下,硼酸酯稳定性增强,受配位作用影响减弱,邻位三氟甲基苯硼酸与果糖结合能力增强。
3.4 含氟苯硼酸对葡萄糖的结合选择性
葡萄糖为人血液中浓度最高的糖,也是糖尿病检测的标志物。葡萄糖与取代硼酸的结合作用通常较弱,因此许多研究[2,42]以提高取代硼酸与葡萄糖的结合能力和选择性为目标。尽管血液中果糖浓度低,但由于果糖与硼酸的结合常数通常较葡萄糖高两个数量级,因此为血糖检测的主要干扰物。葡萄糖主要以吡喃糖形式存在,而果糖主要以呋喃糖形式存在。早期研究葡萄糖探针分子的文献对硼酸探针分子与葡萄糖吡喃糖结合的结构进行了解析[43],但后来的研究多证实葡萄糖也是以呋喃糖形式与硼酸结合[42,44]。葡萄糖探针分子多为二硼酸分子,与葡萄糖的两组顺式二羟基结构结合[42,44],使探针分子与葡萄糖的结合常数远高于其它以吡喃糖为主要形式的单糖分子,如甘露糖、半乳糖,但抗果糖干扰能力差[2]。果糖与取代硼酸分子的结合受邻位基团的影响较大,通过在苯硼酸邻位引入取代基团,可以提高葡萄糖/果糖的相对结合能力[41]。本研究表征了不同位置氟取代苯硼酸与葡萄糖在中性条件下的结合常数。氟取代苯硼酸的结合常数如表2所示,果糖与葡萄糖在中性条件下的相对结合能力数据见表3。
由氟取代苯硼酸与葡萄糖的结合常数可知,邻位氟取代和二氟取代均可使硼酸与葡萄糖在中性条件下的亲和常数提高一个数量级及以上。由表3可见,氟取代提高了苯硼酸在中性条件下对葡萄糖的选择性; 通常,邻位有取代基的苯硼酸对葡萄糖的选择性较高(2,6-二氟苯硼酸除外); 邻位三氟甲基苯硼酸与葡萄糖的结合能力与苯硼酸相似,但其在中性条件下与果糖的结合受到抑制,取代硼酸具有对葡萄糖最高的选择性。
4 结 论
本研究表征了9种氟代苯硼酸与3种典型单糖在不同pH条件下的结合常数,并测量了这9种氟代苯硼酸的酸度系数,通过结构-性质关联,剖析了氟取代位置与硼酸亲和能力强弱之间的关系。此外,本研究还考察了邻位三氟甲基对硼酸电离和成酯的抑制作用,以及对葡萄糖的较高选择性。以上研究为设计和利用高亲和力硼酸配基提供了重要依据。
References
1 Nishiyabu R, Kubo Y, James T D, Fossey J S. Chem. Commun., 2011, 47: 1106-1123
2 Liu Y, Deng C, Tang L, Qin A, Hu R, Sun J Z, Tang B Z. J. Am. Chem. Soc., 2011, 133: 660-663
3 Vlandas A, Kurkina T, Ahmad A, Kern K, Balasubramanian K. Anal. Chem., 2010, 82: 6090-6097
4 Bi X D, Li D J, Liu Z. Anal. Chem., 2015, 87: 4442-4447
5 Dou P, Liang L, He J G, Liu Z, Chen, H Y. J. Chromatogr. A, 2009, 1216: 7558-7563
6 Li H, Liu Z. Trends Anal. Chem., 2012, 37: 148-161
7 Wang H Y, Lü C C, Li H Y, Chen Y, Zhou M, Ouyang J, Liu Z. Anal. Bioanal. Chem., 2013, 405: 8579-8586
8 Wang S S, Ye J, Bie Z J, Liu Z. Chem. Sci., 2014, 5: 1135-1140
9 Ren LB, Liu Z, Dong M M, Ye M L, Zou H F. J. Chromatogr. A, 2009, 1216: 4768-4774
10 Ren L B, Liu Z, Liu Y C, Dou, P, Chen H Y. Angew. Chem. Int. Ed., 2009, 48: 6704-6707
11 Chen M, Lu Y, Ma Q,Guo L, FengY Q. Analyst, 2009, 134: 2158-2164
12 Sun X L, Liu R, He X W, Chen L X, Zhang Y. K. Talanta, 2010, 81: 856-864
13 Lin Z A, Pang J L, Lin Y, Huang H, Cai Z W, Zhang L, Chen G N. Analyst, 2011, 136: 3281-3288
14 Liu Y C, Lu Y, Liu Z. Chem. Sci., 2012, 3: 1467-1471
15 Xu Y W, Wu Z X, Zhang L J, Lu H J, Yang P Y, Webley P A, Zhao D Y. Anal. Chem., 2009, 81: 503-508
16 Tang J, Liu Y, Yin P, Yao G P, Yan G Q, Deng C H, Zhang X M. Proteomics, 2010, 10: 2000-2014
17 Wang Y L, Liu M B, Xie L Q, Fang C Y, Xiong H M, Lu H J. Anal. Chem., 2014, 86: 2057-2064
18 Liu J X, Qu Y Y, Yang K G, Wu Q, Shan Y C, Zhang L H, Liang Z, Zhang Y K. ACS Appl. Mater. Interfaces, 2014, 6: 2059-2066
19 Bie Z J, Chen Y, Li H, Wu R, Liu Z. Anal. Chim. Acta, 2014, 834: 1-8
20 Li Q J, Lü C C, Li H Y, Liu Y C, Wang H Y, Wang X, Liu Z. J. Chromatogr. A, 2012, 1256: 114-120
21 Li D, Li Q, Wang S, Ye J, Nie H, Liu Z. J. Chromatogr. A, 2014, 1339: 103-109
22 Li H, Shan Y H, Qiao L Z, Dou A, Shi X Z,Xu G W. Anal. Chem., 2013, 85: 11585-11592
23 Jiang H P, Qi C B, Chu J M, Yuan B F, Feng Y Q. Sci. Rep., 2015, 5: 1-9
24 Li L, Lu Y, Bie Z J, Chen H Y, Liu Z. Angew. Chem. Int. Ed., 2013, 52: 7451-7454
25 Ye J, Chen Y, Liu Z. Angew. Chem. Int. Ed., 2014, 53: 10386-10389
26 Bi X D, Liu Z. Anal. Chem., 2014, 86: 959-966
27 Bi X D, Liu Z. Anal. Chem., 2014, 86: 12382-12389
28 Pan X H, Chen Y, Zhao P X, Li D J, Liu Z. Angew. Chem. Int. Ed., 2015, 54: 6173-6176
29 O′Hagan D. J. Fluor. Chem., 2010, 131: 1071-1081
30 Purser S, Moore P R, Swallow S, Gouverneur V. Chem. Soc. Rev., 2008, 37: 320-330
31 Yan J, Springsteen G, Deeter S, Wang B H. Tetrahedron, 2004, 60: 11205-11209
32 Lü C C, Li H Y, Wang H Y, Liu Z. Anal. Chem., 2013, 85: 2361-2369
33 Tanaka Y, Terabe S. J. Chromatogr. B, 2002, 768 (1): 81-92
34 Britz-McKibbin P, Chen D D Y. Electrophoresis, 2002, 23 (6): 880-888
35 Ostergaard J, Jensen H, Hoim R. J. Sep. Sci., 2009, 32 (10): 1712-1721
36 Springsteen G, Wang B H. Tetrahedron, 2002, 58: 5291-5300
37 Li H Y, Liu Y C, Liu J, Liu Z. Chem. Commun., 2011, 47 (28): 8169-8171
38 Li H Y, Wang H Y, Liu Y C, Liu Z. Chem. Commun., 2012, 48 (34): 4115-4117
39 Shoji E, Freund M S. J. Am. Chem. Soc., 2002, 124 (42): 12486-12493
40 Nicholls M P, Paul P K C. Org. Bio. Chem., 2004, 2 (10): 1434-1441
41 Wiskur S L, Lavigne J L, Metzger A, Tobey S L, Lynch V, Anslyn E V. Chem. Eur. J., 2004, 10 (15): 3792-3804
42 Eggert H, Frederiksen J, Morin C, Norrild J C. J. Org. Chem., 1999, 64: 3846-3852
43 Tsukagoshi K, Shinkai S. J. Org. Chem., 1991, 56(13): 4089-4091
44 Norrild J C, Eggert H. J. Am. Chem. Soc., 1995, 117: 1479-1484

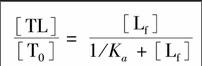
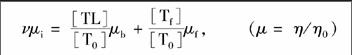
摘 要 取代硼酸与顺式二羟基化合物间的相互作用是设计亲和配基、功能材料和传感元件以分离、富集和识别顺式二羟基化合物的重要基础。氟代苯硼酸在较低pH条件下具有较高的硼亲和力,但其与单糖间的相互作用规律目前尚未得到阐明。本研究以亲和毛细管电泳为相互作用表征手段,研究了9种不同结构的氟代苯硼酸与3种典型单糖(甘露糖、果糖和葡萄糖)在不同pH条件下的结合常数。同时,利用紫外分光光度法测量了这9种氟代苯硼酸的酸度系数。经过结构-性能关联,对氟代苯硼酸与甘露糖、果糖和葡萄糖的结合规律以及对葡萄糖的选择性进行了探讨。
关键词 氟代苯硼酸; 单糖; 相互作用; 亲和毛细管电泳
1 引 言
取代硼酸分子对顺式二羟基结构具有特异性识别作用,被广泛应用于糖、糖蛋白、修饰核苷、RNA等生物分子传感[1~4]和分离富集[5~8]研究中,近年来在亲和分离[9~14]、蛋白质组学[15~19]、代谢组学[20~23]、疾病诊断[24~27]以及固相标记[28]方面得到了越来越多的重要应用。生物样品多为酸性到偏碱性,而且其中含有的顺式二羟基生物分子的丰度低,因硼酸酚基的适用pH范围宽、亲和力高, 在生物学研究中应用广泛。研究取代硼酸与单糖分子间相互作用规律,对于选择合适配基具有重要指导意义。
由于氟原子的特殊结构和电子效应,氟取代被广泛用于药物设计、功能材料等领域中的分子改性,起到增强分子代谢稳定性、改变官能团理化性质和稳定分子构象等作用[29,30]。Yan等[31]考察了卤素取代对硼亲和力的影响,结果表明,氟取代的苯硼酸的亲和力比氯取代和溴取代的高得多。本研究组在前期工作中发现,氟取代能增强苯硼酸在低pH条件下的亲和力[32]。然而,氟取代的位置和数目对苯硼酸的亲和力影响,目前未见文献报道。因此,深入研究氟取代苯硼酸的性质及其与顺式二羟基分子间的相互作用规律具有重要意义。
亲和毛细管电泳(Affinity capillary electrophoresis,ACE)是一种基于被分析物结合前后电泳淌度的变化,表征分子间相互作用的毛细管电泳方法,具有准确度高、重现性好、快速、高通量及操作简便等优点[33]。ACE已被证明是表征取代硼酸与含顺式二羟基生物分子间相互作用的可靠手段[32]。本研究选择3种典型单糖(甘露糖、果糖和葡萄糖)及9种氟代苯硼酸为研究对象,利用ACE考察它们间的相互作用,通过结构-性能关系,分析了氟代苯硼酸与单糖间相互作用与分子结构间的关系规律。硼酸探针分子检测血液中葡萄糖时,果糖为主要干扰物,本研究考察了氟取代苯硼酸对葡萄糖/果糖的选择性。
2 实验部分
2.1 仪器与试剂
2-氟苯硼酸(2-FPBA)、3-氟苯硼酸(3-FPBA)、4-氟苯硼酸(4-FPBA)、2,3-二氟苯硼酸(2,3-DFPBA)、2,4-二氟苯硼酸(2,4-DFPBA)、2,5-二氟苯硼酸(2,5-DFPBA)、2,6-二氟苯硼酸(2,6-DFPBA)、3,5-二氟苯硼酸(3,5-DFPBA)、2-(三氟甲基)苯硼酸(2-TFPBA),均购自百灵威公司,纯度大于97%; 苯硼酸和二甲亚砜(DMSO,分析纯,上海国药集团); D-甘露糖(纯度为99%,Alfa Aesar公司); D-果糖(上海惠兴试剂公司)。以上试剂均未经处理直接使用。实验用水为Milli Q超纯水(Millipore公司),所有溶液使用前用0.45 μm滤膜过滤。
ACE实验在P/ACE MDQ系统(美国Beckman Coulter公司)上进行。实验用毛细管(河北永年锐沣色谱器件有限公司)规格为60 cm×50 μm i.d. (50 cm 至检测器)。若无特殊说明,ACE实验是在25℃下进行,分离电压为 24 kV,二极管阵列检测器检测。每次电泳实验前,依次使用0.1 mol/L NaOH溶液在137.9 kPa条件下冲洗2 min,运行缓冲溶液冲洗2 min。进样采用3.447 kPa,5 s。Nanodrop-2000C微量紫外可见分光光度计(美国Thermo公司)。
2.2 实验方法
2.2.1 亲和毛细管电泳原理 硼酸配基(T)与单糖分子(L)通常以1∶1的化学计量比反应,反应式和结合常数(Ka)如式(1)所示:
当单糖分子对于硼酸分子大大过量时,式(4)中的[Lf]可使用单糖浓度代替。(νμi-μf)是实测的氟代硼酸分子的淌度变化值,而(μb-μf)是硼酸分子与单糖完全结合后与未结合硼酸分子间的淌度差值,对于给定硼酸-糖体系为常数。通过改变运行缓冲溶液中的单糖浓度,可以获得一系列硼酸分子淌度变化值与单糖浓度间关系的数据,根据式(4),用双曲线方程进行数据拟合,获得结合常数Ka的值。
2.2.2 亲和毛细管电泳实验方法 电泳运行缓冲溶液为添加不同浓度单糖分子的50 mmol/L磷酸盐缓冲溶液(PBS,pH 6.0, 7.0 或 8.0),样品使用含有0.1% DMSO的单个或多个硼酸的溶液,浓度为10~10-4 mol/L。对于糖含量大于50 mmol/L的运行缓冲溶液,均对测得的淌度数据进行粘度校正,以排除粘度变化对淌度的影响[34,35]。
2.2.3 数据分析 表观淌度数据由与电泳仪配套的32Karat 软件计算得到。非线性数据分析使用OriginPro8 软件(OriginLab Corporation, USA)。结合常数数据均由3次实验的平均值回归得到。
2.2.4 酸度系数(pKa)的测量
取代硼酸的pKa值利用紫外吸光光度法测量。配制一系列不同pH值的取代硼酸溶液(取代硼酸浓度:3,5-DFPBA为5 mmol/L,其余10 mmol/L,不同pH值溶液硼酸浓度保持一致; 缓冲溶液: 50 mmol/L NaH2PO4-Na2HPO4溶液),测量270 nm处的紫外吸光度,对pH值作图,得到pKa值。
3 结果与讨论
3.1 硼酸酸度的测量
通常认为取代硼酸与糖结合的最佳pH值略高于取代硼酸pKa值,因此pKa值可作为选择结合pH值的参考依据[36]。
通过测量不同pH值下氟代苯硼酸270 nm处的紫外吸光度,得到了不同含氟取代苯硼酸的pKa值(表1)。其中,苯硼酸、4-氟苯硼酸、2,4-二氟苯硼酸和2,5-二氟苯硼酸的结果与文献\[32\]一致。苯环单氟取代可使硼酸pKa值降低0.1~1.2个pH单位,二氟取代可使硼酸pKa值降低1.3~1.9个pH单位。
邻位三氟甲基取代苯硼酸与文献报道的酸性较强的邻位氨基甲基取代苯硼酸[37]和邻位羟基甲基取代苯硼酸[38]结构类似,但却没有测得预期中的低pKa值,pKa值与苯硼酸相比反而升高了一个单位,可能是空间位阻效应阻碍硼酸电离,也可能是三氟甲基能够稳定平面三角形的硼酸结构,具体原因有待进一步实验证实。
3.2 氟代苯硼酸与甘露糖结合常数
甘露糖是糖基化蛋白末端最常见的单糖,研究氟代苯硼酸与甘露糖的结合规律具有重要意义。苯硼酸与甘露糖的结合常数较小[32],实验测得氟取代能使苯硼酸与甘露糖的结合能力最大提高20倍(表2),但结合作用依然较弱,仅勉强达到中等结合强度[36]。结合氟代苯硼酸的pKa值,pH 8.0时,二氟取代苯硼酸的硼酸根主要以四面体结构存在,提高溶液的碱性无法再明显提高硼酸亲和能力。亲和毛细管电泳测量硼酸亲和作用具有高通量、高准确度、适用于不同取代硼酸分子之间亲和能力强弱比较的优势[32],利用该技术对5种二氟取代苯硼酸的结合能力进行了进一步区分。2,3-二氟苯硼酸、2,4-二氟苯硼酸、2,5-二氟苯硼酸与甘露糖的结合强弱与氟取代对其pKa值影响基本一致,而2,6-二氟苯硼酸和3,5-二氟苯硼酸与甘露糖的亲和能力强弱与酸度不一致,说明位阻对硼酸与甘露糖的结合有明显影响。
邻位三氟取代甲基苯硼酸,具有与Wulff型苯硼酸[36]和改进Wulff型苯硼酸[37]相似的结构,如果与硼酸官能团之间存在电子效应,可能会对硼酸的亲和作用有较大影响。从结合常数的数值可知,pH 7.0时,邻位三氟取代甲基苯硼酸与甘露糖的结合常数是苯硼酸的两倍; 而pH 8.0时,邻位三氟取代甲基苯硼酸与甘露糖的结合常数不升反降,说明在pH 7.0 和pH 8.0时邻位三氟取代甲基苯硼酸与甘露糖的结合作用机理可能发生了变化。
3.3 氟代苯硼酸与果糖结合常数
果糖是单糖中与硼酸结合力最强的分子,可用于比较不同取代硼酸亲和能力。测量了氟代苯硼酸与果糖在弱酸性(pH 6.0)\,中性(pH 7.0)和弱碱性(pH 8.0)条件下的结合常数。
对于单氟取代硼酸,在弱酸性和中性条件下,邻、间、对位取代苯硼酸结合能力与其酸度一致; 弱碱性(pH 8.0)条件下,间位氟取代苯硼酸与果糖的结合能力超过了邻位氟取代苯硼酸。对于二氟取代苯硼酸,在中性和弱酸性条件下,2,3-二氟苯硼酸、2,5-二氟苯硼酸、3,5-二氟苯硼酸与果糖的结合能力基本相当,2,4-二氟苯硼酸、2,6-二氟苯硼酸与果糖的结合常数仅为另外3种氟代硼酸结合常数的1/2,与硼酸酸度强弱不完全一致。在弱碱性条件下,邻位氟取代的优势逐渐丧失,3,5-二氟苯硼酸具有最强的亲和能力,说明二氟取代苯硼酸与果糖结合强弱是电子效应和空间位阻共同作用的结果。
邻位三氟取代甲基苯硼酸,在中性和弱酸性条件下,与果糖的结合作用十分弱(中性条件下结合常数不到苯硼酸的1/10)。而在弱碱性条件下,邻位三氟取代甲基苯硼酸与果糖结合能力迅速增强,与苯硼酸接近。关于果糖与苯硼酸的强结合能力,多数文献认为源自其占主导地位的含顺式邻位二羟基结构的呋喃糖形式,使二羟基间角度更适合与硼酸形成硼酸酯五元环[39,40]; 但也有研究认为,果糖的顺式邻二羟基结构与硼酸成酯的同时,环外羟基与硼原子配位增强硼酸酯稳定性,使结合能力强于其它单糖[40],同时受邻位基团的影响更加明显 \[41]。邻位三氟甲基苯硼酸与果糖间相互作用的异常现象佐证了第二种观点,在中性和弱酸性条件下,苯硼酸与果糖的结合受益于果糖环外羟基与硼原子配位,三氟甲基巨大的位阻效应阻止了配位键的形成; 而在弱碱性条件下,硼酸酯稳定性增强,受配位作用影响减弱,邻位三氟甲基苯硼酸与果糖结合能力增强。
3.4 含氟苯硼酸对葡萄糖的结合选择性
葡萄糖为人血液中浓度最高的糖,也是糖尿病检测的标志物。葡萄糖与取代硼酸的结合作用通常较弱,因此许多研究[2,42]以提高取代硼酸与葡萄糖的结合能力和选择性为目标。尽管血液中果糖浓度低,但由于果糖与硼酸的结合常数通常较葡萄糖高两个数量级,因此为血糖检测的主要干扰物。葡萄糖主要以吡喃糖形式存在,而果糖主要以呋喃糖形式存在。早期研究葡萄糖探针分子的文献对硼酸探针分子与葡萄糖吡喃糖结合的结构进行了解析[43],但后来的研究多证实葡萄糖也是以呋喃糖形式与硼酸结合[42,44]。葡萄糖探针分子多为二硼酸分子,与葡萄糖的两组顺式二羟基结构结合[42,44],使探针分子与葡萄糖的结合常数远高于其它以吡喃糖为主要形式的单糖分子,如甘露糖、半乳糖,但抗果糖干扰能力差[2]。果糖与取代硼酸分子的结合受邻位基团的影响较大,通过在苯硼酸邻位引入取代基团,可以提高葡萄糖/果糖的相对结合能力[41]。本研究表征了不同位置氟取代苯硼酸与葡萄糖在中性条件下的结合常数。氟取代苯硼酸的结合常数如表2所示,果糖与葡萄糖在中性条件下的相对结合能力数据见表3。
由氟取代苯硼酸与葡萄糖的结合常数可知,邻位氟取代和二氟取代均可使硼酸与葡萄糖在中性条件下的亲和常数提高一个数量级及以上。由表3可见,氟取代提高了苯硼酸在中性条件下对葡萄糖的选择性; 通常,邻位有取代基的苯硼酸对葡萄糖的选择性较高(2,6-二氟苯硼酸除外); 邻位三氟甲基苯硼酸与葡萄糖的结合能力与苯硼酸相似,但其在中性条件下与果糖的结合受到抑制,取代硼酸具有对葡萄糖最高的选择性。
4 结 论
本研究表征了9种氟代苯硼酸与3种典型单糖在不同pH条件下的结合常数,并测量了这9种氟代苯硼酸的酸度系数,通过结构-性质关联,剖析了氟取代位置与硼酸亲和能力强弱之间的关系。此外,本研究还考察了邻位三氟甲基对硼酸电离和成酯的抑制作用,以及对葡萄糖的较高选择性。以上研究为设计和利用高亲和力硼酸配基提供了重要依据。
References
1 Nishiyabu R, Kubo Y, James T D, Fossey J S. Chem. Commun., 2011, 47: 1106-1123
2 Liu Y, Deng C, Tang L, Qin A, Hu R, Sun J Z, Tang B Z. J. Am. Chem. Soc., 2011, 133: 660-663
3 Vlandas A, Kurkina T, Ahmad A, Kern K, Balasubramanian K. Anal. Chem., 2010, 82: 6090-6097
4 Bi X D, Li D J, Liu Z. Anal. Chem., 2015, 87: 4442-4447
5 Dou P, Liang L, He J G, Liu Z, Chen, H Y. J. Chromatogr. A, 2009, 1216: 7558-7563
6 Li H, Liu Z. Trends Anal. Chem., 2012, 37: 148-161
7 Wang H Y, Lü C C, Li H Y, Chen Y, Zhou M, Ouyang J, Liu Z. Anal. Bioanal. Chem., 2013, 405: 8579-8586
8 Wang S S, Ye J, Bie Z J, Liu Z. Chem. Sci., 2014, 5: 1135-1140
9 Ren LB, Liu Z, Dong M M, Ye M L, Zou H F. J. Chromatogr. A, 2009, 1216: 4768-4774
10 Ren L B, Liu Z, Liu Y C, Dou, P, Chen H Y. Angew. Chem. Int. Ed., 2009, 48: 6704-6707
11 Chen M, Lu Y, Ma Q,Guo L, FengY Q. Analyst, 2009, 134: 2158-2164
12 Sun X L, Liu R, He X W, Chen L X, Zhang Y. K. Talanta, 2010, 81: 856-864
13 Lin Z A, Pang J L, Lin Y, Huang H, Cai Z W, Zhang L, Chen G N. Analyst, 2011, 136: 3281-3288
14 Liu Y C, Lu Y, Liu Z. Chem. Sci., 2012, 3: 1467-1471
15 Xu Y W, Wu Z X, Zhang L J, Lu H J, Yang P Y, Webley P A, Zhao D Y. Anal. Chem., 2009, 81: 503-508
16 Tang J, Liu Y, Yin P, Yao G P, Yan G Q, Deng C H, Zhang X M. Proteomics, 2010, 10: 2000-2014
17 Wang Y L, Liu M B, Xie L Q, Fang C Y, Xiong H M, Lu H J. Anal. Chem., 2014, 86: 2057-2064
18 Liu J X, Qu Y Y, Yang K G, Wu Q, Shan Y C, Zhang L H, Liang Z, Zhang Y K. ACS Appl. Mater. Interfaces, 2014, 6: 2059-2066
19 Bie Z J, Chen Y, Li H, Wu R, Liu Z. Anal. Chim. Acta, 2014, 834: 1-8
20 Li Q J, Lü C C, Li H Y, Liu Y C, Wang H Y, Wang X, Liu Z. J. Chromatogr. A, 2012, 1256: 114-120
21 Li D, Li Q, Wang S, Ye J, Nie H, Liu Z. J. Chromatogr. A, 2014, 1339: 103-109
22 Li H, Shan Y H, Qiao L Z, Dou A, Shi X Z,Xu G W. Anal. Chem., 2013, 85: 11585-11592
23 Jiang H P, Qi C B, Chu J M, Yuan B F, Feng Y Q. Sci. Rep., 2015, 5: 1-9
24 Li L, Lu Y, Bie Z J, Chen H Y, Liu Z. Angew. Chem. Int. Ed., 2013, 52: 7451-7454
25 Ye J, Chen Y, Liu Z. Angew. Chem. Int. Ed., 2014, 53: 10386-10389
26 Bi X D, Liu Z. Anal. Chem., 2014, 86: 959-966
27 Bi X D, Liu Z. Anal. Chem., 2014, 86: 12382-12389
28 Pan X H, Chen Y, Zhao P X, Li D J, Liu Z. Angew. Chem. Int. Ed., 2015, 54: 6173-6176
29 O′Hagan D. J. Fluor. Chem., 2010, 131: 1071-1081
30 Purser S, Moore P R, Swallow S, Gouverneur V. Chem. Soc. Rev., 2008, 37: 320-330
31 Yan J, Springsteen G, Deeter S, Wang B H. Tetrahedron, 2004, 60: 11205-11209
32 Lü C C, Li H Y, Wang H Y, Liu Z. Anal. Chem., 2013, 85: 2361-2369
33 Tanaka Y, Terabe S. J. Chromatogr. B, 2002, 768 (1): 81-92
34 Britz-McKibbin P, Chen D D Y. Electrophoresis, 2002, 23 (6): 880-888
35 Ostergaard J, Jensen H, Hoim R. J. Sep. Sci., 2009, 32 (10): 1712-1721
36 Springsteen G, Wang B H. Tetrahedron, 2002, 58: 5291-5300
37 Li H Y, Liu Y C, Liu J, Liu Z. Chem. Commun., 2011, 47 (28): 8169-8171
38 Li H Y, Wang H Y, Liu Y C, Liu Z. Chem. Commun., 2012, 48 (34): 4115-4117
39 Shoji E, Freund M S. J. Am. Chem. Soc., 2002, 124 (42): 12486-12493
40 Nicholls M P, Paul P K C. Org. Bio. Chem., 2004, 2 (10): 1434-1441
41 Wiskur S L, Lavigne J L, Metzger A, Tobey S L, Lynch V, Anslyn E V. Chem. Eur. J., 2004, 10 (15): 3792-3804
42 Eggert H, Frederiksen J, Morin C, Norrild J C. J. Org. Chem., 1999, 64: 3846-3852
43 Tsukagoshi K, Shinkai S. J. Org. Chem., 1991, 56(13): 4089-4091
44 Norrild J C, Eggert H. J. Am. Chem. Soc., 1995, 117: 1479-1484

