磁性粒子表面自组装辛可宁分子印迹电致化学发光传感器
魏小平等

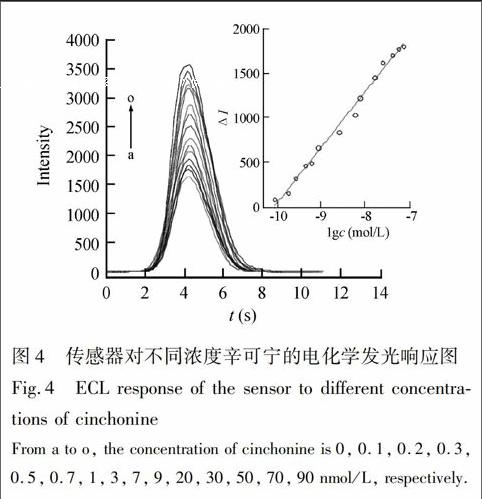
摘 要 以辛可宁为模板分子、十二烷基硫醇为功能单体,在Fe3O4@Au纳米粒子表面自组装辛可宁分子印迹膜,构建了新型磁性粒子分子印迹电化学发光传感器。通过透射电子显微镜对磁性纳米粒子的粒径分布及形貌进行了表征,使用红外光谱对比分析了辛可宁、分子印迹膜洗脱前和洗脱后的结构及成分。结果表明,在最优的实验条件下(0.012 mol/L 硼砂缓冲溶液(pH 9.5),0.8 mmol/L Ru(bpy)2+3),辛可宁浓度的对数在1 × 10 10~9 × 10 8 mol/L范围内,与电化学发光强度变化值有良好的线性关系,检出限为3.5×10 11 mol/L。此传感器灵敏度高、选择性好、易于更新,将其用于血清样品的检测,方法回收率为98.8%~104.7%。
关键词 分子印迹传感器; 磁性纳米粒子; 辛可宁; 自组装; 电致化学发光
1 引 言
分子印迹传感器具有对目标分子专一识别的特性以及良好的机械稳定性和热稳定性,近年来受到越来越多研究者的关注[1~4]。分子印迹传感器的合成方法通常是使目标分子、功能单体以及交联剂三者之间发生三维聚合反应,经洗脱模板分子后,留下对目标分子具有较高选择性和亲和力的识别位点。然而,传统制备方法所得到的印迹传感器每次使用后需要进行印迹膜的更新,繁琐、费时,且重现性差[5~7]。
磁性Fe3O4纳米粒子不仅具有诸多纳米材料的优点,而且还具有超顺磁效应,在外加磁场的作用下,能够快速实现电极敏感膜的更新。利用磁性粒子作为载体, 制备易更新的分子印迹传感器备受关注[8~10]。自组装分子印迹技术[11]是指功能单体与模板分子之间通过非共价键作用(如氢键、静电力、疏水作用力、范德华力等)在溶液中自发的形成单体模板分子稳定复合物的方法,它结合了分子印迹和自组装技术的优点,已被众多学者研究[12]。
辛可宁(Cinchonin,CCN)是一种喹啉类生物碱,具有抗心律失常、抗疟等作用。但辛可宁使用不当,会引起人体中毒,出现头痛、晕眩、耳鸣、恶心、视力及听力减退等症状。目前对辛可宁的检测方法也有报导[13~17]。如文献[13]利用传统电聚合法制备的辛可宁分子印迹膜传感器的膜更新比较困难,且聚合物印迹膜较厚导致电子传递速率慢、传感器灵敏度不高。
本研究在Fe3O4@Au磁性纳米粒子表面自组装辛可宁分子印迹膜,利用辛可宁分子与底液中Ru(bpy)2+3发生共反应以增强其电致化学发光强度的原理,采用电化学发光(ECL)的方法实现对辛可宁的测定。此磁性粒子自组装分子印迹膜传感器不仅检测灵敏度较已报导的辛可宁传感器高,而且利用自组装方法所制备的分子印迹膜结构稳定有序,识别过程扩散阻碍少,响应快。此外,通过施加或移除外加磁场,实现电极表面的快速更新, 有效地克服了传统印迹方法中模板分子洗脱困难的缺点。
2 实验部分
2.1 仪器与试剂
MPIE型电致化学发光分析系统(西安瑞迈分析仪器有限责任公司); 电致化学发光采用三电极系统:工作电极为磁控玻碳电极,参比电极为Ag/AgCl(饱和KCl)电极,对电极为铂丝电极。Bransonic200 超声仪(德国Branson Ultraschall公司); pHS2C型精密酸度计(上海雷磁精密仪器有限公司); GS28B电子恒速搅拌器(上海安亭电子仪器厂); DK8B型电热恒温水槽(上海精宏实验设备有限公司)。
辛可宁(上海化学试剂站); 三联吡啶氯化钌六水合物(百灵威科技有限公司); 氯金酸(国药集团化学试剂有限公司); 硼砂缓冲液由0.01 mol/L H3BO3和0.1 mol/L NaOH配制。实验所用试剂均为分析纯。实验用水均为二次蒸馏水。
2.2 磁性纳米粒子Fe3O4@Au的制备
参照文献[18]方法合成Fe3O4@Au核壳结构的纳米微粒。称取适量FeCl3·6H2O和FeSO4·7H2O,以Fe3+/Fe2+=1∶2的摩尔比混合,并溶解在水中,50 ℃恒温水浴下高速搅拌,匀速加入适量NaOH,调节至pH 10后,升温至80 ℃继续搅拌1 h。整个实验均在 N2保护下进行。制备的黑色悬浮液超声20 min后,磁铁分离,用水反复洗涤,定容,于4 ℃保存备用。
取0.229 g柠檬酸钠溶解在100 mL水中,搅拌下加热,至99 ℃时迅速加入1 mL上述制备的磁性Fe3O4纳米粒子,搅拌片刻,加入5 mL 10 mmol/L氯金酸溶液,继续加热并搅拌15 min,移去热源后继续搅拌15 min,待浅棕红色溶液冷却到室温后,通过外加磁场进行分离,并用水清洗后定容到20 mL,得Fe3O4@Au贮备液,4 ℃保存备用。
2.3 磁性纳米粒子Fe3O4@Au表面自组装分子印迹膜及非分子印迹膜的制备
先将适量上述Fe3O4@Au溶液加入到5 mmol/L 辛可宁乙醇溶液中,超声振荡10 min,室温下静置12 h,确保辛可宁分子通过静电作用吸附到Fe3O4@Au纳米粒子表面; 接着,向上述混合液中加入15 μL十二烷基硫醇,摇匀,室温条件下自组装12 h; 最后,依次用甲醇乙酸(3∶1, V/V)溶液和水洗脱模板分子,即可在Fe3O4@Au表面得到自组装的辛可宁分子印迹膜(Molecularly imprinted membrane, MIM)。用同样的方法制备非分子印迹膜(nMIM),只是在制备过程中不添加模板分子辛可宁。
2.4 电致化学发光检测方法
电极在使用之前,先使用0.05 μm的Al2O3粉末研磨抛光电极表面,然后分别置于50%(V/V)HNO3、无水乙醇、水中超声清洗,晾干备用。
移取5 μL修饰了分子印迹膜的Fe3O4@Au,滴加到磁控玻碳电极表面,以此为工作电极。电化学发光检测是将电极置于不同浓度的辛可宁溶液中进行重吸附后,浸入到含有0.8 mmol/L三联吡啶钌的12 mmol/L硼砂缓冲液(pH=9.5)中,直接测定发光强度。电致化学发光参数设定为: 扫描电位为0.2~1.3 V,扫描速率为100 mV/s,光电倍增管高压为 900 V,放大级数为4级。
2.5 样品处理方法
志愿者的人体血清样品取自桂林理工大学医院。移取血清样本5 mL,加入5 mL过饱和(NH4)2SO4,搅拌5 min,3000 r/min 离心10 min,除去杂质蛋白,取上清液,于4 ℃保存备用。
3 结果与讨论
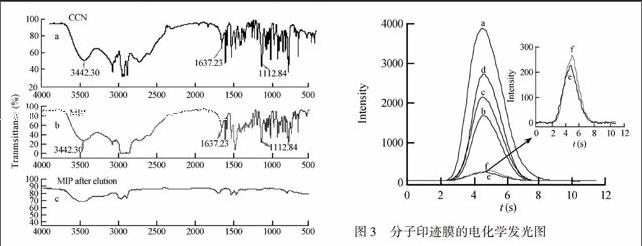
3.1 核壳型Fe3O4@Au磁性粒子的表征采用红外光谱法对分子印迹膜洗脱前后进行了表征。图2a为辛可宁的红外谱图,3442.30 cm 1为OH的伸缩振动峰,1637.23 cm 1为辛可宁中CN的伸缩振动峰,1112.84 cm 1为辛可宁CN的伸缩振动峰; 图2b为分子印迹膜的红外光谱图,分子印迹膜中含有辛可宁的特征峰,当洗脱模板分子辛可宁后,红外光谱中辛可宁的特征峰消失(图2c),由此可以证明,模板分子被成功移除。
3.2 传感器的电化学发光响应
电化学发光反应是利用辛可宁含有的叔氨基对Ru(bpy)2+3的电化学发光信号有增敏作用的原理对辛可宁进行检测。传感器在不同条件下的电化学发光信号见图3。由图3可知,修饰了分子印迹膜的电极,未洗脱模板分子时,发光强度较大(曲线a); 而洗脱模板分子后,发光强度明显减小(曲线b)。这是由于未洗脱模板分子前,膜内含有较多的辛可宁分子,其结构中的叔氨基能够有效增强Ru(bpy)2+3的发光强度; 而洗脱模板分子后,膜内几乎无辛可宁分子,从而使得发光强度明显减小。 对不同浓度的辛可宁进行重吸附,随着吸附辛可宁量的增加,Ru(bpy)2+3的发光强度逐渐增强(曲线c和d)。
反之, 对于非分子印迹膜电极来说(见图3插图)。在电极表面形成一层致密的非分子印迹膜时,由于nMIM电子传递阻碍大,且膜内无模板分子辛可宁,不能促进Ru(bpy)2+3发光,故发光强度极小(曲线e)。经洗脱处理后,发光强度几乎不变(曲线f)。可见洗脱前后nMIM中都不存在印迹位点。
3.3 缓冲溶液的优化
分别考察了PBS、TrisHCl和硼砂3种缓冲溶液对体系ECL响应的影响。结果表明,在硼砂缓冲溶液中,传感器的ECL响应最好。进一 步考察了不同pH硼砂缓冲液对体系ECL响应的影响。当硼砂缓冲溶液pH=9.5时,传感器的发光效果最好,故选择pH 9.5进行后续实验。同时还考察了硼砂缓冲液浓度对体系ECL响应的影响。结果表明,硼砂缓冲溶液浓度为12 mmol/L时, 体系ECL响应最高。
3.4 联吡啶钌浓度的影响
考察了Ru(bpy)2+3浓度对ECL响应强度的影响。在0.3~1.0 mmol/L范围内,当Ru(bpy)2+3浓度较低时,发光强度很弱,其原因可能是此时参与共反应的Ru(bpy)2+3不足,导致了发光强度较低、灵敏度不高的现象; 随着Ru(bpy)2+3浓度增加,发光强度不断增强,但当Ru(bpy)2+3浓度过高时,电化学反应中生成的不稳定中间体Ru(bpy)3+3也较多,从而导致基线不稳, 峰形变差,所以Ru(bpy)2+3 浓度选择为0.8 mmol/L。
3.6 分子印迹传感器的重现性和稳定性分析
用同一支传感器对7×10 9 mol/L辛可宁连续测定5次,电化学发光信号相对偏差为2.5%(浓度的相对标准偏差为2.6%); 同一批次的5支传感器对7×10 9 mol/L辛可宁进行测定,发光强度相对偏差为3.8%(浓度的相对标准偏差为3.9%),说明此传感器有较好的重现性。为考察传感器的稳定性,使传感器重吸附7×10 9 mol/L辛可宁溶液后,置于4 ℃下保存,定期检测电化学发光信号的变化。一星期内,电化学发光强度几乎不变,两星期之后,发光强度减少了4.7%,说明传感器的稳定性较好。
3.7 分子印迹传感器的特异识别性分析
为了研究传感器的特异性识别能力,考察了辛可宁结构类似物、血清样品中常见有机物质及常见离子对传感器选择性的影响。结果表明,200倍浓度的左旋咪唑; 100倍浓度的奎宁、奎宁丁、抗坏血酸、多巴胺、葡萄糖、色氨酸、苯丙氨酸以及不同浓度倍数的常见离子(表1)对传感器识别1×10 9 mol/L辛可宁的电化学发光响应信号变化影响小于5%,说明此传感器对辛可宁具有较好的特异性识别能力。此传感器敏感层的形成是将模板分子CCN通过静电作用吸附在Fe3O4@Au表面,加入十二烷基硫醇后,通过AuS键自组装在金壳表面,利用十二烷基硫醇与模板分子CCN之间的分子间作用力将印迹结构固定,洗脱模板分子CCN后,在印迹膜上留下与CCN结构及大小相互匹配的印迹位点,使得MIM对CCN产生特异性选择识别。
3.8 样品检测及回收率
按照实验方法,将传感器置于处理好的样品中进行重吸附,测定电化学发光信号,同时进行加标回收实验,结果如表2所示,方法的回收率为98.8%~104.7%,相对偏差小于2.7%。
结果表明, 此传感器制备过程简单、易更新、灵敏度高、选择性好,适用于血清样品中辛可宁的检测。
References
1 Yang G M, Zhao F Q, Zeng B Z. Biosens. Bioelectron., 2014, 53: 447-452
2 SHANG ZheYi, HAN ChaoFeng, SONG QiJun. Chinese J. Anal Chem., 2014, 42(6): 904-908
商哲一, 韩超峰, 宋启军. 分析化学, 2014, 42(6): 904-908
3 CHEN ZhiQiang, LI JianPing, LI YuPing. Chinese J. Anal. Chem., 2011, 39(7): 1009-1014
陈志强, 李建平, 李玉平. 分析化学, 2011, 39(7): 1009-1014
4 ZHAO Jun, LI JianPing, JIANG FuYang. Chinese J. Anal Chem., 2009, 37(8): 1219-1222
赵 钧, 李建平, 蒋复阳. 分析化学, 2009, 37(8): 1219-1222
5 Kan X W, Zhao Q, Zhang Z, Wang Z L, Zhu J J. Talanta, 2008, 75(1): 22-26
6 Ho K C, Yeh W M, Tung T S, Liao J Y.Anal. Chim. Acta, 2005, 542(1): 90-96
7 Sun H, Fung Y S. Anal. Chim. Acta, 2006, 576(1): 67-76
8 Liu B Q, Tang D P, Zhang B, Que X H, Yang H H, Chen G N . Biosens. Bioelectron., 2013, 41: 551-556
9 LI JianPing, GAO HuiLing, XIONG ZhiGang. Chem. J. Chinese Universities, 2008, 29(11): 2149-2154
李建平, 高会玲, 熊志刚. 高等学校化学学报, 2008, 29(11): 2149-2154
10 Li X, Zhang L M, Wei X P, Li J P. Electroanalysis, 2013, 25(5): 1286-1293
11 SHI RuiXue, GUO ChengHai, ZOU XiaoHong, ZHU ChunYe, ZUO YanJun, DENG YunDu. Prog. Chem., 2002, 14(3): 182-191
史瑞雪, 郭成海, 邹小红, 朱春野, 左言军, 邓云渡. 化学进展, 2002, 14(3): 182-191
12 Li X, Husson S M. Langmuir, 2006, 22(23): 9658-9663
13 LIU ZhiHang, HUAN ShuangYan, SHEN GuoLi, YU RuQin. Chem. J. Chinese Universities, 2005, 26(6): 1049-1051
刘志航, 宦双燕, 沈国励, 俞汝勤. 高等学校化学学报, 2005, 26(6):1049-1051
14 Yuan J B, Tan Y G, Nie L H, Yao S Z. Anal. Chim. Acta, 2002, 454(1): 65-74
15 Yang Y, Yang X, Yang H F, Liu Z M, Liu Y L, Shen G L, Yu R Q. Anal. Chim. Acta, 2005, 528(2): 135-142
16 Oliveri I P, Di Bella S. Tetrahedron, 2011, 67(48): 9446-9449
17 Lamalle C, Marini R D E A, Debrus B, Lebrun P, Crommen J, Hubert P, Servais A C, Fillet M. Electrophoresis, 2012, 33(11): 1669-1678
18 Li J P, Xu Q, Wei X P, Hao Z B. J. Agric. Food Chem., 2013, 61(7): 1435-1440
Abstract A molecularly imprinted electrochemiluminescence sensor for detection of cinchonine based on surface selfassembly of molecularly imprinted membrane on magnetic nanoparticles was developed. Cinchonine was used as template and lauryl mercaptan was used as assembling monomer. The morphology and particle size distribution of the magnetic nanoparticles were characterized by TEM, and the infrared spectroscopy was used to study the structure and composition of cinchonine, molecularly imprinted membrane before and after elution. The results showed that, cinchonine could be specifically assayed with a linear relationship between the signal intensity and the logarithm of concentrations of cinchonine in the range of 1×10 10 mol/L to 9×10 8 mol/L. The detection limit for cinchonine was 3.5×10 11mol/L. The sensor was used for the determination of cinchonine in serum samples, with the recoveries of 98.8% to 104.7%.
Keywords Molecular imprinted sensor; Magnetic nanoparticles; Cinchonine; Selfassemble; Electrochemiluminescence
(Received 2 August 2014; accepted 28 October 2014)
This work was supported by the National Natural Science Foundation of China (Nos. 21375031, 21165007)



摘 要 以辛可宁为模板分子、十二烷基硫醇为功能单体,在Fe3O4@Au纳米粒子表面自组装辛可宁分子印迹膜,构建了新型磁性粒子分子印迹电化学发光传感器。通过透射电子显微镜对磁性纳米粒子的粒径分布及形貌进行了表征,使用红外光谱对比分析了辛可宁、分子印迹膜洗脱前和洗脱后的结构及成分。结果表明,在最优的实验条件下(0.012 mol/L 硼砂缓冲溶液(pH 9.5),0.8 mmol/L Ru(bpy)2+3),辛可宁浓度的对数在1 × 10 10~9 × 10 8 mol/L范围内,与电化学发光强度变化值有良好的线性关系,检出限为3.5×10 11 mol/L。此传感器灵敏度高、选择性好、易于更新,将其用于血清样品的检测,方法回收率为98.8%~104.7%。
关键词 分子印迹传感器; 磁性纳米粒子; 辛可宁; 自组装; 电致化学发光
1 引 言
分子印迹传感器具有对目标分子专一识别的特性以及良好的机械稳定性和热稳定性,近年来受到越来越多研究者的关注[1~4]。分子印迹传感器的合成方法通常是使目标分子、功能单体以及交联剂三者之间发生三维聚合反应,经洗脱模板分子后,留下对目标分子具有较高选择性和亲和力的识别位点。然而,传统制备方法所得到的印迹传感器每次使用后需要进行印迹膜的更新,繁琐、费时,且重现性差[5~7]。
磁性Fe3O4纳米粒子不仅具有诸多纳米材料的优点,而且还具有超顺磁效应,在外加磁场的作用下,能够快速实现电极敏感膜的更新。利用磁性粒子作为载体, 制备易更新的分子印迹传感器备受关注[8~10]。自组装分子印迹技术[11]是指功能单体与模板分子之间通过非共价键作用(如氢键、静电力、疏水作用力、范德华力等)在溶液中自发的形成单体模板分子稳定复合物的方法,它结合了分子印迹和自组装技术的优点,已被众多学者研究[12]。
辛可宁(Cinchonin,CCN)是一种喹啉类生物碱,具有抗心律失常、抗疟等作用。但辛可宁使用不当,会引起人体中毒,出现头痛、晕眩、耳鸣、恶心、视力及听力减退等症状。目前对辛可宁的检测方法也有报导[13~17]。如文献[13]利用传统电聚合法制备的辛可宁分子印迹膜传感器的膜更新比较困难,且聚合物印迹膜较厚导致电子传递速率慢、传感器灵敏度不高。
本研究在Fe3O4@Au磁性纳米粒子表面自组装辛可宁分子印迹膜,利用辛可宁分子与底液中Ru(bpy)2+3发生共反应以增强其电致化学发光强度的原理,采用电化学发光(ECL)的方法实现对辛可宁的测定。此磁性粒子自组装分子印迹膜传感器不仅检测灵敏度较已报导的辛可宁传感器高,而且利用自组装方法所制备的分子印迹膜结构稳定有序,识别过程扩散阻碍少,响应快。此外,通过施加或移除外加磁场,实现电极表面的快速更新, 有效地克服了传统印迹方法中模板分子洗脱困难的缺点。
2 实验部分
2.1 仪器与试剂
MPIE型电致化学发光分析系统(西安瑞迈分析仪器有限责任公司); 电致化学发光采用三电极系统:工作电极为磁控玻碳电极,参比电极为Ag/AgCl(饱和KCl)电极,对电极为铂丝电极。Bransonic200 超声仪(德国Branson Ultraschall公司); pHS2C型精密酸度计(上海雷磁精密仪器有限公司); GS28B电子恒速搅拌器(上海安亭电子仪器厂); DK8B型电热恒温水槽(上海精宏实验设备有限公司)。
辛可宁(上海化学试剂站); 三联吡啶氯化钌六水合物(百灵威科技有限公司); 氯金酸(国药集团化学试剂有限公司); 硼砂缓冲液由0.01 mol/L H3BO3和0.1 mol/L NaOH配制。实验所用试剂均为分析纯。实验用水均为二次蒸馏水。
2.2 磁性纳米粒子Fe3O4@Au的制备
参照文献[18]方法合成Fe3O4@Au核壳结构的纳米微粒。称取适量FeCl3·6H2O和FeSO4·7H2O,以Fe3+/Fe2+=1∶2的摩尔比混合,并溶解在水中,50 ℃恒温水浴下高速搅拌,匀速加入适量NaOH,调节至pH 10后,升温至80 ℃继续搅拌1 h。整个实验均在 N2保护下进行。制备的黑色悬浮液超声20 min后,磁铁分离,用水反复洗涤,定容,于4 ℃保存备用。
取0.229 g柠檬酸钠溶解在100 mL水中,搅拌下加热,至99 ℃时迅速加入1 mL上述制备的磁性Fe3O4纳米粒子,搅拌片刻,加入5 mL 10 mmol/L氯金酸溶液,继续加热并搅拌15 min,移去热源后继续搅拌15 min,待浅棕红色溶液冷却到室温后,通过外加磁场进行分离,并用水清洗后定容到20 mL,得Fe3O4@Au贮备液,4 ℃保存备用。
2.3 磁性纳米粒子Fe3O4@Au表面自组装分子印迹膜及非分子印迹膜的制备
先将适量上述Fe3O4@Au溶液加入到5 mmol/L 辛可宁乙醇溶液中,超声振荡10 min,室温下静置12 h,确保辛可宁分子通过静电作用吸附到Fe3O4@Au纳米粒子表面; 接着,向上述混合液中加入15 μL十二烷基硫醇,摇匀,室温条件下自组装12 h; 最后,依次用甲醇乙酸(3∶1, V/V)溶液和水洗脱模板分子,即可在Fe3O4@Au表面得到自组装的辛可宁分子印迹膜(Molecularly imprinted membrane, MIM)。用同样的方法制备非分子印迹膜(nMIM),只是在制备过程中不添加模板分子辛可宁。
2.4 电致化学发光检测方法
电极在使用之前,先使用0.05 μm的Al2O3粉末研磨抛光电极表面,然后分别置于50%(V/V)HNO3、无水乙醇、水中超声清洗,晾干备用。
移取5 μL修饰了分子印迹膜的Fe3O4@Au,滴加到磁控玻碳电极表面,以此为工作电极。电化学发光检测是将电极置于不同浓度的辛可宁溶液中进行重吸附后,浸入到含有0.8 mmol/L三联吡啶钌的12 mmol/L硼砂缓冲液(pH=9.5)中,直接测定发光强度。电致化学发光参数设定为: 扫描电位为0.2~1.3 V,扫描速率为100 mV/s,光电倍增管高压为 900 V,放大级数为4级。
2.5 样品处理方法
志愿者的人体血清样品取自桂林理工大学医院。移取血清样本5 mL,加入5 mL过饱和(NH4)2SO4,搅拌5 min,3000 r/min 离心10 min,除去杂质蛋白,取上清液,于4 ℃保存备用。
3 结果与讨论
3.1 核壳型Fe3O4@Au磁性粒子的表征采用红外光谱法对分子印迹膜洗脱前后进行了表征。图2a为辛可宁的红外谱图,3442.30 cm 1为OH的伸缩振动峰,1637.23 cm 1为辛可宁中CN的伸缩振动峰,1112.84 cm 1为辛可宁CN的伸缩振动峰; 图2b为分子印迹膜的红外光谱图,分子印迹膜中含有辛可宁的特征峰,当洗脱模板分子辛可宁后,红外光谱中辛可宁的特征峰消失(图2c),由此可以证明,模板分子被成功移除。
3.2 传感器的电化学发光响应
电化学发光反应是利用辛可宁含有的叔氨基对Ru(bpy)2+3的电化学发光信号有增敏作用的原理对辛可宁进行检测。传感器在不同条件下的电化学发光信号见图3。由图3可知,修饰了分子印迹膜的电极,未洗脱模板分子时,发光强度较大(曲线a); 而洗脱模板分子后,发光强度明显减小(曲线b)。这是由于未洗脱模板分子前,膜内含有较多的辛可宁分子,其结构中的叔氨基能够有效增强Ru(bpy)2+3的发光强度; 而洗脱模板分子后,膜内几乎无辛可宁分子,从而使得发光强度明显减小。 对不同浓度的辛可宁进行重吸附,随着吸附辛可宁量的增加,Ru(bpy)2+3的发光强度逐渐增强(曲线c和d)。
反之, 对于非分子印迹膜电极来说(见图3插图)。在电极表面形成一层致密的非分子印迹膜时,由于nMIM电子传递阻碍大,且膜内无模板分子辛可宁,不能促进Ru(bpy)2+3发光,故发光强度极小(曲线e)。经洗脱处理后,发光强度几乎不变(曲线f)。可见洗脱前后nMIM中都不存在印迹位点。
3.3 缓冲溶液的优化
分别考察了PBS、TrisHCl和硼砂3种缓冲溶液对体系ECL响应的影响。结果表明,在硼砂缓冲溶液中,传感器的ECL响应最好。进一 步考察了不同pH硼砂缓冲液对体系ECL响应的影响。当硼砂缓冲溶液pH=9.5时,传感器的发光效果最好,故选择pH 9.5进行后续实验。同时还考察了硼砂缓冲液浓度对体系ECL响应的影响。结果表明,硼砂缓冲溶液浓度为12 mmol/L时, 体系ECL响应最高。
3.4 联吡啶钌浓度的影响
考察了Ru(bpy)2+3浓度对ECL响应强度的影响。在0.3~1.0 mmol/L范围内,当Ru(bpy)2+3浓度较低时,发光强度很弱,其原因可能是此时参与共反应的Ru(bpy)2+3不足,导致了发光强度较低、灵敏度不高的现象; 随着Ru(bpy)2+3浓度增加,发光强度不断增强,但当Ru(bpy)2+3浓度过高时,电化学反应中生成的不稳定中间体Ru(bpy)3+3也较多,从而导致基线不稳, 峰形变差,所以Ru(bpy)2+3 浓度选择为0.8 mmol/L。
3.6 分子印迹传感器的重现性和稳定性分析
用同一支传感器对7×10 9 mol/L辛可宁连续测定5次,电化学发光信号相对偏差为2.5%(浓度的相对标准偏差为2.6%); 同一批次的5支传感器对7×10 9 mol/L辛可宁进行测定,发光强度相对偏差为3.8%(浓度的相对标准偏差为3.9%),说明此传感器有较好的重现性。为考察传感器的稳定性,使传感器重吸附7×10 9 mol/L辛可宁溶液后,置于4 ℃下保存,定期检测电化学发光信号的变化。一星期内,电化学发光强度几乎不变,两星期之后,发光强度减少了4.7%,说明传感器的稳定性较好。
3.7 分子印迹传感器的特异识别性分析
为了研究传感器的特异性识别能力,考察了辛可宁结构类似物、血清样品中常见有机物质及常见离子对传感器选择性的影响。结果表明,200倍浓度的左旋咪唑; 100倍浓度的奎宁、奎宁丁、抗坏血酸、多巴胺、葡萄糖、色氨酸、苯丙氨酸以及不同浓度倍数的常见离子(表1)对传感器识别1×10 9 mol/L辛可宁的电化学发光响应信号变化影响小于5%,说明此传感器对辛可宁具有较好的特异性识别能力。此传感器敏感层的形成是将模板分子CCN通过静电作用吸附在Fe3O4@Au表面,加入十二烷基硫醇后,通过AuS键自组装在金壳表面,利用十二烷基硫醇与模板分子CCN之间的分子间作用力将印迹结构固定,洗脱模板分子CCN后,在印迹膜上留下与CCN结构及大小相互匹配的印迹位点,使得MIM对CCN产生特异性选择识别。
3.8 样品检测及回收率
按照实验方法,将传感器置于处理好的样品中进行重吸附,测定电化学发光信号,同时进行加标回收实验,结果如表2所示,方法的回收率为98.8%~104.7%,相对偏差小于2.7%。
结果表明, 此传感器制备过程简单、易更新、灵敏度高、选择性好,适用于血清样品中辛可宁的检测。
References
1 Yang G M, Zhao F Q, Zeng B Z. Biosens. Bioelectron., 2014, 53: 447-452
2 SHANG ZheYi, HAN ChaoFeng, SONG QiJun. Chinese J. Anal Chem., 2014, 42(6): 904-908
商哲一, 韩超峰, 宋启军. 分析化学, 2014, 42(6): 904-908
3 CHEN ZhiQiang, LI JianPing, LI YuPing. Chinese J. Anal. Chem., 2011, 39(7): 1009-1014
陈志强, 李建平, 李玉平. 分析化学, 2011, 39(7): 1009-1014
4 ZHAO Jun, LI JianPing, JIANG FuYang. Chinese J. Anal Chem., 2009, 37(8): 1219-1222
赵 钧, 李建平, 蒋复阳. 分析化学, 2009, 37(8): 1219-1222
5 Kan X W, Zhao Q, Zhang Z, Wang Z L, Zhu J J. Talanta, 2008, 75(1): 22-26
6 Ho K C, Yeh W M, Tung T S, Liao J Y.Anal. Chim. Acta, 2005, 542(1): 90-96
7 Sun H, Fung Y S. Anal. Chim. Acta, 2006, 576(1): 67-76
8 Liu B Q, Tang D P, Zhang B, Que X H, Yang H H, Chen G N . Biosens. Bioelectron., 2013, 41: 551-556
9 LI JianPing, GAO HuiLing, XIONG ZhiGang. Chem. J. Chinese Universities, 2008, 29(11): 2149-2154
李建平, 高会玲, 熊志刚. 高等学校化学学报, 2008, 29(11): 2149-2154
10 Li X, Zhang L M, Wei X P, Li J P. Electroanalysis, 2013, 25(5): 1286-1293
11 SHI RuiXue, GUO ChengHai, ZOU XiaoHong, ZHU ChunYe, ZUO YanJun, DENG YunDu. Prog. Chem., 2002, 14(3): 182-191
史瑞雪, 郭成海, 邹小红, 朱春野, 左言军, 邓云渡. 化学进展, 2002, 14(3): 182-191
12 Li X, Husson S M. Langmuir, 2006, 22(23): 9658-9663
13 LIU ZhiHang, HUAN ShuangYan, SHEN GuoLi, YU RuQin. Chem. J. Chinese Universities, 2005, 26(6): 1049-1051
刘志航, 宦双燕, 沈国励, 俞汝勤. 高等学校化学学报, 2005, 26(6):1049-1051
14 Yuan J B, Tan Y G, Nie L H, Yao S Z. Anal. Chim. Acta, 2002, 454(1): 65-74
15 Yang Y, Yang X, Yang H F, Liu Z M, Liu Y L, Shen G L, Yu R Q. Anal. Chim. Acta, 2005, 528(2): 135-142
16 Oliveri I P, Di Bella S. Tetrahedron, 2011, 67(48): 9446-9449
17 Lamalle C, Marini R D E A, Debrus B, Lebrun P, Crommen J, Hubert P, Servais A C, Fillet M. Electrophoresis, 2012, 33(11): 1669-1678
18 Li J P, Xu Q, Wei X P, Hao Z B. J. Agric. Food Chem., 2013, 61(7): 1435-1440
Abstract A molecularly imprinted electrochemiluminescence sensor for detection of cinchonine based on surface selfassembly of molecularly imprinted membrane on magnetic nanoparticles was developed. Cinchonine was used as template and lauryl mercaptan was used as assembling monomer. The morphology and particle size distribution of the magnetic nanoparticles were characterized by TEM, and the infrared spectroscopy was used to study the structure and composition of cinchonine, molecularly imprinted membrane before and after elution. The results showed that, cinchonine could be specifically assayed with a linear relationship between the signal intensity and the logarithm of concentrations of cinchonine in the range of 1×10 10 mol/L to 9×10 8 mol/L. The detection limit for cinchonine was 3.5×10 11mol/L. The sensor was used for the determination of cinchonine in serum samples, with the recoveries of 98.8% to 104.7%.
Keywords Molecular imprinted sensor; Magnetic nanoparticles; Cinchonine; Selfassemble; Electrochemiluminescence
(Received 2 August 2014; accepted 28 October 2014)
This work was supported by the National Natural Science Foundation of China (Nos. 21375031, 21165007)

