对样品中粗蛋白测定的商榷
胡爱军+蔡小玲
摘要:KDN-04(08)A、C、D定氮仪为粮食、饲料、乳品、土肥、化工、医药、商检样品的理想检测设备,与传统的仲裁法测定样品粗蛋白方法相比,具有速度快,准确率高,安全简单易操作等优点。
关键词:取样;消化;蒸馏;滴定;计算
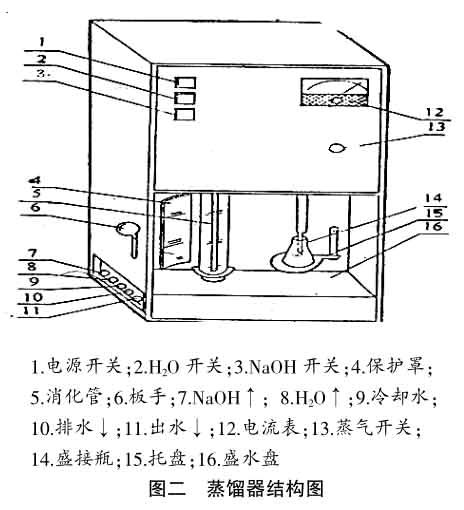
KDN-04(08)A、C、D定氮仪为粮食、饲料、乳品、土肥、化工、医药、商检样品的理想检测设备,与传统的仲裁法测定样品粗蛋白方法相比,具有速度快,准确率高,安全简单易操作等优点。KDN型定氮仪检测整套装置,由消化器(见图一)、蒸馏器(见图二)两大部分组成。提高蛋白质含量测定的检测速度,关键要加速样品消化的时间。KDN系列定氮仪消化装置,由于采用井式电加热方式,增大了消化管受热面,使消化样品在消化管内取得最佳的消化效果。如果使用硒片作为催化剂可进一步加速消化煮解,大大缩短了消化时间。消化时产生的SO2等有害气体,通过消化炉上的排污管经过抽气泵把气体融合在水中排入下水道,有效的抑制有害气体的外逸,又省去实验中安装毒气通风柜。试样经过40分钟的消化,即能完全消化。自来水进入蒸馏器,经稳压器流入蒸发炉,因水位的上升碰到电极产生电流,快速加热产生蒸汽,对已消化完全的样品进行蒸馏,将蒸馏过程中产生的硫酸铵转化成铵并与硼酸反应生成硼酸氢铵。然后经滴定计算蛋白质含量,滴定的过程是盐酸(或硫酸)和硼酸氢铵反应的过程。澧县农产品质量安全检测中心在样品中粗蛋白测定上进行一些探索,现将工作中的体会与质检工作者作些商讨交流。
一、KDN-04 (08) A、C、D定氮仪技术参数
1.测定品种:粮食、饲料、食品、乳制品、土肥、医药;
2.测定范围:含氮量0.05%-90%;
3.精度:相对差≤2%,平行差≤0.2%;
4.测定时间:消化45分钟左右(视样品含氮量而定,催化剂用硫酸铜、硫酸钾则需2.5小时),蒸馏6分钟左右;
5.电源:AC220V/50HZ;
6.功率:消化器(四孔)1200W(八孔)2400W;
7.体积:04消化器650×220×150
08消化器730×300×150;
蒸馏器380×330×740单位(mm),1000Kw;
二、操作过程
1.选取具有代表性的试样用四分法缩减至200g,粉碎后全部通过40目筛,装于密封容器内,防止试样成分变化。
2.混合催化剂:2g硫酸铜加上30g硫酸钾,磨碎混匀。(或用35g硒粉代替)
3.称取0.5g试样,精确至0.0002g,,放入消化管内,加上6.4g混合催化剂与试样混合,加入10ml的浓硫酸和2粒玻璃珠,将消化管分别放入各个消化架各个孔内,然后置于消化器上,放上已经装好密封圈的排污管,打开抽气三通进水(自来水)使抽气通处于吸气状态,在接通电源,打开各自控制开关,转动电位器,调节电压指示220v,使其快速消化。消化结束后(一般2.5小时),消化管及排污管和整个托架一起移到冷却架上进行冷却。注意:在冷却过程中,排污管必须保持吸气状态(千万不能将消化管放入水中冷却)防止废气逸出。
4.混合指示剂:0.05g甲基红加上50ml乙醇混匀后为0.1%的甲基红乙醇溶液,0.25g溴甲酚绿加上50ml乙醇混匀后为0.5%溴甲酚绿乙醇溶液,然后把两溶液等体积混合,在阴凉处保存期为三个月。
5.配制0.1mol的硫酸标准滴定液:3ml硫酸缓缓的注入1000ml去离子水中,冷却,摇匀。
6. 0.1mol的硫酸标准滴定液的标定:称取0.2g无水碳酸钠(270℃-300℃的高温炉中灼烧),溶于50ml水中,加入10滴溴甲酚绿-甲基红指示剂,用配制好的硫酸溶液滴定至溶液由绿色变成暗红色,记住加了多少毫升,然后煮沸2分钟,冷却后继续滴定至溶液再呈暗红色,记住加了多少毫升,两次的和为V1,同时做空白试验,代入公式:
C=m×1000/〔(V1-V2)M〕
M为无水碳酸钠的摩尔质量的数值,为52.994
m为无水碳酸钠的质量的准确数值,单位为g
7.40%氢氧化钠水溶液(M∕V):20g氢氧化钠加上50ml蒸馏水混匀。
8.2%硼酸水溶液(M∕V):2g硼酸加上100ml蒸馏水混匀。
9.打开定氮仪的开关,关掉排水阀打开自来水,打开面板蒸汽开关,水位达到后蒸汽开关的灯会自动亮,这时关掉自来水,打开冷却水龙头,仪器进入自动加热状态,直到蒸汽喷出来为止(再喷半分钟)。关掉蒸汽开关,把接收液(25ml硼酸加上2滴溴甲酚绿———甲基红指示剂)的三角烧瓶放到大圆盘上,接收管浸入液面。
10.把消化好的样品的消化管与蒸馏器连接,稍加旋转使其密封后打开蒸馏水开关H2O加蒸馏水20ml,关掉开关,再打开NaOH开关加50mlNaOH,关闭NaOH开关。打开蒸汽开关,仪器进入正常工作状态,当三角烧瓶的接收液满150ml,下移三角烧瓶继续蒸馏半分钟。关闭蒸汽开关,倒掉消化管内废液,进行滴定计算。
三、讨论
1.如果开机电源指示灯不亮,检查电源插头和15A熔丝管,请必须使用良好接地的三眼插座。
2.消化时如有气体外逸,加大三通抽气泵的进水量。在消化初始阶段,需注意观察防止试样因急速加热而飞溅。缓解办法可在消化过程,当发现试样飞溅时关机5分钟后再开机继续加热。
3.如果开机后电流上升中,指示灯突然不亮,请先切断电源,检查熔丝管是否损坏(如损坏,应更换15A熔丝管),然后关闭冷却水,打开排水阀和蒸汽开关进行排水,故障排除后重新开机操作。冷却水接口必须连接自来水,其他水源不能使用(如蒸馏水或经过处理后的深井水),如果其他水源的话,仪器内蒸发炉因不导电引起仪器不能加热,仪器将无法工作。开机前先观察仪器右侧面下部蒸发炉内水位,应不能超过电极底部。(如果超过请先排水,否则很容易造成仪器损坏,操作时应先关闭冷却水,再打开排水阀和蒸汽开关,然后排水。)打开面板上“蒸汽”开关,机器开始自动加热,加热期间请注意观察面板上电流表指针是否有电流指示(如果没有电流指示,表示仪器没有加热或加热功率很小,其原因为可能水质有问题),直到蒸汽从前下方蒸馏塑管内喷出,让其喷半分钟左右。关掉蒸汽开关,仪器进入待机状态。(如果待机时间过长,蒸馏前应先开一下蒸汽开关,待蒸汽喷出后再关掉蒸汽开关)接收液取下(在取下接收瓶时,用少量蒸馏水冲洗导出管前端,洗液与吸收液合并),关掉蒸汽开关,倒掉蒸馏完的废液仪器还原到待机状态,接收液待滴定之用。
4.如果开机后自来水不能正常进水蒸发炉(右下方有一个观察窗口)请用手挤压出水口胶管或打开后盖挤压稳压器连接到蒸发炉的橡胶管
(可能橡胶管内有空气)。使水正常流入蒸发炉内进行加热。
5.如果打开水泵或碱泵有工作声音,但不出液体,检查仪器内部单向阀是否连接,消除方法是拔掉单向阀一头橡胶管,用硬物使单向阀中间蓝色维体活动即可。如果水泵或碱泵没有工作声音时,应检查2A保险丝是否断裂。
6.试验做完后,冷却水不能关,每天工作结束后,清洗碱泵,方法如下:碱液管从容器中取出,放入蒸馏水容器内(蒸馏水必须在40℃左右)的温水中然后在蒸馏器前放上一只空的消化管,打开NaOH开关,抽取200ml蒸馏水(温水)2-3次清洗完成,保证使用寿命,尽量减少碱泵因结晶而无法使用。
7.KDN系列定氮仪采用凯氏定氮的原理进行测定,但是不同的样品,实际含氮量也有区别。所以,不同的样品必须采用不同的换算系数。如花生、大豆、蚕豆、大麦小麦、燕麦等的含氮量为17.6%,求得K=5.7;荞麦、葵花籽、亚麻籽、棉花籽、蓖麻子等换算系数则为K=5.5;玉米菜籽则为6.0;水稻为5.95,上述以外的其他样品换算系数均适用6.25,在计算公式中A也就不一样。
蛋白含量(%)=[(V1-V2)C×0.014×A×100]/W
公式中:V1-消耗盐酸(或硫酸)的毫升数
V2-空白实验时消耗盐酸(或硫酸)的毫升数
C-盐酸(或硫酸)的当量浓度
0.014-1ml盐酸(或硫酸)的当量数
A-A固定系数(6.25,5.7等)
W-试样重量g
空白测定:用0.1克糖代替样品或不加样品作空白测定。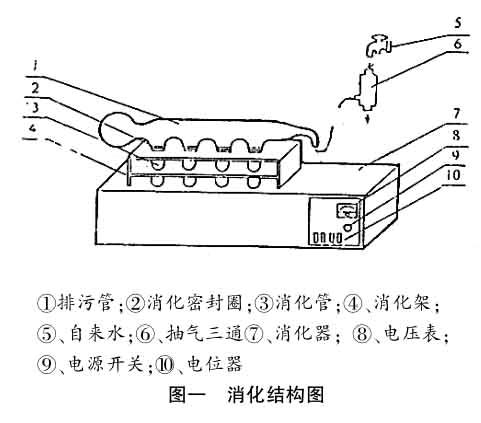
摘要:用高效液相色谱法对饲料中维生素D3的检测过程中,BHT(2,6-二叔丁基对甲酚)对测定会产生影响。当维生素D3含量较低或检测人员经验不足时,检测峰易发生误判,造成检测结果的偏离。从BHT结构和实验入手,对检测过程进行优化,可消除BHT对饲料中维生素D3检测的影响,达到准确定性和准确定量的目的。
关键词:维生素D3;高效液相色谱仪;抗氧化剂;准确定量
维生素D3是维持机体正常活动必不可少的物质,常用于维生素D缺乏症的预防与治疗,适量的各种维生素D3作为饲料添加剂能促进禽畜生长,增强禽畜体质,产生显著的经济效益。
饲料中维生素D3的检测一般是按照GB/T 17818-2010进行,但是在分析检测过程中,经常会有饲料中维生素D3超过标准值的情况,在排除了企业添加值错误的情况外,本文首次发现了在检测过程中添加的抗氧化剂BHT对维生素D3含量测定结果产生的影响,并且对其进行了详细的讨论,达到了准确定量饲料中维生素D3的目的。
1.实验部分
1.1 实验仪器与试剂
高效液相色谱仪:岛津;电子分析天平(德国梅特勒);氮吹仪;圆底烧瓶(带回流冷凝器);电热套;抗坏血酸;乙醇;氢氧化钾;乙醚;氯化钠;BHT(2,6-二叔丁基对甲酚)。
1.2 样品前处理
称取样品10g,精确至0.0001g,置于250mL圆底烧瓶中,加入50mL L-抗坏血酸乙醇溶液,10mL氢氧化钾溶液,混合均匀,沸水浴上回流30min皂化。
皂化完成后,皂化液转移至装有50mL乙醚的250mL分液漏斗中提取,再分别用40mL、30mL乙醚重复提取2次,弃去水相,合并三次乙醚相。用氯化钠溶液50mL洗涤一次,弃去水相,再用50mL水洗涤乙醚提取液至中性。乙醚提取液用无水硫酸钠脱水,转移到100mL棕色容量瓶中,加入100mgBHT使之溶解,用乙醚定容至刻度。
取5.0mL乙醚溶液,氮气吹干,用甲醇定容至1.0mL,高效液相色谱仪分析。
1.3 色谱条件
色谱柱:C18 5μm 150×4.6 mm,流动相:甲醇:水=95:5,流速:1.0 mL/min,柱温:30℃,进样量:20.0μL,波长:264 nm
2.结果讨论
2.1 结果影响
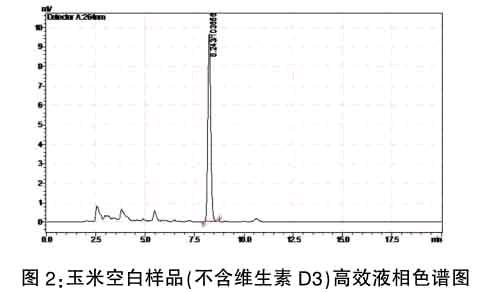
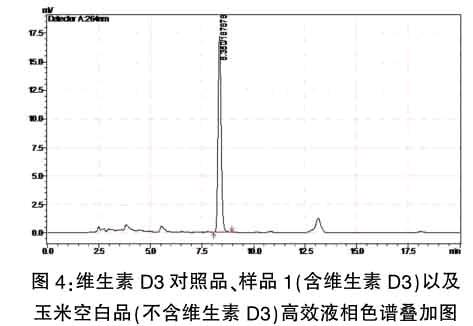
实际测定中,我们发现,在1.3色谱条件下,维生素D3的含量普遍比标示含量偏高,而且在空白基质中,在与维生素D3对照品同一保留时间出现了强吸收峰,而且面积比较大,见图2,与维生素D3对照品检测重叠,对饲料中维生素D3的检测产生影响,具体谱图见图1-图4。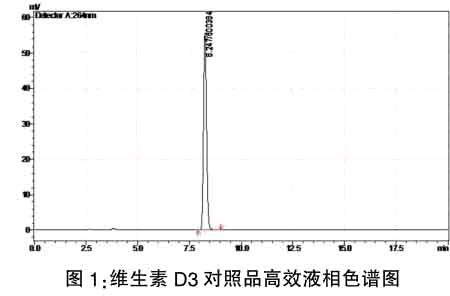
2.2 影响因素分析验证
通过对样品的分析过程进行拆解,对可能存在的影响因子一一进行排查,最后确定,用GB/T 17818-2010方法对样品进行分析检测,是BHT对整个的分析结果产生了影响。
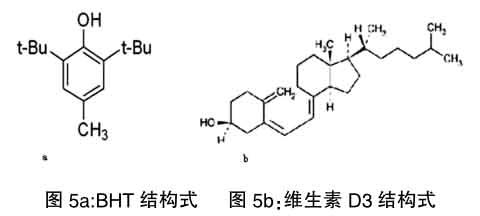
2.2.1BHT结构剖析验证
维生素D3对光、热不稳定,在空气中容易氧化,光化成前反式维生素D3和后维生素D3等产物而失去活性。在实际测定中,加入BHT抗氧化剂,可防止其氧化。
在维生素D3提取过程中,在最后一步加入了抗氧化剂BHT,对其结构进行分析后发现BHT结构与维生素D3有相似的紫外吸收基团(具体结构式见图5)。维生素D3在264nm下,有较强的吸收。而BHT由于具有苯环结构,因此在由苯环共轭系统下π-π※跃迁产生B带特征吸收在254nm下有较强的吸收,又由于在BHT结构中,苯环上面有羟基,作为助色基团,会导致BHT最大特征吸收波长发生红移,因此BHT最大吸收波长会大于254nm,因此,可以考虑,在图2空白玉米样中,出现与维生素D3相同保留时间下出现的物质,是BHT带来的干扰
2.2.2 BHT的影响实验验证
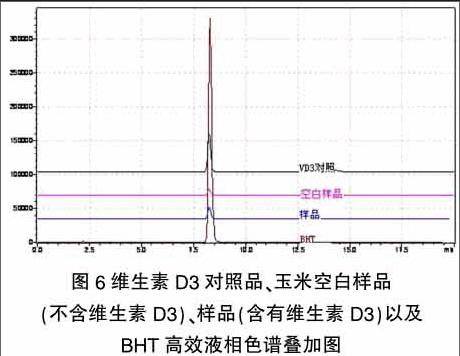
介于BHT对维生素D3分析可能存在的影响,称取一定量的BHT,用甲醇溶解,按照1.3中色谱条件,进行分析,色谱图见图6.
从图6中可以看出,维生素D3对照品以及样品和单独的BHT在保留时间都为8.45min,因此可以证明,BHT对维生素D3含量的测定产生了影响,在图2中也得到了验证。在图3样品中出现的色谱峰物质,不完全是样品中维生素D3,而是维生素D3与BHT叠加后得到的色谱吸收峰。因此,在GB/T 17818-2010方法下,如果单纯的以保留时间作为维生素D3检测峰的话,对测定结果会产生很大的影响。
2.3 BHT影响的解决方法
2.3.1流动相的优化
为消除BHT的干扰,我们尝试更改有机相比例。
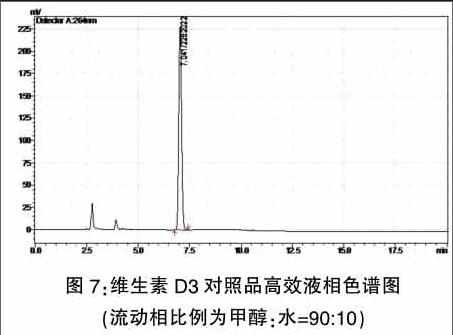
2.3.1.1调整流动相比例为90:10
当减小有机相甲醇的比例,调整为甲醇:水为
2.3.1.2调整流动相比例为98:2
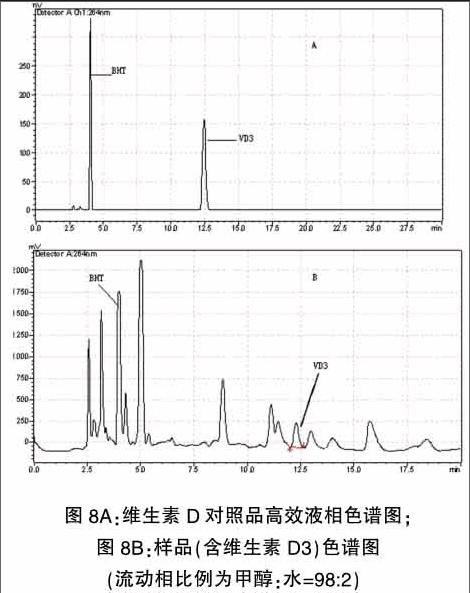
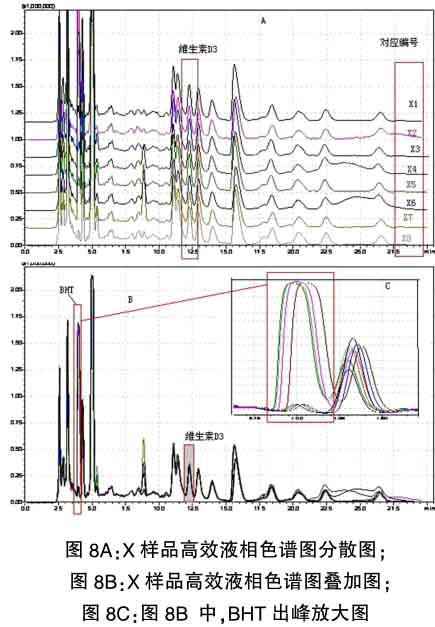
更改流动相有机相比例为98:2时,发现此时维生素D3对照品和BHT能够彻底分开,见图8A;样品中的VD3和BHT也能完全的分开,见图8B,可排除BHT对维生素D3检测的干扰。
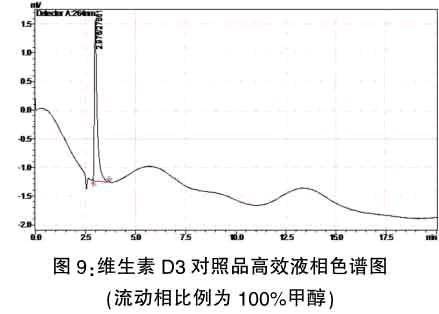
2.3.1.3调整流动相比例为100%甲醇
继续调整流动相比列为100%甲醇,我们发现,此时维生素D3对照品和BHT均无显著相应,具体情况见图9。
2.3.2BHT的添加及放置时间影响剖析
介于BHT对维生素D3存在的影响,本文取同一样品X,平行称取两份,X1样品按照1.2前处理方法进行前处理检测,X2样品亦按照1.2前处理方法进行前处理,但最后一步,X2样品定容时不加BHT,分别于4℃条件下放置0天(样品编号X1、X2)、3天(样品编号X3、X4)、7天(样品编号X5、X6)、15天(样品编号X7、X8),然后以2.3.1.3的色谱条件对其进行高效液相色谱检测分析,具体实验设计见表1。
从图8A中,可以看出,X样品在未加BHT的情况下,放置3天、7天以及15天的情况下,样品中维生素D3的含量与其加入BHT检测后的结果是基本不变的,也就是说,在检测饲料样品中的维生素D3时,半个月之内检测完毕,为了防止BHT对维生素D3的结果产生影响,是完全可以不添加BHT的。
3结论
本文首次发现了在检测过程中添加的抗氧化剂BHT对维生素D3含量测定产生的影响,并且从结构剖析方面以及单独的实验对其进行了验证,优化流动相比例,对其进行分离,同时对于检测过程中,BHT的添加与否在不同时间内对饲料中维生素D3含量测定的影响进行了详细的讨论。最后确定,在饲料中维生素D3的检测过程中,流动相的比例优化为98:2时,BHT与维生素D3可以有效的分离;其次,为避免BHT在检测过程中产生的干扰,在放置15天以内进行检测,不加BHT进行检测,亦可得到准确的结果,排除了BHT对其的影响,达到了准确定量饲料中维生素D3含量的目的,但由于维生素D3的前处理方法比较复杂,如何能够更快速有效的检测其含量还有待进一步研究。
参考文献(略)



摘要:KDN-04(08)A、C、D定氮仪为粮食、饲料、乳品、土肥、化工、医药、商检样品的理想检测设备,与传统的仲裁法测定样品粗蛋白方法相比,具有速度快,准确率高,安全简单易操作等优点。
关键词:取样;消化;蒸馏;滴定;计算
KDN-04(08)A、C、D定氮仪为粮食、饲料、乳品、土肥、化工、医药、商检样品的理想检测设备,与传统的仲裁法测定样品粗蛋白方法相比,具有速度快,准确率高,安全简单易操作等优点。KDN型定氮仪检测整套装置,由消化器(见图一)、蒸馏器(见图二)两大部分组成。提高蛋白质含量测定的检测速度,关键要加速样品消化的时间。KDN系列定氮仪消化装置,由于采用井式电加热方式,增大了消化管受热面,使消化样品在消化管内取得最佳的消化效果。如果使用硒片作为催化剂可进一步加速消化煮解,大大缩短了消化时间。消化时产生的SO2等有害气体,通过消化炉上的排污管经过抽气泵把气体融合在水中排入下水道,有效的抑制有害气体的外逸,又省去实验中安装毒气通风柜。试样经过40分钟的消化,即能完全消化。自来水进入蒸馏器,经稳压器流入蒸发炉,因水位的上升碰到电极产生电流,快速加热产生蒸汽,对已消化完全的样品进行蒸馏,将蒸馏过程中产生的硫酸铵转化成铵并与硼酸反应生成硼酸氢铵。然后经滴定计算蛋白质含量,滴定的过程是盐酸(或硫酸)和硼酸氢铵反应的过程。澧县农产品质量安全检测中心在样品中粗蛋白测定上进行一些探索,现将工作中的体会与质检工作者作些商讨交流。
一、KDN-04 (08) A、C、D定氮仪技术参数
1.测定品种:粮食、饲料、食品、乳制品、土肥、医药;
2.测定范围:含氮量0.05%-90%;
3.精度:相对差≤2%,平行差≤0.2%;
4.测定时间:消化45分钟左右(视样品含氮量而定,催化剂用硫酸铜、硫酸钾则需2.5小时),蒸馏6分钟左右;
5.电源:AC220V/50HZ;
6.功率:消化器(四孔)1200W(八孔)2400W;
7.体积:04消化器650×220×150
08消化器730×300×150;
蒸馏器380×330×740单位(mm),1000Kw;
二、操作过程
1.选取具有代表性的试样用四分法缩减至200g,粉碎后全部通过40目筛,装于密封容器内,防止试样成分变化。
2.混合催化剂:2g硫酸铜加上30g硫酸钾,磨碎混匀。(或用35g硒粉代替)
3.称取0.5g试样,精确至0.0002g,,放入消化管内,加上6.4g混合催化剂与试样混合,加入10ml的浓硫酸和2粒玻璃珠,将消化管分别放入各个消化架各个孔内,然后置于消化器上,放上已经装好密封圈的排污管,打开抽气三通进水(自来水)使抽气通处于吸气状态,在接通电源,打开各自控制开关,转动电位器,调节电压指示220v,使其快速消化。消化结束后(一般2.5小时),消化管及排污管和整个托架一起移到冷却架上进行冷却。注意:在冷却过程中,排污管必须保持吸气状态(千万不能将消化管放入水中冷却)防止废气逸出。
4.混合指示剂:0.05g甲基红加上50ml乙醇混匀后为0.1%的甲基红乙醇溶液,0.25g溴甲酚绿加上50ml乙醇混匀后为0.5%溴甲酚绿乙醇溶液,然后把两溶液等体积混合,在阴凉处保存期为三个月。
5.配制0.1mol的硫酸标准滴定液:3ml硫酸缓缓的注入1000ml去离子水中,冷却,摇匀。
6. 0.1mol的硫酸标准滴定液的标定:称取0.2g无水碳酸钠(270℃-300℃的高温炉中灼烧),溶于50ml水中,加入10滴溴甲酚绿-甲基红指示剂,用配制好的硫酸溶液滴定至溶液由绿色变成暗红色,记住加了多少毫升,然后煮沸2分钟,冷却后继续滴定至溶液再呈暗红色,记住加了多少毫升,两次的和为V1,同时做空白试验,代入公式:
C=m×1000/〔(V1-V2)M〕
M为无水碳酸钠的摩尔质量的数值,为52.994
m为无水碳酸钠的质量的准确数值,单位为g
7.40%氢氧化钠水溶液(M∕V):20g氢氧化钠加上50ml蒸馏水混匀。
8.2%硼酸水溶液(M∕V):2g硼酸加上100ml蒸馏水混匀。
9.打开定氮仪的开关,关掉排水阀打开自来水,打开面板蒸汽开关,水位达到后蒸汽开关的灯会自动亮,这时关掉自来水,打开冷却水龙头,仪器进入自动加热状态,直到蒸汽喷出来为止(再喷半分钟)。关掉蒸汽开关,把接收液(25ml硼酸加上2滴溴甲酚绿———甲基红指示剂)的三角烧瓶放到大圆盘上,接收管浸入液面。
10.把消化好的样品的消化管与蒸馏器连接,稍加旋转使其密封后打开蒸馏水开关H2O加蒸馏水20ml,关掉开关,再打开NaOH开关加50mlNaOH,关闭NaOH开关。打开蒸汽开关,仪器进入正常工作状态,当三角烧瓶的接收液满150ml,下移三角烧瓶继续蒸馏半分钟。关闭蒸汽开关,倒掉消化管内废液,进行滴定计算。
三、讨论
1.如果开机电源指示灯不亮,检查电源插头和15A熔丝管,请必须使用良好接地的三眼插座。
2.消化时如有气体外逸,加大三通抽气泵的进水量。在消化初始阶段,需注意观察防止试样因急速加热而飞溅。缓解办法可在消化过程,当发现试样飞溅时关机5分钟后再开机继续加热。
3.如果开机后电流上升中,指示灯突然不亮,请先切断电源,检查熔丝管是否损坏(如损坏,应更换15A熔丝管),然后关闭冷却水,打开排水阀和蒸汽开关进行排水,故障排除后重新开机操作。冷却水接口必须连接自来水,其他水源不能使用(如蒸馏水或经过处理后的深井水),如果其他水源的话,仪器内蒸发炉因不导电引起仪器不能加热,仪器将无法工作。开机前先观察仪器右侧面下部蒸发炉内水位,应不能超过电极底部。(如果超过请先排水,否则很容易造成仪器损坏,操作时应先关闭冷却水,再打开排水阀和蒸汽开关,然后排水。)打开面板上“蒸汽”开关,机器开始自动加热,加热期间请注意观察面板上电流表指针是否有电流指示(如果没有电流指示,表示仪器没有加热或加热功率很小,其原因为可能水质有问题),直到蒸汽从前下方蒸馏塑管内喷出,让其喷半分钟左右。关掉蒸汽开关,仪器进入待机状态。(如果待机时间过长,蒸馏前应先开一下蒸汽开关,待蒸汽喷出后再关掉蒸汽开关)接收液取下(在取下接收瓶时,用少量蒸馏水冲洗导出管前端,洗液与吸收液合并),关掉蒸汽开关,倒掉蒸馏完的废液仪器还原到待机状态,接收液待滴定之用。
4.如果开机后自来水不能正常进水蒸发炉(右下方有一个观察窗口)请用手挤压出水口胶管或打开后盖挤压稳压器连接到蒸发炉的橡胶管
(可能橡胶管内有空气)。使水正常流入蒸发炉内进行加热。
5.如果打开水泵或碱泵有工作声音,但不出液体,检查仪器内部单向阀是否连接,消除方法是拔掉单向阀一头橡胶管,用硬物使单向阀中间蓝色维体活动即可。如果水泵或碱泵没有工作声音时,应检查2A保险丝是否断裂。
6.试验做完后,冷却水不能关,每天工作结束后,清洗碱泵,方法如下:碱液管从容器中取出,放入蒸馏水容器内(蒸馏水必须在40℃左右)的温水中然后在蒸馏器前放上一只空的消化管,打开NaOH开关,抽取200ml蒸馏水(温水)2-3次清洗完成,保证使用寿命,尽量减少碱泵因结晶而无法使用。
7.KDN系列定氮仪采用凯氏定氮的原理进行测定,但是不同的样品,实际含氮量也有区别。所以,不同的样品必须采用不同的换算系数。如花生、大豆、蚕豆、大麦小麦、燕麦等的含氮量为17.6%,求得K=5.7;荞麦、葵花籽、亚麻籽、棉花籽、蓖麻子等换算系数则为K=5.5;玉米菜籽则为6.0;水稻为5.95,上述以外的其他样品换算系数均适用6.25,在计算公式中A也就不一样。
蛋白含量(%)=[(V1-V2)C×0.014×A×100]/W
公式中:V1-消耗盐酸(或硫酸)的毫升数
V2-空白实验时消耗盐酸(或硫酸)的毫升数
C-盐酸(或硫酸)的当量浓度
0.014-1ml盐酸(或硫酸)的当量数
A-A固定系数(6.25,5.7等)
W-试样重量g
空白测定:用0.1克糖代替样品或不加样品作空白测定。


摘要:用高效液相色谱法对饲料中维生素D3的检测过程中,BHT(2,6-二叔丁基对甲酚)对测定会产生影响。当维生素D3含量较低或检测人员经验不足时,检测峰易发生误判,造成检测结果的偏离。从BHT结构和实验入手,对检测过程进行优化,可消除BHT对饲料中维生素D3检测的影响,达到准确定性和准确定量的目的。
关键词:维生素D3;高效液相色谱仪;抗氧化剂;准确定量
维生素D3是维持机体正常活动必不可少的物质,常用于维生素D缺乏症的预防与治疗,适量的各种维生素D3作为饲料添加剂能促进禽畜生长,增强禽畜体质,产生显著的经济效益。
饲料中维生素D3的检测一般是按照GB/T 17818-2010进行,但是在分析检测过程中,经常会有饲料中维生素D3超过标准值的情况,在排除了企业添加值错误的情况外,本文首次发现了在检测过程中添加的抗氧化剂BHT对维生素D3含量测定结果产生的影响,并且对其进行了详细的讨论,达到了准确定量饲料中维生素D3的目的。
1.实验部分
1.1 实验仪器与试剂
高效液相色谱仪:岛津;电子分析天平(德国梅特勒);氮吹仪;圆底烧瓶(带回流冷凝器);电热套;抗坏血酸;乙醇;氢氧化钾;乙醚;氯化钠;BHT(2,6-二叔丁基对甲酚)。
1.2 样品前处理
称取样品10g,精确至0.0001g,置于250mL圆底烧瓶中,加入50mL L-抗坏血酸乙醇溶液,10mL氢氧化钾溶液,混合均匀,沸水浴上回流30min皂化。
皂化完成后,皂化液转移至装有50mL乙醚的250mL分液漏斗中提取,再分别用40mL、30mL乙醚重复提取2次,弃去水相,合并三次乙醚相。用氯化钠溶液50mL洗涤一次,弃去水相,再用50mL水洗涤乙醚提取液至中性。乙醚提取液用无水硫酸钠脱水,转移到100mL棕色容量瓶中,加入100mgBHT使之溶解,用乙醚定容至刻度。
取5.0mL乙醚溶液,氮气吹干,用甲醇定容至1.0mL,高效液相色谱仪分析。
1.3 色谱条件
色谱柱:C18 5μm 150×4.6 mm,流动相:甲醇:水=95:5,流速:1.0 mL/min,柱温:30℃,进样量:20.0μL,波长:264 nm
2.结果讨论
2.1 结果影响
实际测定中,我们发现,在1.3色谱条件下,维生素D3的含量普遍比标示含量偏高,而且在空白基质中,在与维生素D3对照品同一保留时间出现了强吸收峰,而且面积比较大,见图2,与维生素D3对照品检测重叠,对饲料中维生素D3的检测产生影响,具体谱图见图1-图4。



2.2 影响因素分析验证
通过对样品的分析过程进行拆解,对可能存在的影响因子一一进行排查,最后确定,用GB/T 17818-2010方法对样品进行分析检测,是BHT对整个的分析结果产生了影响。
2.2.1BHT结构剖析验证
维生素D3对光、热不稳定,在空气中容易氧化,光化成前反式维生素D3和后维生素D3等产物而失去活性。在实际测定中,加入BHT抗氧化剂,可防止其氧化。
在维生素D3提取过程中,在最后一步加入了抗氧化剂BHT,对其结构进行分析后发现BHT结构与维生素D3有相似的紫外吸收基团(具体结构式见图5)。维生素D3在264nm下,有较强的吸收。而BHT由于具有苯环结构,因此在由苯环共轭系统下π-π※跃迁产生B带特征吸收在254nm下有较强的吸收,又由于在BHT结构中,苯环上面有羟基,作为助色基团,会导致BHT最大特征吸收波长发生红移,因此BHT最大吸收波长会大于254nm,因此,可以考虑,在图2空白玉米样中,出现与维生素D3相同保留时间下出现的物质,是BHT带来的干扰

2.2.2 BHT的影响实验验证
介于BHT对维生素D3分析可能存在的影响,称取一定量的BHT,用甲醇溶解,按照1.3中色谱条件,进行分析,色谱图见图6.

从图6中可以看出,维生素D3对照品以及样品和单独的BHT在保留时间都为8.45min,因此可以证明,BHT对维生素D3含量的测定产生了影响,在图2中也得到了验证。在图3样品中出现的色谱峰物质,不完全是样品中维生素D3,而是维生素D3与BHT叠加后得到的色谱吸收峰。因此,在GB/T 17818-2010方法下,如果单纯的以保留时间作为维生素D3检测峰的话,对测定结果会产生很大的影响。
2.3 BHT影响的解决方法
2.3.1流动相的优化
为消除BHT的干扰,我们尝试更改有机相比例。
2.3.1.1调整流动相比例为90:10
当减小有机相甲醇的比例,调整为甲醇:水为

2.3.1.2调整流动相比例为98:2
更改流动相有机相比例为98:2时,发现此时维生素D3对照品和BHT能够彻底分开,见图8A;样品中的VD3和BHT也能完全的分开,见图8B,可排除BHT对维生素D3检测的干扰。
2.3.1.3调整流动相比例为100%甲醇
继续调整流动相比列为100%甲醇,我们发现,此时维生素D3对照品和BHT均无显著相应,具体情况见图9。
2.3.2BHT的添加及放置时间影响剖析
介于BHT对维生素D3存在的影响,本文取同一样品X,平行称取两份,X1样品按照1.2前处理方法进行前处理检测,X2样品亦按照1.2前处理方法进行前处理,但最后一步,X2样品定容时不加BHT,分别于4℃条件下放置0天(样品编号X1、X2)、3天(样品编号X3、X4)、7天(样品编号X5、X6)、15天(样品编号X7、X8),然后以2.3.1.3的色谱条件对其进行高效液相色谱检测分析,具体实验设计见表1。


从图8A中,可以看出,X样品在未加BHT的情况下,放置3天、7天以及15天的情况下,样品中维生素D3的含量与其加入BHT检测后的结果是基本不变的,也就是说,在检测饲料样品中的维生素D3时,半个月之内检测完毕,为了防止BHT对维生素D3的结果产生影响,是完全可以不添加BHT的。


3结论
本文首次发现了在检测过程中添加的抗氧化剂BHT对维生素D3含量测定产生的影响,并且从结构剖析方面以及单独的实验对其进行了验证,优化流动相比例,对其进行分离,同时对于检测过程中,BHT的添加与否在不同时间内对饲料中维生素D3含量测定的影响进行了详细的讨论。最后确定,在饲料中维生素D3的检测过程中,流动相的比例优化为98:2时,BHT与维生素D3可以有效的分离;其次,为避免BHT在检测过程中产生的干扰,在放置15天以内进行检测,不加BHT进行检测,亦可得到准确的结果,排除了BHT对其的影响,达到了准确定量饲料中维生素D3含量的目的,但由于维生素D3的前处理方法比较复杂,如何能够更快速有效的检测其含量还有待进一步研究。
参考文献(略)

