摘 要 硫酸氢根离子(HSO4)在生命、环境科学中发挥着非常重要的作用,进入环境后会污染环境,对人体造成危害。因此,选择性和高灵敏识别检测生物与环境样品中HSO4具有非常重要的意义。在众多的分析检测手段中,基于分子识别理念发展起來的光化学传感分子(探针)具有独特的优势。阴离子光化学传感体系以其选择性好、灵敏度高、易于实现在线分析,特别是可通过目视比色识别和原位检测等特点成为目前研究的热点。本文根据探针分子与HSO
4之间的作用机理, 对近年来HSO4的光化学探针分子进行分类和总结,综述了HSO4光化学探针的研究进展,并对其应用前景与发展趋势进行了展望。
关键词 硫酸氢根; 分子识别; 比色识别; 荧光探针; 综述
1 引 言
阴离子识别与传感是当前超分子化学研究领域一个重要和活跃的研究课题,与之相关的合成受体设计备受关注[1~4]。酰胺、胺、硫脲、脲、胍、吡咯/吲哚和酚羟基等具有氢键作用的基团作为阴离子结合单元,已被广泛应用于合成受体设计和阴离子识别研究,而具有荧光/吸收光谱响应的信号报告基团的引入赋予受体良好的光化学传感性能。基于分子识别理念发展起来的光化学传感分子(探针)具有独特的优势[5~8]。阴离子光化学传感体系以其选择性好、灵敏度高、易于实现在线分析,特别是可通过目视比色识别和原位检测等特点成为目前研究的热点。在众多阴离子中,HSO4在生物、环境科学和催化科学领域中起到重要作用:(1)SO24和HSO4在人体细胞中大量存在,在人体血浆中,SO24和HSO4的含量排在第4位,生物体细胞生长发育所需成分。很多重要的生物过程,包括生物合成和解毒都是通过将外源性和内源性物质硫酸盐化实现的。(2)HSO4常与其它的氧化性离子共存于核废料中,对放射性废物修复中的玻璃化过程产生非常不利的影响,在较高pH值的环境下会转化为毒性的SO24,进入到环境后会刺激人的皮肤和眼部,甚至造成呼吸麻痹。此外,很多化肥中含有HSO4,会污染耕地;煤炭中含有HSO4,有时会导致煤发电厂供电中断。(3)NaHSO4是非常重要的催化剂,特别是对催化缩合、脱水反应相当有效,受到广泛关注。因此,HSO4的检测非常重要。检测阴离子的手段主要有电感耦合等离子体质谱(ICP-MS)、电感耦合等离子体原子发射光谱法(ICP-AES)、离子色谱法和离子电极法。这些方法使用的仪器一般比较昂贵,并且需要训练有素的专业操作人员。而光化学探针方法所使用的紫外分光光度计和荧光分光光度计比较常见,操作简单,选择性好,灵敏度高,具有独特的优势[9~16]。但是,HSO4是两亲性离子,具有氢键给体/受体的双重特性,还具有四面体结构,由于受体对底物的选择性识别,可形象地描述为“锁与钥匙”的空间匹配,HSO4的特殊性质导致其受体设计比较复杂,目前关于HSO4的光化学探针分子的研究报道还相对较少。识别HSO4的机理主要通过氢键、金属-配体配位相互作用和化学反应等。本文根据其识别机理,综述了近十年HSO4光化学探针分子的研究进展。
2 基于氢键/质子化作用的硫酸氢根离子光化学探针分子
2.1 吡咯/吲哚类
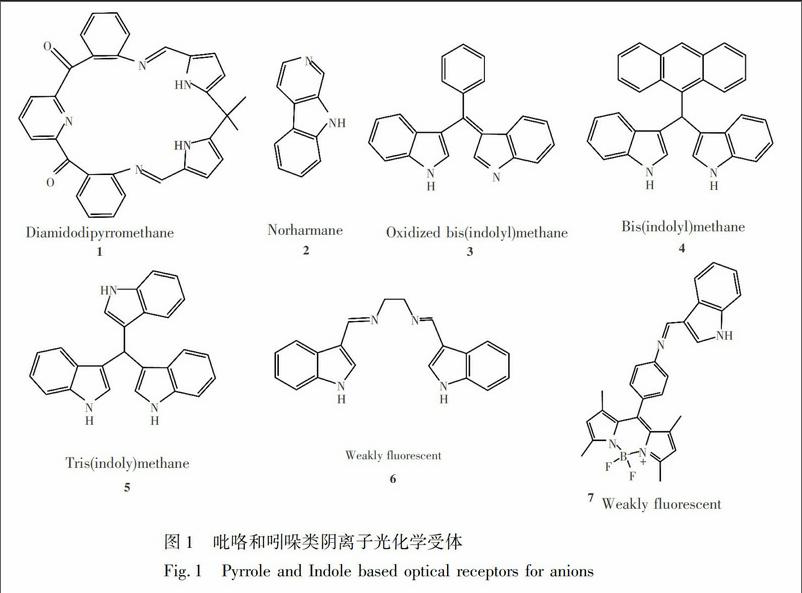
Sessler等[17]合成了一类大环状阴离子受体1(结构见图1),该受体由吡啶-二酰胺基团和二吡咯甲烷基团通过C=N链接在一起。该受体可在CN3CN溶液中选择性识别HSO4和H2PO4,有可能应用于硝酸盐废料中HSO4的去除。通过DFT理论计算,受体1具有一个深穴,构象柔顺,受体中的NH可直接与HSO4通过多重氢键形成1∶1氢键络合物。但是吡咯类阴离子受体光化学信号较弱,影响了吡咯类受体在光化学传感中的应用。
而苯并吡咯类衍生物即吲哚类化合物,不但可提供NH基团作为氢键给体,还可作为基本的光化学信号报告单元,在光化学传感分子设计中引起了广泛关注。Mallick等[18]研究了β-咔啉9H-吡啶并[3,4-b]吲哚(去甲哈尔满,Norharmane)2的阴离子识别与传感性能。该分子含有酸性氢键给体NH和1个碱性氢键受体单元N,可与碱性物质形成氢键,也可被酸性物质质子化。该受体可通过紫外和荧光手段选择性识别F和HSO4,呈现出不同的比率荧光变化特性,可高灵敏的检测阴离子。
本课题组首次合成了双吲哚烯类阴离子光化学传感分子3,该受体具有一个酸性氢键给体单元NH和一个碱性氢键受体单元N原子,是具有双重功能的比色传感分子[19]。可在有机溶剂中选择性识别F,在含水体系中选择性识别HSO4。在含水体系中HSO4可将受体质子化,从而引起体系颜色变化,达到比色识别HSO4的目的。
Sain等[20]研究了介位蒽取代的双吲哚烷4和三吲哚烷5的阴离子识别与传感性能,发现双吲哚烷4可通过比色和荧光双渠道高选择性识别HSO4,而受体5可选择性识别CN和HSO4,但是颜色变化不同。通过紫外-可见吸收光谱、荧光光谱、核磁共振谱和DFT理论计算研究了识别机理,双吲哚烷4和三吲哚烷5主要通过NH基团与HSO4发生氢键作用,而其它CH基团与阴离子之间形成的氢键也起到一定的辅助作用。
Wan等[21]合成了一类简单的双吲哚类阴离子荧光传感分子6,吲哚基团通过CN连接起来,该分子可作为HSO4的比色和荧光增强型荧光探针。通过紫外可见吸收光谱、荧光光谱与核磁共振谱和研究了其识别机理,发现HSO4可在乙醇溶剂中与受体中N(CN)原子以及吲哚NH质子形成多重氢键,从而抑制受体的CN异构化,增强平面刚性,从而引起荧光增强,探针分子与HSO4结合后荧光增强31倍。该探针分子合成简单,是一类荧光增强型的探针分子,但是荧光发射波长短(329 nm),在复杂体系中可能会有干扰。
吲哚类衍生物的合成相对比较简单,并且具有优良的阴离子识别性能,但是简单的吲哚类化合物的荧光信号较弱,共轭结构较小,量子产率较低,很难实现荧光传感与成像。因此在吲哚受体中引入强荧光信号单元,能够提高吲哚类受体的光化学信号。
氟硼荧(4,4-Difluoro-4-borata-3a-azonia-4a-aza-s-indacene,BODIPY)作为一类重要的有机荧光染料备受关注[22~24]。通过分子设计、有效组合不同的活性官能基团制备的功能化荧光探针分子成功应用于阴离子、阳离子和气体等的检测。本课题组合成了BODIPY修饰的吲哚类荧光受体7,该受体可在有机相和含水体系中高选择性识别HSO4,可作为HSO4的关-开型荧光探针分子[25]。采用多种谱学手段研究表明, 受体在乙腈有机体系中,HSO4与受体之间形成多重氢键,从而抑制了光诱导的电子转移(Photo-induced electron transfer, PET)过程,增强了受体平面刚性,导致受体荧光增强;在含水体系中,HSO4可将受体质子化,同样抑制PET过程,导致受体荧光增强。
2.2 含有杯[4]芳烃类
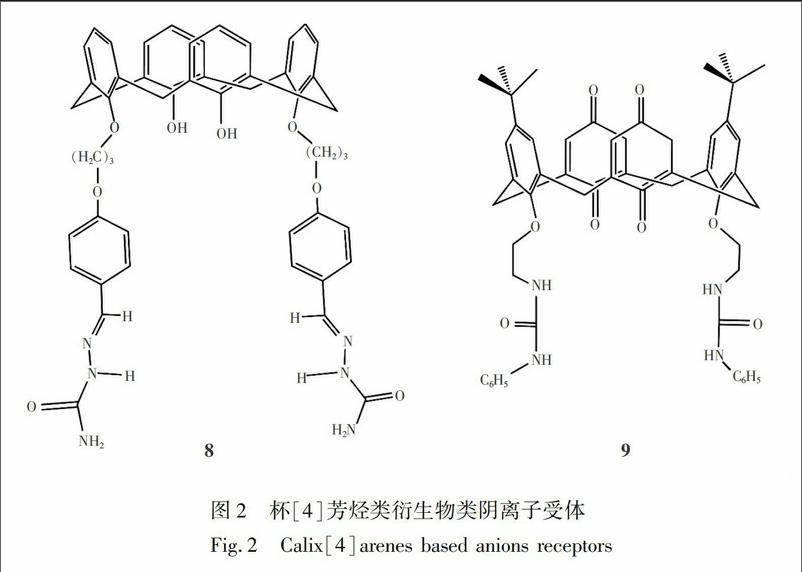
杯芳烃是由对位取代的苯酚与醛经缩合反应得到的一类大环化合物,因其形状像一个酒杯,故被称为杯芳烃(见图2),是继冠醚和环糊精之后出现的“第三代”主体分子。杯芳烃以其大小可调的空腔、构象可变和易于修饰等优点, 可借助于氢键、静电作用、分子作用力、堆积等非共价键作用来识别客体分子。目前,杯芳烃在分子组装、酶模拟,分子识别和光化学传感器等方面的应用已得到广泛而深入的研究[26]。
Chawla等[27]合成了杯[4]芳烃修饰的胺基脲受体8,该受体可高选择性识别HSO4,核磁滴定实验表明, 受体中NCH和NNH质子与HSO4在氯仿溶剂中通过多重氢键形成1∶1的氢键络合物,可高选择性识别HSO4。Nam等[28]合成了杯[4]芳烃修饰脲类受体分子氧化得到杯[4]二醌修饰的脲类受体9,该受体可高选择性识别HSO4,研究表明,HSO4与受体中的NH质子和喹啉基团形成了多重氢键。受体8和9与HSO4之间的作用机制已经得到充分研究,该类受体具有良好的识别性能,但是由于其光化学信号较弱,光化学传感性能未得到进一步研究。此外,该类受体需要多步合成才能得到,合成相对复杂,限制了其在光化学传感领域的应用。
2.3 苯并咪唑盐类
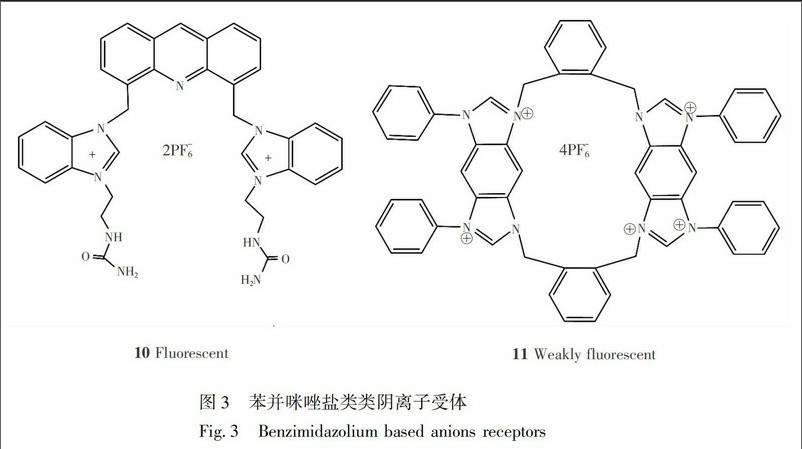
Zhang等[29]合成了系列吖啶作为荧光团的传感分子,该类分子含有两个苯并咪唑盐,具有钳型结构(见图3)。其中受体10含有两个脲作为阴离子键和单元,可通过紫外和荧光光谱高选择性识别检测HSO4和H2PO4。受体与H2PO4结合后呈现出比率荧光变化的特性,当与HSO4结合后荧光会发生一定程度的淬灭,可归因于PET过程。核磁滴定研究发现,受体中NH、CH质子和吖啶N與HSO4形成了多重氢键,这也是受体可高选择性键合HSO4的原因。
Song等[30]合成了一类环状的苯并二咪唑盐衍生物11,该化合物可在含水体系中通过紫外和荧光高选择性识别HSO4,是HSO4的关-开型荧光传感分子,受体在结合HSO4后,荧光强度增强6倍。紫外、荧光、核磁滴定、X-射线衍射以及理论计算表明,受体的预组织化、中性CH氢键作用和静电作用是受体能够实现在水中识别HSO4的关键原因。另一方面,理论计算表明,受体键合HSO4后电子分布在整个荧光团和苯并二咪唑单元中,电子密度的平均化是荧光增强的原因。
在荧光受体10和11的识别过程中,静电作用和CH的氢键作用均起到非常重要的作用,为HSO4受体的设计提供很好的思路。另一方面,受体11是“关-开”型探针分子,而受体10是“开关型”探针分子,就选择性而言,受体11的识别性能优于受体10。
2.4 其它类型荧光探针
Sen等[31]合成了含有苯并咪唑基团作为荧光信号报告单元的七元环化合物12,该传感分子可在含水体系中通过紫外可见吸收光谱和荧光光谱选择性检测HSO4,分子与HSO4结合后,呈现出比率荧光增强变化的特性。核磁滴定实验和理论计算结果表明,传感分子通过氢键和鳌合作用与HSO4结合后,形成新的体系,会抑制探针分子的PET过程,所以传感分子荧光增强。该分子具有良好的光谱性能和生物相容性,已经成功应用于Hela细胞荧光成像,可用于细胞内检测识别HSO4。
Kaur等[32]研究了喹啉作为荧光报告信号单元的荧光传感分子13的阴离子识别性能(见图4),该分子可选择性识别HSO4,与其作用之后呈现荧光淬灭的现象,通过Stern-Volmer plot 线性拟合结果阐明受体荧光淬灭过程为静态淬灭。核磁滴定和DFT理论计算结果表明HSO4与NH(与喹啉基团相连的)和喹啉基团的C-5位CH形成氢键,形成了没有荧光的氢键络合物。该探针分子合成方法较为成熟,荧光量子产率较低(0.024),灵敏度较高,具有良好的线性范围(0~60 μmol/L)范围,但是该探针分子是荧光淬灭型的探针分子,在复杂体系中干扰物可能会影响受体的选择性。
Li等[33]合成了一类硝基取代的偶氮苯基团作为光化学信号报告单元的比色传感分子14,该分子还包含希夫碱单元和羧基,可通过比色方法在含水体系中选择性识别HSO4。紫外和核磁滴定光谱分析表明传感分子与HSO4形成了多重氢键,具有较高的结合常数(Ka=6.59 × 104 L/mol),因此可实现在含水体系中对HSO4的选择性键合。并且具有较低的检出限(2.0 × 106 mol/L),具有良好的应用前景。
Alfonso等[34]合成了一类双二茂铁-苯并二咪唑的三元体系分子15,该分子可作为HSO4和Hg2+的荧光传感分子。该传感分子具有较低的量子产率(Φ=0.001),在乙醇溶剂中与HSO4作用后,荧光增强100倍(Φ=0.1)。核磁滴定和电化学实验发现,当HSO4与传感分子作用后,HSO4可能先发生质子转移,一方面对苯并咪唑的N原子质子化,另一方面HSO4的氧原子与苯并二咪唑NH形成双重氢键。该分子是一类荧光增强型探针分子,具有良好的荧光性能,并且提供一种相对较新的HSO4识别与传感机制,但是该探针分子不能在水溶液中实现对HSO4的识别检测。
Xue等[35]合成了系列杂环类化合物16,该类分子含有吡啶、呋喃和嘧啶基团。研究发现该类探针分子可在CHCl3/CH3OH混合溶剂中通过紫外和荧光光谱双渠道检测HSO4,探针分子通过氢键作用于HSO4结合,结合配比为1∶2。探针分子与HSO4作用后,紫外和荧光光谱均呈现出比率变化的特性,荧光发射波长由380 nm红移至470 nm,具有良好的光谱性能,但是探针分子在含水体系中的识别和传感性能没有被研究,限制了其进一步应用。
2.5 荧光传感分子材料化
基于氢键弱相互作用的阴离子探针分子,很难将其应用到含水体系中阴离子的检测,为了将其推向实际应用,开发固态传感材料,实现含水体系中HSO4的原位、快速检测具有重要意义。
罗丹明类化合物是以氧杂蒽为母体的碱性呫吨染料, 由于苯环间有“氧桥”相联,分子具有刚性平面结构,具有较高的荧光量子产率。而闭环结构的罗丹明内酰胺摩尔吸光系数和荧光量子产率非常低,几乎没有荧光。近年来,利用罗丹明的内酰胺螺环状结构设计荧光探针分子成为研究的热点[36]。
Rull-Barrull等将罗丹明传感分子修饰到纸上[37],二者通过羧酸酯键连接,形成了易携带、可重复使用的识别传感材料17。该材料可通过比色和荧光增强双渠道识别检测水中的HSO4,通过比色检测可实现对HSO4的半定量检测,检测极限为0.1~0.5 mmol/L。荧光分析手段检测HSO4的线性范围为0.5~30 mmol/L,检出限为11.6 μmol/L,该方法具有很强的实用性。这是首例可实现对含水体系中HSO4检测的固体传感材料,提供了一种简便的固态传感器的制备方法。
Kaur等[38]使用再沉淀法将罗丹明类传感分子18制成纳米聚集体N1,然后进一步将金纳米离子包裹在N1上,形成新的有机-无机杂化材料H1。研究表明, H1可在含水体系中选择性检测HSO4,H1与HSO4作用后荧光增强。荧光分析手段检测HSO4的线性范围为0~37 μmol/L,该材料具有较强的应用前景,已经将其应用于日常用品中HSO4的检测。Chopra等[39]再次使用再沉淀法将萘类荧光传感分子19作为纳米聚集体N2,研究发现,N2可在含水体系中选择性检测HSO4,呈现出荧光淬灭的现象,但是该传感材料具有良好的线性范围(0~65 μmol/L)和较低的检出限(1.12 μmol/L),适用于实际环境和生物样品的检测。
Lu等[40]合成了一类水溶性的共聚物20,可在含水体系中实现对HSO4的识别检测,与HSO4作用后呈现出比率荧光增强现象。核磁共振研究表明HSO4与聚合物的N(CN)原子和羟基形成氢键,会增强萘基团和CN基团之间的分子内电荷转移(Intramolecular charge transfer,ICT)。该聚合物材料具有良好的成膜性能,将其制作在石英片上,具有良好的稳定性,可实现在含水体系中对HSO4快速和高选择性识别。该薄膜对检测HSO4的线性范围为50~160 μmol/L,检出限为50 μmol/L。
通过不同的方法制备了不同的荧光传感材料(图5),这些材料均可在含水体系中选择性检测HSO4,适用于实际样品的检测,对HSO4具有不同的荧光响应、线性范围和检出限,可根据实际需要选择不同的材料。
3 基于希夫碱水解反应机理的硫酸氢根离子光化学探针
Kim等[41]首先合成了化合物21~23,并研究了其在含水体系中对阴离子的传感性能,研究发现荧光探针21和23可通过氢键作用选择性识别HSO4,引起传感分子的荧光增强。然而,Kumar等[42]否定了其作用方式和传感机理,重新研究了探针21~23的分子识别与传感性能,并且合成了化合物24作为参照。他们采用多种谱学手段证实HSO4在含水体系中会导致C=N水解,这是传感分子21~24实现对HSO4识别与光化学检测的原因。反应型阴离子荧光探针结构见图6。
Luo等[43]研究了喹啉-萘酰亚胺体系25的阴离子识别与传感性能,发现探针24可在含水体系中实现对HSO4的高选择性识别,探针分子与HSO4作用后荧光(λem=542 nm)增强8倍,是HSO4的荧光增强型荧光探针分子。通过核磁滴定和质谱研究发现,HSO4在含水体现中可将CN水解,形成醛基喹啉和萘酰肼类混合物。该探针分子检测HSO4的线性范围为5~50 μmol/L,检出限为0.78 μmol/L。而且,探针分子对HSO4的响应时间较短(3.5 min),响应pH值较宽(6~8),具有检测生物和环境中HSO4的应用潜力。
Wang等[44]合成并研究了BODIPY-希夫碱类化合物26在含水体系中的阴离子识别与传感性能,发现荧光探针26可通过紫外和荧光光谱高选择性检测HSO4,是一类关-開型荧光探针分子。探针分子与HSO4作用后荧光(533 nm)增强116倍,体系溶液发出绿色荧光。通过核磁滴定和高分辨质谱研究发现,HSO4在含水体现中可将探针26的CN水解,形成醛基BODIPY和萘胺类混合物。探针分子对HSO4的响应时间为2 min,检出限为0.065 μmol/L。该探针分子具有良好的水溶性和生物相容性,成功应用于HeLa细胞中HSO4的成像研究。此外,他们进一步将探针分子涂覆在试纸上,制成检测HSO4的试纸。
硝基苯呋咱(Nitrobenzofurazan, NBD)是荧光传感研究中一类重要的荧光团,其系列衍生物具有摩尔吸光系数大、荧光量子产率高、对环境变化灵敏以及荧光辐射波长在可见光区域等优点,引起了广泛关注[45]。Lin等[46]合成了NBD-希夫碱类化合物27,并研究了该探针分子在含水体系中对阴离子识别作用和光化学传感行为,发现探针27可通过比色和荧光双通道选择性检测HSO4,是HSO4的关-开型荧光探针。探针分子对HSO4的响应时间为1 min,检出限为0.24 μmol/L。核磁共振、质谱和X-射线衍射检测结果表明,HSO4与探针27作用后导致CN水解,这是实现HSO4检测的机理。
基于希夫碱(CN)水解反应的HSO4荧光探针相比于基于氢键作用的荧光探针分子具有明显的优势:(1)希夫碱化合物的合成一般较为容易,通常是将羰基化合物与胺(肼)类物质在乙醇/甲醇溶剂中一步反应得到,产物在室温下一般不溶于醇类溶剂,所以后处理较为简单;(2)探针分子是通过化学反应识别检测HSO4,具有很高的选择性和灵敏度,能够应用到含水体系和实际样品中HSO4的检测。因此,希夫碱的水解反应提供了一种方便、快捷和专一的分析检测HSO4的方法。
4 基于金属-配体的配位作用
Shen 等[47,48]合成了氧杂蒽酮修饰的冠醚化合物28,研究发现该化合物可与多种金属离子形成配合物,其中金属配合物28a和28b可选择性识别HSO4。配合物28由于PET作用,本身荧光比较弱,当探针28与金属离子形成配合物28a和28b,金属离子会阻断PET過程,所以金属配合物的荧光较强,金属-配体的阴离子探针结构见图7。当探针28a与HSO4作用后,HSO4会将Mg2+萃取出来,形成MgSO4,同时释放出的质子可能会将冠醚中的氧质子化或者形成水合氢离子包裹在大环内,导致体系荧光减弱,从而实现对HSO4的检测。探针28b与HSO4作用后,Zn2+被萃取出来形成ZnSO4,导致体系荧光减弱,达到分析检测HSO4的目的。
近年来,四苯基乙烯类化合物引起了极大关注,四苯基乙烯具有特殊的荧光性能,在溶液中荧光较弱或者没有荧光,在固体状态下荧光较强,被称为聚集诱导荧光。Zhang等合成了四(吡啶基苯基)乙烯29, 该化合物在溶液中荧光较弱,在加入4倍量的Hg2+后,荧光增强,但是依然较弱,然后在体系中加入HSO4,体系的荧光大幅度增强,然而在探针29的溶液中只加入HSO4并不能使体系荧光增强。研究表明,探针29中吡啶氮原子首先与Hg2+形成配合物,然后再通过HSO4互相连接,形成新的聚集体,导致体系荧光增强。这是首例阴阳离子协同调控四苯基乙烯荧光的报道,对于合成新的四苯乙烯类的离子对荧光探针有重要意义[49]。
Alfonso等[50]合成了二茂铁类荧光离子对配体30, 该配体可与Pb2+和Zn2+在CH3CN溶液中形成配合物,这两类配合物可选择性识别HSO4,与HSO4作用后形成新的配合物,分别使体系荧光增强5倍和7倍,是HSO4的关-开型荧光探针。但是,该配合物无法实现含水体系和实际样品中HSO4的检测,实际应用受到限制。
Fegade等[51]报道了吡咯取代的水杨酰亚胺-锌离子配合物31,该配合物可在含水体系中选择性识别HSO4,可通过紫外和荧光光谱双通道检测HSO4。HSO4与配合物作用后,会诱发体系的PET过程,使体系荧光减弱,是开-关型荧光探针。该探针分子检测HSO4的线性范围为0.2~80 μmol/L,检出限为0.04 μmol/L,具有良好的应用前景。
Sen等[52]合成了喹唑啉衍生物,并与Cu2+形成了水溶性无荧光的金属配合物32,可选择性与HSO4作用形成螯合物,使得体系荧光增强,荧光量子产率由0.07增加到0.51。HSO4与配合物中NH两个原子通过分子间氢键形成稳定的六元环结构,是通过鳌合作用使得荧光增强过程。该探针分子检测HSO4的线性范围为0.32~12.5 μmol/L,检出限为0.03 μmol/L,由于该配合物具有良好的生物相容性,可应用于Hela细胞中HSO4的检测。
5 总结与展望
近年来, HSO4光化学探针分子的研究已经取得了很大的进展,大部分探针分子的识别机理是氢键作用,使其很难应用到含水体系中,限制了其实际应用。此外,具有良好生物相容性,适用于活细胞和活体内HSO4成像检测的新型荧光分子探针还比较少。HSO4探针分子的研究应侧重以下两个方面:(1)通过设计合成新的探针母体和信号响应基团,制备稳定性高、选择性好、能够在含水体系中检测HSO4,并且具有良好生物相容性的探针分子,可实现在含水体系和生物体系的识别检测和成像,发展新型的基于希夫碱水解反应和其它反应型的探针分子可能实现这一目标;(2)探针分子器件化,有机探针分子与纳米材料、高分子材料等结合,发展器件化的探针分子,实现含水体系和实际样品中HSO4的检测。
References
1 Busschaert N, Caltagirone C, Van Rossom W, Gale P A. Chem. Rev., 2015, 115(15): 8038-8155
2 Li A, Wang J, Wang F, Jiang Y. Chem. Soc. Rev., 2010, 39: 3729-3745
3 Duke R, Veale E, Pfeffer F, Kruger P, Gunnlaugsson T. Chem. Soc. Rev., 2010, 39: 3936-3953
4 Gale P. Chem. Soc. Rev., 2010, 39: 3746-3771
5 Sakai R, Satoh T, Kakuchi T. Polym. Rev., 2017, 57: 159-174
6 Moragues M, Martínez-Mez R, Sancenón F. Chem. Soc. Rev., 2011, 40: 2593-2643
7 Santos-Figueroa L E, Moragues M E,Climent E, Agostini A, Martinez-Manez R, Sancenon F. Chem. Soc. Rev., 2013, 42: 3489-3613
8 Martinez-Manez R, Sancenon F. Chem. Rev., 2003, 103: 4419-4476
9 Wang L Y, Yang L L, Cao D R. J. Fluoresc., 2014, 24: 1347-1355
10 Mukherjee M, Pal S, Sen B, Lohar S, Banerjee S, Banerjee S, Chattopadhyay P. RSC Adv., 2014, 4: 27665-27673
11 Li Q, Yue Y, Guo Y, Shao S J. Sens. Actuators B, 2012, 173: 797-801
12 Yang S T, Liao D J, Chen S J, Hu C H, Wu A T. Analyst, 2012, 137: 1553-1555
13 Erdemir S, Tabakci B, Tabakci M. Sens. Actuators B, 2016, 228: 109-116
14 Paul S, Karar M, Mitra S, Sher Shah S A, Majumdar T, Mallick A. Chem. Select., 2016, 1: 5547-5553
15 Lu W, Chen D, Jiang H, Jiang L M, Shen Z Q. J. Polym. Sci. A, 2012, 50: 590-598
16 Lu W, Zhang M Y, Liu K Y, Fan B, Xia Z, Jiang L M. Sens. Actuators B, 2011, 160: 1005-1010
17 Sessler J L, Katayev E, Pantos G D, Ustynyuk Y A. Chem. Commun., 2004: 1276-1277
18 Mallick A, Katayama T, Ishibasi Y, Yasuda M, Miyasaka H. Analyst, 2011, 136: 275-277
19 He X M, Hu S Z, Liu K, GuoY, Xu J, Shao S J. Org. Lett., 2006, 8: 333-336
20 Sain D, Kumari C, Kumar A, Dey S. Supramol. Chem., 2016, 28: 239-248
21 Wan C F, Yang S, Lin H Y, Chang Y J, Wu, A T. Luminescence, 2014, 29: 500-503
22 Boens N, Leen V, Dehaen W. Chem. Soc. Rev., 2012, 41: 1130-1172
23 Ulrich G, Ziessel R, Harriman A. Angew. Chem. Int. Ed., 2008, 47: 1184-1201
24 Loudet A, Burgess, K. Chem. Rev., 2007, 107: 4891-4932
25 Li Q, Guo Y, Shao S J. Analyst, 2012, 137: 4497-4501
26 LYU Jian-Quan, HE Xi-Wen, CHEN Lang-Xing, LAI Jia-Ping. Chinese J. Anal. Chem., 2001, 29(11): 1336-1344
呂鉴泉, 何锡文, 陈朗星, 赖家平. 分析化学, 2001, 29(11): 1336-1344
27 Chawla H M, Sahu S N, Shrivastava, R. Tetrahedron Lett., 2007, 48: 6054-6058
28 Nam K C, Kang S O, Jeong H S, Jeon S. Tetrahedron Lett., 1999, 40: 7343-7346
29 Zhang D W, Jiang X Z, Dong Z Y, Yang H Q, Martinez A, Gao G H. Tetrahedron, 2013, 69: 10457-10462
30 Song N R, Moon J H, Choi J, E J Jun, Kim Y, Kim S J, Lee J Y, Yoon J. Chem. Sci., 2013, 4: 1765-1771
31 Sen B, Mukherjee M, Pal S, Mandal S K, Hundal M S, Khuda-Bukhsh A R, Chattopadhyay P. RSC Adv., 2014, 4: 15356-15362
32 Kaur P, Kaur H, Singh K. Analyst, 2013, 138: 425-428
33 Li P, Zhang YM, Lin Q, Li J Q, Wei T B. Spectrochim. Acta A, 2012, 90: 152-157
34 Alfonso M, Trraga A, Molina P. Org. Lett., 2011, 13: 6432-6435
35 Xue W J, Li L, Li Q, Wu A X. Talanta, 2012, 88: 734-738
36 Chen X Q, Pradhan T H, Wang F, Kim J S, Yoon J. Chem. Rev., 2012, 112(3): 1910-1956
37 Rull-Barrull J, d'Halluin M, Le Grognec E, Felpin F X. Chem. Commun., 2016, 52: 2525-2528
38 Kaur R, Singh J, Saini A, Singh N, Kaur N. RSC Adv., 2014, 4: 48004-48011
39 Chopra S, Singh J, Singh N, Kaur N. Anal. Methods, 2014, 6: 9030-9036
40 Lu W, Zhou J T, Liu K Y, Chen D, Jiang L M, Shen Z Q. J. Mater. Chem. B, 2013, 1: 5014-5020
41 Kim H J, Bhuniya S, Mahajan R K, Puri R, Liu H G, Ko K C, Lee J Y, Kim J S, Chem. Commun., 2009: 7128-7130
42 Kumar V, Kumar A, Diwan U, Upadhyay K K. Chem. Commun., 2012, 48: 9540-9542
43 Luo Z L, Yin K, Yu Z, Chen M X, Li Y, Ren J. Spectrochim. Acta A, 2016, 169: 38-44
44 Wang L Y, Ou J J, Fang G P, Cao D R. Sens. Actuators B, 2016, 222: 1184-1192
45 GU Zhen-Yuan, XU Qin-Chao, XING Guo-Wen. Prog. Chem., 2013, 25(8): 1302-1312
古振遠, 徐勤超, 邢国文. 化学进展, 2013, 25(8): 1302-1312
46 Lin C Y, Huang K F, Yen Y P. Spectrochim. Acta A, 2013, 115: 552-558
47 Shen R, Pan X B, Wang H F, Wu J C, Tang N. Inorg. Chem. Commun., 2008, 11: 318-322
48 Shen R, Pan X B, Wang H F,Y L H, Wu J C, Tang N. Dalton Trans., 2008: 3574-3581
49 Huang G X, Zhang G X, Zhang D Q. Chem. Commun., 2012, 48: 7504-7506
50 Alfonso M, Espinosa A, Tarraga A, Molina P, Chem. Commun., 2012, 48: 6848-6850
51 Fegade U, Bhosale J, Sharma H, Singh N, Bendre R, Kuwar A. J. Fluoresc., 2015, 25: 819-824
52 Sen B, Mukherjee M, Pal S, Sen S, Chattopadhyay P, RSC Adv., 2015, 5: 50532-50539
- 初中数学教学中关于小组合作教学模式的思考
- 数学实验在小学数学教学活动中的应用研究
- 生活情境方法在小学数学教学中的运用分析
- 巧设共建“上”出精彩
- 核心素养背景下高中数学教学信息化探究
- 浅谈初中数学教学中的四个“适”
- 论提高小学中高段数学“学困生”的学习能力的对策
- 小学数学教学中“问与学”有机结合的策略研究
- 分类讨论思想在初中数学教学中的应用分析
- 高中数学“问题-互动”教学的探索与实践
- 小组合作构建初中数学自主探究课堂的思考
- 变式教学在初中数学教学中的实践与应用
- 高中数学高质量试卷命制的研究
- 分层教学视阈下“圆与相似”教学设计研究
- 基于问题导向的极大线性无关组教学设计研究
- 提升高等数学教学质量的几点思考
- 网络信息资源对小学数学教学有效性的影响
- 信息技术在小学数学“图形与几何”课堂教学中的应用解析
- 影响小学高年级学生数学自主学习的原因及对策
- 浅谈学生数学创新力的引导与养成
- 多媒体技术在初中数学教育教学中的应用分析
- 利用微课提升初中数学学困生学习能力的要点分析
- 数学图形在高中数学教学中的重要性
- 最优旅行目的地选择及旅行路径规划
- 关于扩充基定理的一个注记
- stockpiler
- stockpilers
- stockpiles
- stockpiling
- stockprice
- stock price
- stock right
- stockright
- preplanned
- preplanning
- preplans
- preplanted
- preplants
- prepledge
- prepledged
- prepledges
- prepledging
- preplot
- preplots
- preplotted
- preplotting
- prepoetic
- prepoetical
- prepolice
- prepolish
- hiphop
- hiv
- hiv
- hm
- hnd
- hng
- hold住体
- hold住
- h.o.l.l.a.n.d
- h.o.l.l.a.n.d.
- homepage
- hong
- honɡ
- hou
- hp
- hrm
- hsk
- hsk
- hth
- hu
- hu~
- hua
- huai
- huan
- huang