摘要:介绍了液膜扩散法鉴定溶液中存在的Fe3+和Fe2+。鉴于不同浓度的Fe3+、Fe2+与不同的鉴定试剂反应呈现不同的现象,通过不同反应体系的“比邻式”或“同心圆”的自然扩散实验,得出一定实验条件下Fe3+、Fe2+与不同鉴定试剂反应的最佳浓度比,可以鲜明、准确地对Fe3+、Fe2+进行鉴定,由此为中学化学实验中其他常见阳离子的鉴定提供了新思路。
关键词:液膜扩散;Fe3+和Fe2+;离子鉴定;实验探究
文章编号:1005–6629(2017)11–0053–03 中图分类号:G633.8 文献标识码:B
《普通高中化学课程标准(实验)》中指出:“要鼓励教师开发实验仪器,研究低成本、少污染的化学实验,体现绿色化学的思想,同时在教学中培养学生的环境保护意识。[1]”目前,中学化学实验存在实验现象不够直观鲜明、实验成功率不高、实验在安全性环保性方面有欠缺、不符合绿色化学要求等问题[2]。如Fe3+和Fe2+是中学化学常见的阳离子,其鉴定方法较为单一,药品用量不够明确,实验现象也不够清晰等,这非常不利于学生科学探究能力和实践创新能力的培养和提高。
液膜扩散法是我们教研室自2010年应用于无机化学实验和中学化学实验教学的新方法,取得了较好的教学效果。对于中学常见离子Fe3+和Fe2+的鉴定现象明显,试剂用量少,成功率高,体现了绿色化学的思想,能够有效地落实中学化学学科核心素养中科学精神和实践创新的培养要求。
1 实验部分
1.1 实验仪器与试剂
仪器:正方形玻璃片若干、尖头玻璃棒、照相机、100mL小烧杯等
试剂:0.5mol/L Fe3+、0.1mol/L Fe3+、0.1mol/L KSCN、2.0mol/L NaOH、5%淀粉溶液、0.2mol/L KI;0.5mol/L Fe2+、0.1mol/L Fe2+、0.05mol/L KMnO4
1.2 Fe3+鉴定新方法
方法一:Fe3+与KSCN溶液“比邻式”自然扩散实验
在两片玻璃片上,相距约1.5cm处,分别滴加1滴0.1mol/L Fe3+、1滴0.1mol/L KSCN和1滴0.5mol/L Fe3+、1滴0.1mol/L KSCN溶液,用尖头玻璃棒将两种溶液涂成薄薄的液膜,并引导这两种相邻液膜靠近至自然扩散,见图1和图2。

在两片玻璃片上分别滴3滴2.0mol/L NaOH,用尖头玻璃棒涂成一层薄膜,在同心位置距离液膜3mm处分别垂直滴下1滴0.1mol/L Fe3+和0.5mol/L Fe3+,Fe3+由中间向四周逐渐扩散,见图3和图4。

图3与图4分别是浓度为0.1mol/L和0.5mol/ L Fe3+与2.0mol/L NaOH“同心圆”自然扩散反应的照片,其反应原理:Fe3++OH-=Fe(OH)3↓。对于同心的位置滴下1滴氯化铁,液滴的中间厚两边薄,首先接触氢氧化钠的氯化铁浓度低,随着氯化铁的扩散,最先反应的部分已经变成深褐色,表现出氯化铁是逐级扩散发生反应的。可以看出0.5mol/L Fe3+反应中从反应物到生成物形成的黄色(FeCl3)溶液膜、红褐色[Fe(OH)3]和无色(NaOH)液膜的三阶对比,实验现象更明显,有利于演示实验教学。所以用2.0mol/L NaOH鉴定Fe3+,0.5mol/L是Fe3+的适宜浓度。
方法三:Fe3+与淀粉KI溶液“比邻式”自然扩散实验
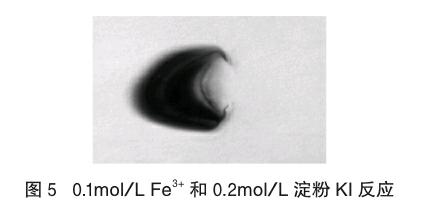
在两片玻璃片上,相距约1.5cm处,分别滴加1滴0.1mol/L Fe3+、1滴0.2mol/L淀粉KI和1滴0.5mol/L Fe3+、1滴0.2mol/L淀粉KI,用尖頭玻璃棒将两种溶液涂成薄薄的液膜,并引导这两种相邻液膜靠近至自然扩散,见图5和图6。

方法二:Fe2+与NaOH溶液“同心圆”自然扩散实验
在两片玻璃片上分别滴3滴2.0mol/L NaOH,用尖头玻璃棒涂成一层薄膜,在同心位置距离液膜3mm处分别垂直滴下1滴0.1mol/L Fe2+和1滴0.5mol/L Fe2+,Fe2+由中间向四周逐渐扩散,见图9和图10。

用2.0mol/L NaOH鉴定Fe2+,选择0.5mol/L Fe2+进行实验较适合,c(NaOH):c(Fe2+)=4:1时,Fe2+的鉴定实验效果较明显。
3 实验说明
(1)选用玻璃片时,最好选用无色透明的材料,有利于观察颜色的变化,使用时注意用砂布磨去四边锋刃,洗净备用[3],保证实验教学的效果和师生的安全。
(2)在配制溶液过程中,注意准确称量固体样品,配制溶液时用蒸馏水,避免引入其他杂质,影响实验效果。
(3)在用尖嘴玻璃棒将两种溶液涂成薄薄的液膜时,注意避免液体散落;在同心位置上面滴溶液时,注意高度,避免液体飞溅。
(4)实验在透明的平面玻璃上进行,避免了点滴板或试管底部凹面对光线的影响,可以直视实验部位[4]。所以对实验现象进行拍照时需注意直视实验颜色部位。
4 总结
目前,高中化学实验中普遍存在一些问题:一是实验药品用量不明确,通常用“少量”、“适量”、“过量”、“几滴”等较笼统的词语概括,学生在实验过程中,对实验药品的实际用量难以把握,易导致药品浪费,使实验成本升高,甚至会造成污染;二是实验现象观察不够全面,有的只能观察到起点与终点的变化,对于中间的反应过程则不易观察到;三是实验结果只能以文字形式保存,对有些直观现象不能保留下来。而本文采用定量的方式对Fe3+和Fe2+进行鉴定,通过自制的正方形玻璃片作为点滴板,使用相机记录溶液间反应的颜色变化,克服了上述存在的问题,对探索中学实验中其他常见显色离子的鉴定提供了新思路。
参考文献:
[1]中华人民共和国教育部制定.普通高中化学课程标准(实验)[S].北京:人民教育出版社,2003:41.
[2]李猛等.中学化学实验改进研究述评[J].中学化学,2016,(1):6.
[3]杨兴等.淀粉与碘水自然扩散显色反应过程的研究[J].化学教学,2015,(10):59.
[4]北京师范大学无机教研室等编.无机化学实验(第3版)[M].北京:高等教育出版社,2009:15.
- 科技型中小企业创新能力对企业价值的影响研究
- F分数模型在上市公司财务风险预警中的应用
- 论双重股权结构在我国企业的运用
- 永辉超市慈善捐赠与经济责任的承担策略研究
- 基于主成分分析法的我国钢铁行业财务预警模型构建研究
- 企业产品毛利率变化分析方法探讨
- 企业外部资金需求量预测及动态调整解析
- 我国企业海外并购的风险分析与对策研究
- 共享服务模式下会计师事务所年报审计优化研究
- 财务共享中流程管理现状与再造
- 资产证券化业务中涉及的金融资产终止确认问题探讨
- 机构投资者、会计信息质量与融资约束
- 环境不确定性、资产持有意图不明晰与双重计量模式
- 基于“双功能、双基础、双报告”的政府会计信息系统核算体系研究
- 全面“营改增”对利益相关者的影响分析
- 税收优惠政策对企业研发投入的激励效应研究
- PPP模式下税收政策供给研究
- 企业赠送物品涉税管理及风险实例研究
- 面向扶贫审计的大数据审计案例研究
- 上市公司运用非经常性损益进行盈余管理的案例研究
- 社会责任会计:必要性、面临挑战与优化路径
- 我国重污染企业环境会计信息披露现状及其改进
- 清产核资为农村集体产权制度改革开路
- 基于Malmquist指数的烟草商业企业全要素生产率分析
- 基于DEA和Malmquist指数的区域科技金融效率测度
- cayenne-pepper
- cayenne pepper
- cayenne's
- cayennes
- caˌshier's cheque
- cba
- cbd
- cbi
- cbt
- cbu
- cc
- c, c
- -cc-
- cc'd
- cc'ed
- cc'ing
- ccing
- cc's
- cctv
- cctvs
- cc’ed
- cc’ing
- cc’s
- cd
- c /d
- r2022090420001133
- r2022090420001135
- r2022090420001136
- r2022090420001137
- r2022090420001138
- r2022090420001139
- r2022090420001142
- r2022090420001143
- r2022090420001144
- r2022090420001145
- r2022090420001146
- r2022090420001147
- r2022090420001148
- r2022090420001149
- r2022090420001150
- r2022090420001152
- r2022090420001154
- r2022090420001155
- r2022090420001156
- r2022090420001157
- r2022090420001158
- r2022090420001159
- r2022090420001161
- r2022090420001163
- r2022090420001164