胡雅芹 魏好程 何传波 李志强 熊何健


摘要?以天然栀子黄色素为材料,以色素损失率为指标,分别考察了不同pH、温度、光照强度和常见食品体系氧化剂、还原剂、金属离子条件对其稳定性的影响,探究了pH、高温、日光照射、Fe3+、H2O2和Na2SO3等因素对色素稳定性破坏程度,同时开展了食品体系中栀子黄色素应用分析。研究结果表明,栀子黄色素在pH 3~11内稳定性良好,短时耐热性良好,避光稳定性良好,0.3% 浓度的H2O2氧化剂或Na2SO3还原剂环境中色素稳定性良好,在NaCl、Na2CO3、CaCl2、CuSO4盐溶液体系中性质稳定,但在Fe3+环境中易于褪色。建议通过提高色素纯度,降低栀子苷含量和利用β-环糊精、EDTA-Na2等食品胶体共混体系包埋、鳌合特性,避免使用金属铁制容器和工具等方法,提高栀子黄色素稳定性。该研究结果为栀子黄色素在食品中的应用提供了基础参考依据。
关键词?栀子黄色素;色素损失率;稳定性
中图分类号?TS?264.4文献标识码?A
文章编号?0517-6611(2020)17-0178-04
doi:10.3969/j.issn.0517-6611.2020.17.046
开放科学(资源服务)标识码(OSID):
Study on the Stability of Gardenia Yellow Pigment
HU Ya?qin,WEI Hao?cheng,HE Chuan?bo et al
(School of Food and Bioengineering,Jimei University,Xiamen,Fujian 361021)
Abstract?The natural gardenia yellow pigment used as the material and the pigment loss rate as indicators,the effects of different pH,temperature,light intensities and common food system oxidants,reducing agents,and metal ion conditions on their stability were investigated.The damage degree of factors such as pH,high temperature,sunlight,Fe3+,H2O2,and Na2SO3 to the stability of pigments was explored.At the same time,the application analysis of gardenia yellow pigment in food systems was carried out.The results showed that gardenia yellow pigment had good stability in the pH range of 3-11,good short?term heat resistance,and good light stability.The 0.3% concentration of H2O2 oxidant or Na2SO3 reducing agent had good pigment stability in NaCl,Na2CO3,CaCl2,CuSO4 salt solution system,but it was easy to fade in Fe3+ environment.It was recommended to improve the gardenia yellow pigment stability by improving the purity of the pigment,reducing the content of gardenoside and using the embedding and chelating characteristics of food colloidal blending systems such as β?cyclodextrin and EDTA?Na2,and avoiding the use of metal iron containers and tools.The results of this study provided a basic reference for the application of gardenia yellow pigment in food.
Key words?Gardenia yellow pigment;Pigment loss rate;Stability
栀子黄(crocin,gardenia yellow)色素是以梔子果实为原料,提取精制的一种天然食用黄色物质[1]。与其他人工合成色素相比,栀子黄色素自然、艳丽,色价达400以上,加工应用稳定性好,不易褪色,更易被加工者和消费者所接受,广泛应用于食品烘焙、酱料、饮料等加工领域[2]。其主要成分是类胡萝卜素类的藏花素(crocin)和藏花酸(crocetin),是一类水溶性类胡萝卜素,极易被人体吸收,在人体内可以转化为维生素A,是一种营养型着色剂[3-4]。
栀子在我国有上千年的食用历史,民间有用栀子泡茶饮用的习俗,是1998年卫生部公布的第一批既是食品又是药品的品种名单。栀子黄色素在小鼠体内慢性毒理学试验表明,大于22 000 mg/kg(体重)剂量对小鼠有弱蓄积性,无致突变作用。小鼠食用含有2%栀子黄色素的饲料亚慢性试验表明,小鼠无任何异常,表明该色素安全无毒[5]。栀子黄色素具有清热祛火,凉血利胆,降低胆固醇的保健功能,是一种集着色、营养等多功能为一体的天然植物色素。栀子黄色素分子中含有多个共轭双键,既是其发色基团,又是其化学性质不稳定的内因,易于受环境中光照、温度、酸碱等因素影响而发生氧化,导致产品褪色和变色,限制了其在食品加工领域的广泛应用[6]。
基于人们对天然栀子黄色素在食品加工领域长期使用的习惯和其自身高色价,易溶于水,且具有的天然保健功效等特点,了解栀子黄色素在自然环境及复杂食品加工体系中的稳定性就显得十分有意义。生产栀子黄的方法有乙醇溶液提取法、水提取法和乙醇、乙醚浸提法等[7-9]。张伦等[10]发现栀子黄色素溶液在高温环境中稳定性不佳,同时氧化剂的存在也会加速色素的损失。张兆英等[11]、邹玉红等[12]对金丝小枣中天然红色素的研究表明,光照、酸性条件对其稳定性影响显著。而对于天然栀子黄色素应用稳定性研究鲜有报道。该研究以天然栀子黄色素为材料,研究了其光谱特性,并以色素损失率为考核指标,对不同pH、温度、光照和常见食品体系氧化剂、还原剂、金属离子环境对该色素的稳定性进行研究,以期为栀子黄色素在工业中的应用提供基础参考,促进栀子黄色素应用和产业发展。
1?材料与方法
1.1?材料、试剂与仪器
1.1.1?材料与试剂。
栀子黄色素,食品级,由厦门璞真食品有限公司提供;柠檬酸、碳酸氢二钠、双氧水、亚硫酸钠、硫酸铜、三氯化铁、氯化钠、氯化钙、无水乙醇均为分析纯,购于西陇科学股份有限公司和中国医药上海化学试剂公司。
1.1.2?主要仪器。
EL104电子天平(梅特勒托利多仪器有限公司);SY-2-2电热式恒温水浴锅(天津欧诺仪器仪表公司);UV-5200紫外可见分光光度计(上海元析仪器有限公司);DHP-9052电热恒温干燥箱(上海精宏实验设备有限公司);GZX-250光照度培养箱(常州国宇仪器制造有限公司)。
1.2?方法
1.2.1?栀子黄色素吸收波长的检测。
参照国家标准GB 7912—2010方法,准确称取恒温干燥后的栀子黄色素粉末0.10 g,用重蒸水定容至100 mL容量瓶,摇匀静置后得到1 mg/mL栀子黄色素标准溶液。以蒸馏水作空白,用紫外可见分光光度计对栀子黄色素标准溶液进行全波长扫描,确定其最大吸收波。
1.2.2?栀子黄色素稳定性的评价指标。参照文献略有修改[13],采用色素损失率作为栀子黄色素稳定性的评价指标,见公式(1)。
色素损失率=A前-A后A前×100%(1)
式(1)中,A前为处理前栀子黄色素溶液在最大波长处的吸光值;A后为处理后栀子黄色素溶液在最大波长处的吸光值。
1.2.3?栀子黄色素稳定性研究。
1.2.3.1?pH对栀子黄色素稳定性的影响。
准确称取5份恒温干燥后的栀子黄色素粉末各0.10 g,分别用pH为3、5、7、9、11的柠檬酸/磷酸氢二钠缓冲液定容至100 mL,摇匀静置。分别在0、2、4、6、8 h用各自相对应pH缓冲水溶液为参比液,测定不同pH溶液中栀子黄色素损失率,试验重复3次。
1.2.3.2?温度对栀子黄色素稳定性的影响。
准确移取1 mg/mL栀子黄色素标准溶液3.0 mL共45份于玻璃试管,分别避光置于室温(25 ℃)、60 ℃水浴和100 ℃水浴中,分别在0、2、4、6、8 h时测定不同温度环境中栀子黄色素损失率,试验重复3次。
1.2.3.3?光照对栀子黄色素稳定性的影响。
准确移取1 mg/mL栀子黄色素标准溶液3.0 mL共45份于玻璃试管,分别置于太阳直射(中国南方4月9:00—18:00阳光直射,平均气温25 ℃)、室内自然光和室内避光3种环境中,分别在0、2、4、6、8 h时测定不同光照强度下栀子黄色素损失率,试验重复3次。
1.2.3.4?H2O2氧化劑对栀子黄色素稳定性的影响。
准确称取5份恒温干燥后的栀子黄色素粉末各0.10 g,分别用浓度为0.1%、0.2%、0.3%的H2O2溶液定容至100 mL,摇匀静置,分别在0、2、4、6、8 h用各自相对应浓度H2O2水溶液为参比液测定不同浓度H2O2溶液中栀子黄色素损失率,试验重复3次。
1.2.3.5?Na2SO3还原剂对栀子黄色素稳定性的影响。
准确称取5份恒温干燥后的栀子黄色素粉末各0.10 g,分别用浓度为0.1%、0.2%、0.3%的Na2SO3溶液定容至100 mL,摇匀静置,分别在0、2、4、6、8 h用各自相对应浓度Na2SO3水溶液为参比液测定不同浓度Na2SO3溶液中栀子黄色素损失率,试验重复3次。
1.2.3.6?食品体系常见金属离子对栀子黄色素稳定性的影响。
准确称取5份恒温干燥后的栀子黄色素粉末各0.10 g,分别用0.2%(M/V)的FeCl3、CuSO4、NaCl、Na2CO3、CaCl2金属盐溶液定容至100 mL,摇匀静置,分别在0、2、4、6、8 h用各自相对应盐溶液为参比液测定不同金属离子溶液中栀子黄色素损失率,试验重复3次。
1.3?数据处理
使用Excel软件进行统计分析,数据用Mean ± SE表示,采用 LSD 对数据进行多重比较和显著性分析。使用 SPSS19.0 统计软件对试验结果进行方差分析。
2?结果与分析
2.1?栀子黄色素特征吸收波长检测?栀子黄色素的扫描图谱如图1所示。由图1可知,栀子黄色素水溶液在238、325、440 nm处有3个典型特征吸收峰值,分别是栀子苷、绿原酸、藏花素和藏花酸特征吸收峰。从图1可发现440 nm处藏花素和藏花酸特征吸收峰值强烈,与GB 7912—2010中所描述的(440±5) nm结果一致,故试验采用440 nm作为栀子黄特征吸收波长进行后续稳定性试验检测。
238、325 nm處吸收峰值的存在反映供试栀子黄色素的加工水平和纯度。供试栀子黄色素材料A238/A440=0.378,小于0.4表明该样品纯度较高,能满足该试验和生产所用。
2.2?栀子黄色素稳定性结果
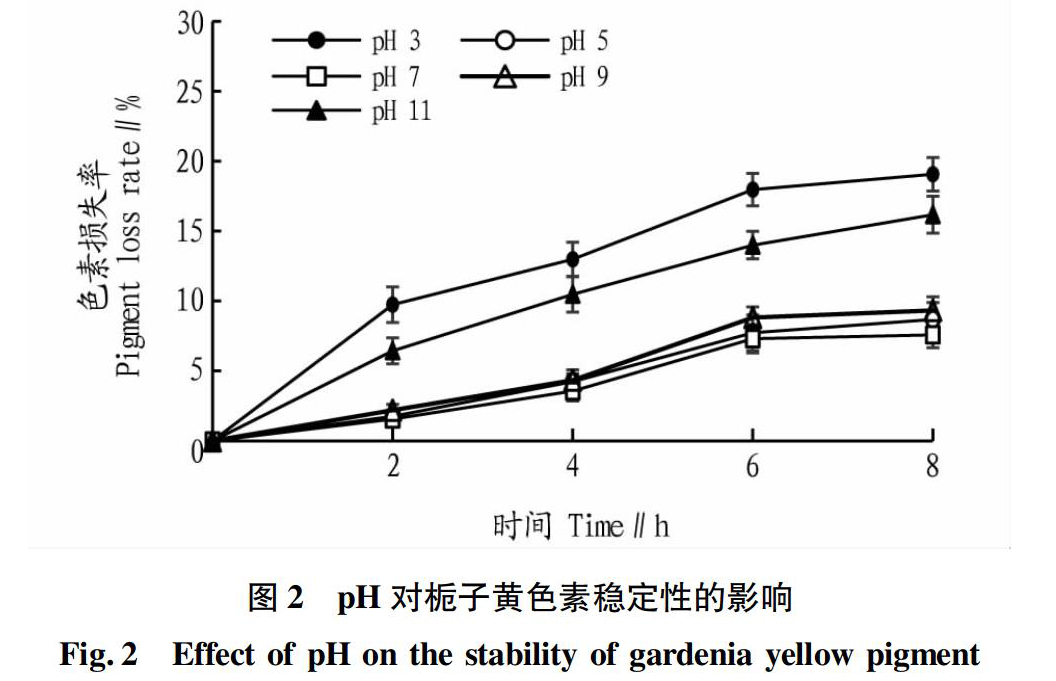
2.2.1?pH对栀子黄色素稳定性的影响。由图2可知,在pH为3~11时,栀子黄色素损失率均小于20%,pH在5~9内,色素损失率小于10%。其中pH分别为3、11时,损失率分别为14%和18%,表明栀子黄色素pH稳定性好。在酸碱环境中,栀子黄色素颜色略有差异。观察发现,在酸性条件下栀子黄色素呈橙黄色,在中性和碱性条件下呈亮黄色。碱性条件下色素稳定性和色相更适宜食品加工所用。天然色素大都具有色移现象,最典型的是花色苷类在酸性条件下呈红色,中性呈紫色,而在碱性条件下呈蓝色[14]。栀子黄色素中含有多个不饱和共轭双键,易受亲电试剂H+作用而氧化为饱和烃,色素特征吸收峰向紫外区漂移,发生色移和褪色。这也很好地解释了栀子黄色素在碱性条件下稳定性和色度优于在酸性条件下的原因。
另外从图中可发现,在酸碱环境中前2 h内色素损失率增加最快,达到8 h内总色素损失率的50%左右,而6 h后色素损失率趋于稳定。加工应用中可通过调整色素所在食品体系的酸碱度和减少酸碱处理时间的方法来降低和防止色素褪色。
2.2.2?温度对栀子黄色素稳定性的影响。
由图3可知,随着热处理温度和加热时间的提高,栀子黄色素损失率呈直线上升趋势。100 ℃、60 ℃和25 ℃(室温)条件下水浴加热8 h后栀子黄色素损失率分别约为70%、35%和15%,而在热处理2 h以内,色素损失率均小于20%。双因素方差分析表明,处理温度和处理时间对栀子黄色素损失率影响均显著(P≤0.05),而处理时间对色素稳定性影响更显著。
数据表明生产应用中降低热处理时间和温度是保持色素稳定性的良好方法,建议热处理时间不宜超过2 h。
2.2.3?光照条件对栀子黄色素稳定性的影响。
由图4可知,太阳光直射曝光8 h后栀子黄色素损失率达18%,而室内自然光和室内避光处理差异不显著,色素损失率在8%左右,表明生产中应当避免阳光直射。文献表明天然萝卜红色素[15]、马齿苋红素[16]和蓝莓色素[17]均表现出良好的耐日光性,而栀子黄色素耐日光性相对较差。方差分析表明曝光时间对色素损失率的影响是显著的(P≤0.05),生产应用中应当控制产品曝光时间和避光处理。
2.2.4?H2O2氧化剂对栀子黄色素稳定性的影响。
由图5可知,H2O2氧化剂对栀子黄色素稳定性有破坏作用,持续处理8 h后,0.3% H2O2的栀子黄色素溶液的色素损失率接近20%,而0.2%和0.1% H2O2的色素损失率差异不显著,为13%左右。与文献所报道的黑米色素氧化稳定性比较,栀子黄色素在强氧化剂H2O2中表现出良好的氧化稳定性[18]。栀子黄色素特殊的共轭双键抗氧化能力,也是其实现抗疲劳和抗衰老生物活性的主要原因[5,19]。但生产中也应避免氧化剂的共混,可在不影响产品风味和其他质量指标的前提下,通过添加抗坏血酸、异抗坏血酸钠等食品级抗氧化剂,延缓色素的褪色,提高色素稳定性。
2.2.5?Na2SO3还原剂对栀子黄色素稳定性的影响。由图6可知,0.1%、0.2%和0.3% 浓度Na2SO3在处理8 h内,色素损失率均小于15%。方差分析表明,Na2SO3浓度和处理时间2个因素对栀子黄色素损失率的影响均无显著影响(P≥0.05),表明栀子黄色素在还原剂Na2SO3环境中表现出良好的稳定性。
2.2.6?金属离子对栀子黄色素稳定性的影响。
选择食品加工体系中常见金属离子盐溶液,如NaCl、Na2CO3、CaCl2、CuSO4以及FeCl3,考察上述金属离子溶液对栀子黄色素损失率的影响,结果如图7所示。由图7可知,0.2%(M/V)NaCl、Na2CO3、CaCl2、CuSO4溶液与栀子黄色素溶液共混8 h后,其色素损失率均小于10%左右,而0.2%(M/V)FeCl3中Fe3+对栀子黄色素损失率影响极显著(P≤0.01),在2 h时色素损失率已达80%,并且色素溶液为褐色。表明食品共混体系中Na+、Ca2+、Cu2+、Cl-、CO32-、SO42-对栀子黄色素损失率影响不显著,而Fe3+对其损失率影响极显著。试验结果表明在栀子黄色素加工、应用、储存、运输中,要避免铁制金属容器和工具的接触,可通过塑料容器或其他非金属器具的替换,同时加入金属螯合剂如EDTA-Na2来降低金属离子对色素稳定性的影响。
2.3?栀子黄色素在食品加工体系中的应用分析
栀子黄色素是一种易溶于水,化学性质稳定,色泽鲜艳的天然黄色素,主要成分物质为藏花素和藏花酸,是我国《食品安全法》允许限量使用的食品色素,同时也是卫生部公布的第一批既是食品又是药品的保健食品栀子黄中的主要功能活性物质。按照GB2760—2011《食品添加剂使用卫生标准》规定,栀子黄色素可广泛用于饮料、糕点、糖果、罐头等食品制作中,尤其对蛋白质、淀粉等具有优良的染色能力,建议最大使用量为0.3 g/kg。但是栀子黄色素原料纯度、食品共混体系成分以及贮运环境对其稳定性影响依然十分显著,因此分析和探讨食品加工体系对其稳定性影响因素及防治措施是十分有意义的。
首先天然栀子黄色素中含有栀子苷,其在蛋白酶或β-葡萄糖苷酶的作用下易与伯氨基化合物发生反应而生成栀子蓝色素,呈现绿色[20]。因此,需提高色素提取和纯化水平,选用纯度较高的色素,降低色素中栀子苷含量,防止在糕点类产品应用中发生变色[21]。其次食品体系往往是复杂的胶体共混体系,可利用胶体体系如β-环糊精包埋特性,与栀子黄色素形成1∶1包合物,使色素长链结构进入β-环糊精疏水内腔,通过改变色素所处微环境,抑制光、热、酸碱、氧化等因素引起的褪色反应,增强色素的稳定性[22]。另外可利用食品体系中EDTA-Na2、多聚磷酸钠盐、咖啡酰奎宁酸等多种共混添加物质的鳌合特性,作为色素护色剂,提高色素稳定?性,防止褪色。最后,金属三价铁离子作为亲和试剂易引起栀子黄色素褪色,生产中应当避免使用铁制容器或工具。
3?结论
开展常见食品加工环境如酸碱、温度、光照、金属离子、氧化剂和还原剂对栀子黄色素损失率影响的调查,阐明pH、高温、日光照射、Fe3+、H2O2和Na2CO3等因素对色素稳定性破坏程度,同时开展食品体系中栀子黄色素应用分析。结果表明,栀子黄色素在pH 3~11内稳定性良好,短时耐热性良好,避光稳定性良好,0.3% H2O2氧化剂和Na2CO3还原剂环境中色素稳定性良好,在NaCl、Na2CO3、CaCl2、CuSO4盐溶液体系中性质稳定,但在Fe3+环境中易于褪色。建议通过提高色素纯度,降低栀子苷含量和利用β-环糊精、EDTA-Na2等食品胶体共混体系包埋、鳌合特性,提高栀子黄色素稳定性,避免使用金属铁制容器和工具。该研究结果为栀子黄色素在食品中的应用提供了基础参考依据。
参考文献
[1] 陈毅怡,刘晓静,曾晓房,等.食用天然紅色素的研究进展[J].广州化工,2017,45(23):6-8.
[2] 徐娟,涂炳坤,邓先珍,等.栀子成分开发利用研究进展[J].湖北林业科技,2005(6):42-46.
[3] LEE I A,LEE J H,BAEK N I,et al.Antihyperlipidemic effect of crocin isolated from the fructus of Gardenia jasminoides and its metabolite crocetin[J].Biological and pharmaceutical bulletin,2005,28(11):2106-2110.
[4] ATTOE E L,VON ELBE J H.Photochemial degradation of betanine and selected anthocyanins[J].Journal of food science,1981,46(6):1934-1937.
[5] 李茂星,王先敏,毛婷,等.栀子黄色素对模拟高原缺氧小鼠运动性疲劳的改善作用[J].解放军药学学报,2017,33(1):28-32.
[6] 刘建,孟春丽.水提取天然栀子黄色素稳定性研究[J].针织工业,2008(4):55-57.
[7] 李卫,邵友元,胡立新.栀子黄色素的提取工艺及热分析[J].冷饮与速冻食品工业,2002,8(2):29-31.
[8] 王帆林,武巧,胡娜娜,等.栀子黄色素提取工艺优化及品质评价研究[J].生物化工,2016,2(1):4-6.
[9] 姚超.栀子品质评价及其黄色素制备研究[D].南宁:广西中医药大学,2017.
[10] 张伦,林华庆,余楚钦,等.栀子黄色素溶液稳定性的影响因素研究[J].中国药房,2016,27(10):1370-1373.
[11] 张兆英,张亚楠,赵慧慧.金丝小枣红色素最佳提取条件及稳定性[J].北方园艺,2019(24):111-117.
[12] 邹玉红,郭琳,寇小燕.枣皮红色素提取工艺的优化及稳定性研究[J].安徽农业科学,2012,40(25):12659-12661.
[13] 张伦.天然栀子黄色素稳定性的研究与应用[D].广州:广东药科大学,2016.
[14] 江澜.紫薯花色苷的提取纯化分析及其应用[D].保定:河北农业大学,2015.
[15] 廖远东,刘顺字,陈文田.2种天然红色色素的稳定性及其在果汁饮料中的应用效果探析[J].饮料工业,2019,22(6):28-31.
[16] 陈红,朱宝伟,梁海,等.微波辅助提取马齿苋红色素及稳定性研究[J].广州化工,2018,46(21):58-60.
[17] 赵慧芳,姚蓓,吴文龙,等.蓝莓色素的光热和化学稳定性研究[J].食品安全质量检测学报,2016,7(12):4939-4945.
[18] 曹利慧.黑米色素稳定性研究[J].安徽化工,2019,45(5):66-69.
[19] 郝昭琳,江璐,车会莲,等.栀子苷和栀子黄色素改善睡眠作用的研究[J].食品科学,2009,30(15):208-210.
[20] 张德权,吕飞杰,台建祥,等.用大孔树脂纯化栀子黄色素的研究[J].农业工程学报,2004,20(4):165-167.
[21] 叶杭菊.栀子黄色素的绿变原因及防止法[J].食品科学,1988(4):16-19.
[22] 刘伟,黄立新,张彩虹,等.不同干燥方法对栀子黄色素品质的影响[J].食品工业科技,2012,33(10):257-259.
- 多元化护理干预在手、足外伤患者中的应用效果
- 全程护理干预对儿童视频脑电图监测伪差的影响
- 循证护理对糖尿病周围神经病变患者自我效能及负面情绪的影响
- 鱼腥草药浴配合莫匹罗星软膏治疗新生儿毒性红斑的效果
- 综合护理模式在股骨粗隆间骨折患者中的应用效果
- 优质护理在继发性高血压并发脑出血护理中的应用
- 静脉溶栓治疗需遵循个体化原则
- 独活寄生汤对胶原诱导性关节炎大鼠免疫功能的影响
- 影响子宫内膜不典型增生诊断及病理升级的相关因素分析
- 数字化阅片在病理诊断中的可重复性和正确率研究
- 初中流动儿童生活事件、心理弹性与孤独感的调查研究
- 手工与清洗机清洗消毒对使用后呼吸机外管路的清洗消毒效果对比
- 小儿神经内科住院医师规范化培训面临的挑战和对策分析
- 智能时代医院信息化建设面临的挑战及对策
- 我院门诊“一站式服务中心”的实践效果
- 盐酸达克罗宁胶浆在结肠镜检查中的应用效果
- 右美托咪定在重症监护病房谵妄治疗中的应用价值
- 不同透析用血管通路对老年维持性血液透析患者左心室肥厚及功能的影响
- 左氧氟沙星和莫西沙星治疗耐多药肺结核病的临床效果比较
- 无痛肠镜结合复方聚乙二醇电解质散在老年结肠息肉中的治疗效果
- 沙库巴曲缬沙坦钠治疗慢性心力衰竭的效果
- 厄贝沙坦联合心可舒治疗腹型肥胖合并原发性高血压、高血脂患者的临床效果
- 奥美拉唑、奥曲肽联合康复新液治疗急性上消化道出血的效果 ·
- 气管镜下肺泡灌洗治疗阻塞性肺不张的效果
- 复方甲氧那明联合孟鲁司特钠治疗咳嗽变异性哮喘的临床效果
- pimpish
- pimple
- pimpled
- pimplelike
- pimples
- pimpliest
- pimpliness
- pimply
- pimps
- pin
- pinafore
- pinafored
- pinafores
- pinball
- pinballed
- pinballs
- pincer
- pincers
- pinch
- pinchable
- pinched
- pincher
- pinches
- pinch-hit
- pinch hit
- 颐指气役
- 颐指色授
- 颐指进退
- 颐指风使
- 颐摄
- 颐旨
- 颐气
- 颐灵
- 颐然
- 颐爱
- 颐生
- 颐真
- 颐示
- 颐神
- 颐神保年
- 颐神养寿颐精养寿
- 颐神养志
- 颐神养性
- 颐神养气
- 颐福
- 颐精养气
- 颐精养神
- 颐绥
- 颐老
- 颐育