基于3D Max探究判断分子中心原子杂化类型的方法
高茹婷 彭庆蓉 刘丰茂
【摘要】提供一种可以判断常见分子和离子中心原子杂化类型的方法,即画出分子合适的电子式,用3D Max转换成空间立体构型,根据原子间斥力最小的原则可以判断出分子的空间构型,进而利用价层电子对互斥模型来判断分子中心原子杂化类型。
【关键词】电子式 3D Max 杂化轨道理论 中心原子杂化类型 价层电子对互斥模型
利用杂化轨道理论,在已知分子的空间构型,可以判断分子或部分离子的中心原子的杂化类型;利用VSEPR模型可以预测分子或部分离子的空间构型,但需要结合中心原子杂化理论才能确定中心原子杂化类型,所以教学的过程基本是将两种理论结合。然而,对于初次接触这两种理论的学生,如果没有一定的空间感知能力,想象出空间构型是比较困难的,或者容易把所接触到的分子杂化类型以及空间构型弄混淆。有人提到了一种利用电子式的观察法,但并没有详细说明应该怎样利用。本文介绍一种让刚升入大学的学生清晰、快速掌握这两种理论并且可判断中心原子杂化类型的方法,即画出电子式,用3D Max转换成空间立体构型,然后根据VSEPR理论和杂化轨道理论推测出中心原子杂化类型。此方法适用于由主族元素组成的无机化合物和少量碳四以内有机化合物。
一、根据分子最外层电子数目画出分子的电子式
在画电子式时,要满足两个条件:(1)保证每个原子提供电子数为其价层电子数,并且中心原子为其他每一个原子提供电子,而且能得到其他任意一个原子提供的电子,在原子间形成电子对。如果中心原子或者其他原子电子不够,电子对中的电子均源于同一原子,则形成配位键。比如,铵根离子(NH4)其中一个氢原子失去一个电子变成氢离子,不能够给氮原子提供电子,这个氢离子和氮原子之间的电子全部由氮原子提供,进而形成配位键。(2)使分子中每个原子最外层电子均达到稳定结构。若部分原子无法达到稳定结构,则要满足除中心原子外其他原子均满足稳定结构,此类化合物一般会形成离域键。(3)补充说明离域键。部分中心原子无法达到稳定结构的分子,是因为形成化学键的π电子不局限于两个原子的区域,而是在参加成键的多个原子的分子骨架中运动,这种由多个原子形成的π型化学键称作离域π键。但是对于这类分子,依旧可以画出其电子式,只需要满足除中心原子外其他原子达到稳定结构。如表二氧化硫(SO2)分子电子式和二氧化氮(NO2)分子电子式,这两个电子式中,中心原子都未满足稳定结构。
二、确定分子空间构型
根据分子的二维电子式图,将其变成三维空间图像。由排斥力大小为孤对电子-孤对电子>成键电子-孤对电子>成键电子-成键电子,且在键长一定的情况下互相间距离越远越稳定,根据最小排斥原则,可判断分子空间构型。为了让学生能够直观的看到空间模型,更好地理解理论,可以采用两种方法。
1.如果时间充裕,让学生们用简单的材料自己制作分子模型。比如,用粘土或者是易得的橡皮泥和木棒搭建模型,帮助学生想象和理解几何图形,将几何图形与分子形状连接起来,让学生能够理解分子在空间的排列,最后引入更抽象的价电子对排斥理论。
2.如果时间不够充裕,教师可以利用3Dmax软件更好的讲解。本文以3ds max2015版为例,进行说明。这个软件的优点是可以看到分子模型的空间立体结构,也可以看到分子主视图、左视图、俯视图的透视结构,同时在调整位置过程中通过看每一个结构的x、y、z坐标和三视图,进而可以更直观的感受到原子的相对位置。教师既可以做好了模型展示给学生,也可以直接一边做一边展示。
3.为了让学生更好地掌握结构,可以将阅读和写作结合使用,以促进通常由死记硬背学习的主题的概念性学习。让学生通过查找很久以前的相关文章,试着自己编写论文的摘要来解释关键点,试着自己画出电子式。它还使教师能够看到学生的学习成果。
三、根据分子空间构型推断VSEPR模型和中心原子杂化类型
为了便于判断,需要将未成键的孤对电子甚至是单电子看成键电子,再根据最小排斥力原则,确定VSEPR模型。最后,根据VSEPR模型,考虑需要中心原子最多可形成几条共价键,进而考虑需要多少条杂化轨道。再根据杂化理论判断中心原子杂化类型。
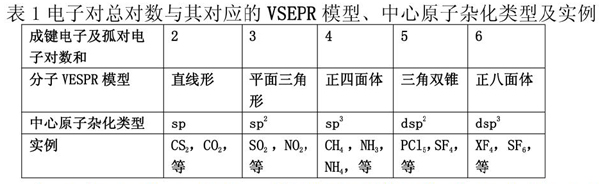
利用這种方法,可以先列出一个成键电子及孤对电子的总对数与VSEPR模型、杂化类型、相应的分子及其电子式(如表1所示),然后分析推断中心原子杂化类型的成因。
本文提出的方法是,教师在讲授的过程中做出电子式和3Dmax立体结构,时间充裕,让学生自己做出立体模型,或者是通过论文摘要写作。
这样让学生更直观的理解和记忆分子空间结构、VSEPR结构和中心原子杂化类型;而且无论是电子式还是3Dmax软件,都容易操作和掌握,是一种高效的学习方式。
但是,由于过渡金属有d轨道参与轨道杂化成键,中心原子杂化轨道与主族元素的p轨道参与形成的杂化轨道不同,这种方法不适合过度金属,部分特殊情况仍需要单独记忆。
参考文献:
[1]揭念芹.基础化学(无机及分析化学).第二版[M].北京:科学出版社,2016.7.57.61.
[2]席改卿.杂化轨道理论与价层电子对互斥理论的互补性[J].邯郸师专学报,2000,(3):46.
[3]卢国锋,卢敬萱.中心原子杂化类型的确定方法与应用.化学教学,2012,(07):70.
[4]周公度,段连运.结构化学基础(第四版)[M].北京:北京大学出版社,2008.149-155.162-163.
[5]大连理工大学无机化学教研室.无机化学(第四版)[M].北京:高等教育出版社,2004.260.
[6]Kelley J.Donaghy and Kathleen J.Saxton. Connecting Geometry and Chemistry:A Three-Step Approach to Three-Dimensional Thinking.Journal of Chemical Education,2012,(7):917-920.
[7]Shultz G V,Gere A R.Writing-to-Learn the Nature of Science in the Context of the Lewis Dot Structure Model[J].Journal of Chemical Education,2015,(8).

